名校
1 . 下列类比推理的结果正确的是
| A.Na能在空气中燃烧生成Na2O2,故同主族的Li在空气中燃烧生成Li2O2 |
| B.H2S与SO2能反应生成S,故NH3与NO2能在一定条件下反应生成N2 |
| C.Al(OH)3无法通过化合反应制取,推测Fe(OH)3也无法通过化合反应制取 |
| D. Na2O2与CO2反应生成Na2CO3和O2,故Na2O2与SO2反应生成Na2SO3和O2 |
您最近一年使用:0次
名校
2 . 使用下列装置及试剂,可以实现元素不同价态之间的转化的是
| 选项 | 转化 | 试剂a | 试剂b | 试剂c |
|
| A | 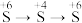 | 浓硫酸 | Cu |  溶液 溶液 | |
| B | 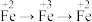 | 稀硫酸 | FeS |  溶液 溶液 | |
| C | 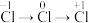 | 浓盐酸 |  | 水 | |
| D | 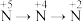 | 浓硝酸 | Cu | 水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 钼酸铵[(NH4)2MoO4]是生产高纯度钼制品、钼催化剂、钼颜料等的基本原料。一种以钼精矿(主要含MoS2,还含有少量SiO2、As、Sn、P、Cu、Pb、CaO)为原料制备钼酸铵的工艺流程如图所示: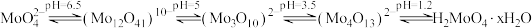 回答下列问题:
回答下列问题:
(1)锡为主族元素,在周期表中的位置是___________ ,(NH4)2MoO4中Mo元素的化合价为___________ 价。
(2)“氧化焙烧”时MoS2转化为MoO3,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(3)“除铜”时选择在60~80℃的条件下进行的原因为___________ 。
(4)“沉淀”过程中加入H2SO4调节溶液pH=2.1,则所得沉淀的化学式为___________ ,加入氨水后生成(NH4)2MoO4的化学方程式为___________ 。
(5)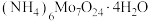 的热重曲线如图所示:
的热重曲线如图所示: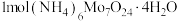 在A点失去H2O的物质的量为
在A点失去H2O的物质的量为___________ ,B点所得的物质为___________ (填化学式)。

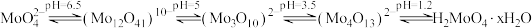 回答下列问题:
回答下列问题:(1)锡为主族元素,在周期表中的位置是
(2)“氧化焙烧”时MoS2转化为MoO3,该反应中氧化剂与还原剂的物质的量之比为
(3)“除铜”时选择在60~80℃的条件下进行的原因为
(4)“沉淀”过程中加入H2SO4调节溶液pH=2.1,则所得沉淀的化学式为
(5)
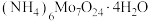 的热重曲线如图所示:
的热重曲线如图所示: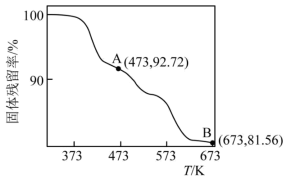
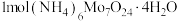 在A点失去H2O的物质的量为
在A点失去H2O的物质的量为
您最近一年使用:0次
4 . 海水中溴元素以 形式存在,工业上用“空气吹出法”从海水中提取溴的工艺流程如图:
形式存在,工业上用“空气吹出法”从海水中提取溴的工艺流程如图:不正确 的是
 形式存在,工业上用“空气吹出法”从海水中提取溴的工艺流程如图:
形式存在,工业上用“空气吹出法”从海水中提取溴的工艺流程如图: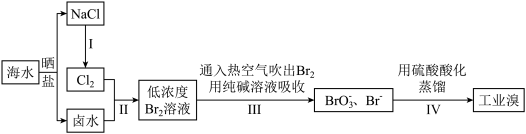
| A.步骤Ⅰ工业上通常用电解饱和食盐水来实现 |
B.步骤Ⅱ通入 的同时需进行酸化,以减少副反应 的同时需进行酸化,以减少副反应 |
C.步骤Ⅲ的反应中氧化产物与还原产物的物质的量之比为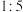 |
D.步骤Ⅳ中 发生的反应的离子方程式: 发生的反应的离子方程式: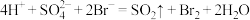 |
您最近一年使用:0次
名校
解题方法
5 . 下列反应的离子方程式书写正确的是
A.氯气通入冷的氢氧化钠溶液中: |
B.过量 通入 通入 溶液: 溶液: |
C.将足量 通入 通入 溶液中: 溶液中: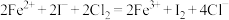 |
D.向水中加入金属钠: |
您最近一年使用:0次
名校
6 . 下列各组离子在溶液中能够大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
解题方法
7 . 已知:氧化还原反应可看成由两个半反应组成,每个半反应具有一定的电极电势(用“E”表示),E越大则该电对中氧化型物质的氧化性越强,E越低则该电对中还原型物质的还原性越强。下表为部分电极的电极电势。根据表格数据分析,下列说法中错误的是
下列说法错误的是
| 氧化还原电对(氧化型/还原型) | 电极电势(E/V) | 氧化还原电对(氧化型/还原型) | 电极电势(E/V) |
 | 0.77 | 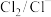 | 1.36 |
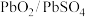 (或 (或 ) ) | 1.69 | 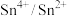 | 0.151 |
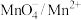 | 1.51 |  | 0.54 |
| A.向含0.2molFeCl2的溶液中加0.1molPbO2,滴加KSCN溶液,可观察到溶液变红 |
| B.往淀粉-KI溶液中滴加SnCl4溶液,溶液不变蓝 |
C.还原性: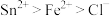 |
| D.酸化高锰酸钾溶液时,可使用盐酸 |
您最近一年使用:0次
8 . 某课外小组为探究金属铜的还原性,进行如下实验:①将金属铜投入用 酸化的
酸化的 的
的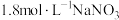 溶液中,现象不明显②将金属铜投入用盐酸酸化的
溶液中,现象不明显②将金属铜投入用盐酸酸化的 的
的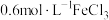 溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用
溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用 酸化的
酸化的 的
的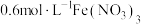 溶液中,铜粉溶解,溶液变为深棕色[经检验含
溶液中,铜粉溶解,溶液变为深棕色[经检验含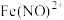 ],无气泡生成。下列分析正确的是
],无气泡生成。下列分析正确的是
 酸化的
酸化的 的
的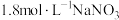 溶液中,现象不明显②将金属铜投入用盐酸酸化的
溶液中,现象不明显②将金属铜投入用盐酸酸化的 的
的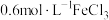 溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用
溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用 酸化的
酸化的 的
的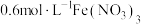 溶液中,铜粉溶解,溶液变为深棕色[经检验含
溶液中,铜粉溶解,溶液变为深棕色[经检验含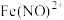 ],无气泡生成。下列分析正确的是
],无气泡生成。下列分析正确的是A.①说明 的 的 溶液不与铜粉反应 溶液不与铜粉反应 |
B.②证明氧化性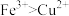 还原性 还原性 |
C.③中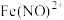 的生成速率一定小于 的生成速率一定小于 被还原的速率 被还原的速率 |
| D.在①中加入少量绿矾,铜粉可溶解,溶液变为深棕色 |
您最近一年使用:0次
9 . H、C、N、O是自然界和化学研究中最重要的四种元素。下列有关说法错误的是
A. 、 、 有还原性 有还原性 | B.C有多种同位素和同素异形体 |
| C.浓硝酸可用于苯的硝化反应 | D. 参与的反应一定为氧化还原反应 参与的反应一定为氧化还原反应 |
您最近一年使用:0次
名校
解题方法
10 . 下列说法或有关反应的离子方程式不正确 的是
A.与Al反应能放出H2的溶液中:NO 、Na+、Fe3+、SO 、Na+、Fe3+、SO 一定不能大量共存 一定不能大量共存 |
B.铅酸蓄电池充电时的阳极反应: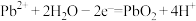 |
C.乙酰甲胺在稀盐酸中水解: |
D.向含溶质a mol的FeBr2溶液中通入b mol Cl2,充分反应,当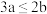 时,反应的离子方程式为: 时,反应的离子方程式为: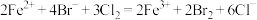 |
您最近一年使用:0次




