名校
1 . 物质的应用性是化学科学研究的重要内容。下列物质的性质与用途不具有 对应关系的是
A. 有漂白性,故能使酸性高锰酸钾溶液褪色 有漂白性,故能使酸性高锰酸钾溶液褪色 |
B.浓硫酸有吸水性,故可以干燥 |
| C.液氨汽化时要吸收大量的热,可用作制冷剂 |
D. 有强氧化性,故可以作自来水的消毒剂 有强氧化性,故可以作自来水的消毒剂 |
您最近一年使用:0次
名校
解题方法
2 . 化学与社会、生活以及工业生产密切相关。下列说法不正确 的是
| A.用铝槽车可以运输浓硫酸 | B.二氧化硫不能用于食品加工 |
| C.氮氧化物可以引起呼吸道疾病 | D.水玻璃可以做粘合剂和防火剂 |
您最近一年使用:0次
名校
3 . 下列说法正确的是
| A.工业上常用氧化钠和水的反应制取氢氧化钠 |
| B.氯气可用于制造盐酸、农药和药品等 |
| C.铝制餐具可长时间存放酸性或碱性食物 |
| D.二氧化硫有毒,不能用作食品添加剂 |
您最近一年使用:0次
4 . 下列有关“实验”栏目中说法正确的是
| A.干燥的氯气能使有色鲜花变色,原因是氯气具有漂白性 |
| B.浓硫酸能使蔗糖变黑,原因是浓硫酸具有吸水性 |
| C.乙烯能使溴的四氯化碳溶液褪色,也能使高锰酸钾溶液褪色,两者原理不相同 |
| D.向蔗糖溶液中加入几滴稀硫酸,煮沸后冷却,加入银氨溶液,没有银镜,说明蔗糖未水解 |
您最近一年使用:0次
名校
5 . 下列物质的名称与化学式对应不正确 的是
A.生石灰: | B.芒硝: |
C.金刚砂: | D.黄铁矿: |
您最近一年使用:0次
名校
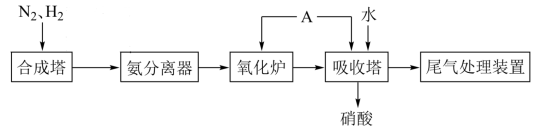
6 . 下图为合成氨以及氨氧化制硝酸的流程示意图。
(1)物质A(纯净物)的化学式是___________ 。
(2)写出吸收塔中发生反应的离子方程式___________ 。
(3)为避免硝酸生产尾气中的氮氧化物污染环境,可以采用催化还原法处理尾气。写出使用氨气处理二氧化氮尾气的化学方程式___________ 。
(4)下列说法不正确 的是___________。
(1)物质A(纯净物)的化学式是
(2)写出吸收塔中发生反应的离子方程式
(3)为避免硝酸生产尾气中的氮氧化物污染环境,可以采用催化还原法处理尾气。写出使用氨气处理二氧化氮尾气的化学方程式
(4)下列说法
| A.铝的化学性质活泼,不能作为罐体材料盛装大量浓硝酸 |
| B.合成氨工业是最主要的人工固氮的途径 |
| C.氨极易溶于水,可形成喷泉实验 |
| D.工业制硝酸和制硫酸中都需要吸收塔装置,利用水吸收相应气体 |
您最近一年使用:0次
7 . 绿矾具有广泛的用途,下列说法不正确的是
| A.医疗上常用于治疗缺铁性贫血 |
| B.工业常用作污水的处理剂,是利用其还原性 |
C.高温分解产生 、 、 和 和 |
| D.可用KSCN溶液检验其是否变质 |
您最近一年使用:0次
名校
8 . 回答下列问题:
(1)①写出NH3的电子式_______ ;
②甘氨酸的结构简式为_______ 。
(2)写出碳和浓硫酸加热时发生反应的化学方程式_______ ;
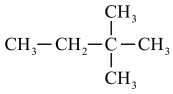
(3)图的系统命名法的名称_______ ,其二氯代物有_______ 种。
(1)①写出NH3的电子式
②甘氨酸的结构简式为
(2)写出碳和浓硫酸加热时发生反应的化学方程式
(3)图的系统命名法的名称
您最近一年使用:0次
名校
解题方法
9 . 根据实验操作和和现象得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 将 和 和 分别装入两支试管,滴入 分别装入两支试管,滴入 溶液。前者不溶,后者溶解 溶液。前者不溶,后者溶解 | Mg的金属性大于Al |
B | 试管中加入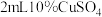 溶液,滴加5滴5%NaOH溶液,再加入2mL尿液,加热后无砖红色沉淀出现 溶液,滴加5滴5%NaOH溶液,再加入2mL尿液,加热后无砖红色沉淀出现 | 尿液中没有葡萄糖 |
C | 淀粉和稀硫酸混合加热,冷却后加入足量NaOH溶液,取少量中和液加入碘水未变蓝 | 淀粉已水解完全 |
D | 某溶液中滴加 酸化的 酸化的 溶液,出现白色沉淀 溶液,出现白色沉淀 | 溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
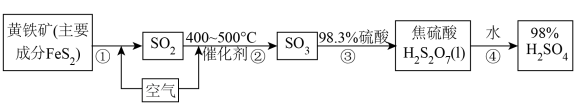
10 . 工业上用黄铁矿为原料制备硫酸的流程如图所示:
(1)已知FeS2的阴离子达到稳定结构,则FeS2的电子式为___________ 。
(2)已知: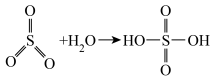 ,请写出焦硫酸的结构式
,请写出焦硫酸的结构式___________ 。
(3)写出步骤①的化学方程式___________ 。
(4)室温下,SO3为液体,SO2为气体。SO3熔点高于SO2的原因___________ 。
(5)下列说法正确的是___________ 。
A.步骤①,产生的气体进入接触室之前无需净化处理
B.步骤②,使用催化剂能使SO2的转化率达到100%
C.步骤③,吸收设备中填充瓷环可提高SO3吸收率
D.可以预测:Na2S2O7的水溶液呈酸性,H2S2能将Fe2+氧化成Fe3+
E.17.8g H2S2O7与2.2g水充分混合后,可获得98%浓硫酸
(6)若硫铁矿煅烧不充分,则炉渣中混有+2价的铁元素,试设计一个简单的实验证明之。简述实验操作和有关的实验现象___________ 。(供选择的试剂:KSCN溶液、稀硫酸、稀盐酸、KMnO4溶液、品红溶液、NaOH溶液)
(1)已知FeS2的阴离子达到稳定结构,则FeS2的电子式为
(2)已知:
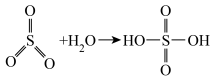 ,请写出焦硫酸的结构式
,请写出焦硫酸的结构式(3)写出步骤①的化学方程式
(4)室温下,SO3为液体,SO2为气体。SO3熔点高于SO2的原因
(5)下列说法正确的是
A.步骤①,产生的气体进入接触室之前无需净化处理
B.步骤②,使用催化剂能使SO2的转化率达到100%
C.步骤③,吸收设备中填充瓷环可提高SO3吸收率
D.可以预测:Na2S2O7的水溶液呈酸性,H2S2能将Fe2+氧化成Fe3+
E.17.8g H2S2O7与2.2g水充分混合后,可获得98%浓硫酸
(6)若硫铁矿煅烧不充分,则炉渣中混有+2价的铁元素,试设计一个简单的实验证明之。简述实验操作和有关的实验现象
您最近一年使用:0次



