名校
解题方法
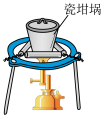
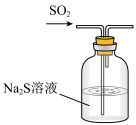
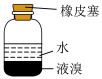
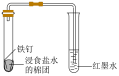
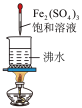
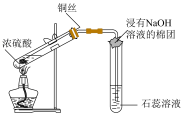
1 . 下列装置能达到实验目的的是
|
|
|
|
| A.熔化Na2CO3 | B.验证SO2氧化性 | C.实验室制CO2 | D.实验室保存液溴 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-05更新
|
353次组卷
|
4卷引用:2024届浙江省金华市义乌市高三下学期三模化学试题
2024届浙江省金华市义乌市高三下学期三模化学试题(已下线)湖南师大附中2024届高三下学期第三次模拟考试化学试题广西壮族自治区贵港市2024届高三下学期收网考化学试题黑龙江省大庆市实验中学实验二部2023-2024学年高三下学期阶段考试(二)化学试题
名校
解题方法
2 . 下列实验操作及现象与实验结论不相符的是
| 选项 | 实验目的 | 实验操作及现象 | 实验结论 |
| A | 检验乙醇中是否含有水 | 向乙醇中加入无水硫酸铜固体,固体变浅蓝色 | 乙醇中含有水 |
| B | 检验某溶液中是否含 | 向某溶液中滴加硝酸酸化的 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 该溶液中可能含有 |
| C | 配制1.00 的 的 溶液 溶液 | 称取10.6g  固体于100mL容量瓶中,加入蒸馏水溶解至液面与容量瓶刻度线相平 固体于100mL容量瓶中,加入蒸馏水溶解至液面与容量瓶刻度线相平 | 成功配制1.00 的 的 溶液 溶液 |
| D | 探究 的还原性 的还原性 | 向盛有硫酸亚铁溶液的试管中滴加几滴KSCN溶液,振荡,再滴加几滴新制的氯水,溶液呈红色 |  具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-29更新
|
687次组卷
|
8卷引用:2024届浙江省舟山中学高三下学期模拟预测化学试题
名校
解题方法
3 . 工业上由黄铁矿(主要成分为 ,含As、Se等杂质)生产发烟硫酸的主要工艺流程如图所示:
,含As、Se等杂质)生产发烟硫酸的主要工艺流程如图所示:
 ,含As、Se等杂质)生产发烟硫酸的主要工艺流程如图所示:
,含As、Se等杂质)生产发烟硫酸的主要工艺流程如图所示:
| A.“煅烧”时可将黄铁矿粉从炉顶加入、富氧空气从炉底通入 |
| B.“干燥”可防止部分金属设备被水蒸气腐蚀 |
C.“吸收”中所得尾气的主要成分是未被吸收的 |
D.若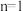 ,则 ,则 的结构式可能为 的结构式可能为 |
您最近一年使用:0次
2024-05-29更新
|
161次组卷
|
2卷引用:2024届浙江省舟山中学高三下学期模拟预测化学试题
名校
解题方法
4 . 从饱和AlCl3溶液中制备无水AlCl3固体,某小组设计方案如下所示,下列说法不正确 的是
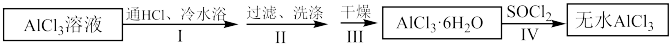
| A.步骤Ⅰ通入HCl的作用是抑制AlCl3水解并有利于AlCl3⋅6H2O结晶 |
| B.步骤Ⅱ洗涤用的洗涤剂是水 |
| C.步骤Ⅲ可采用减压干燥或低温干燥 |
| D.步骤Ⅳ试剂SOCl2与水反应的产物可使品红溶液褪色 |
您最近一年使用:0次
5 . 利用下列装置(夹持装置省略)进行实验,能达到实验目的的是
|
|
| A.证明氯水中有酸 | B.观察铁的的吸氧腐蚀 |
|
|
| C.制备Fe(OH)3胶体 | D.检验二氧化硫的漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 一种制备 的工艺路线如图所示,反应②所得溶液
的工艺路线如图所示,反应②所得溶液 在3~4之间,反应③需及时补充
在3~4之间,反应③需及时补充 以保持反应在
以保持反应在 条件下进行。
条件下进行。 的电离平衡常数
的电离平衡常数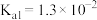 ,
,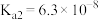 。请回答:
。请回答:
(1)溶液①中阴离子浓度大小(用“>”表示):___________ 。
(2)下列说法正确的是___________。
(3)写出反应③的化学方程式:___________ 。
(4)“低温真空蒸发”可防止 被氧化。请设计实验证明
被氧化。请设计实验证明 是否被氧化
是否被氧化___________ 。若 部分被氧化,为不降低
部分被氧化,为不降低 的产率,补充
的产率,补充 的量应适当
的量应适当___________ (填“增加”“减少”或“不变”)。
 的工艺路线如图所示,反应②所得溶液
的工艺路线如图所示,反应②所得溶液 在3~4之间,反应③需及时补充
在3~4之间,反应③需及时补充 以保持反应在
以保持反应在 条件下进行。
条件下进行。
 的电离平衡常数
的电离平衡常数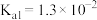 ,
,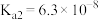 。请回答:
。请回答:(1)溶液①中阴离子浓度大小(用“>”表示):
(2)下列说法正确的是___________。
| A.反应①、②和③均为氧化还原反应 |
| B.气体①和②是造成酸雨的主要成分 |
| C.往反应①后的溶液中加水可得到硫酸铜溶液 |
| D.溶液Y可循环用于反应②进行吸收气体① |
(3)写出反应③的化学方程式:
(4)“低温真空蒸发”可防止
 被氧化。请设计实验证明
被氧化。请设计实验证明 是否被氧化
是否被氧化 部分被氧化,为不降低
部分被氧化,为不降低 的产率,补充
的产率,补充 的量应适当
的量应适当
您最近一年使用:0次
2024-04-15更新
|
278次组卷
|
2卷引用:浙江省金华市十校2023-2024学年高三下学期4月模拟考试化学试题
7 . 下列有关工业制硫酸的说法正确的是
A.一般以硫磺或黄铁矿(主要成分: )为原料 )为原料 |
B.鼓入足量的空气,原料可直接转化为 |
C.用水吸收 ,可提高吸收效率 ,可提高吸收效率 |
D.含 的废气经回收可用于制备硫酸 的废气经回收可用于制备硫酸 |
您最近一年使用:0次
2024-04-15更新
|
281次组卷
|
3卷引用:浙江省金华市十校2023-2024学年高三下学期4月模拟考试化学试题
8 . Fe3S4固体是一种重要的磁性材料,以它为原料实现如下化合物的转化: 的形式存在,溶液呈亮黄色。
的形式存在,溶液呈亮黄色。
请回答:
(1)依据B→C→D的现象,判断Cl-、SCN-、CN-与Fe3+的配位能力由强到弱依次为___________ ,无色酸性溶液F中的含硫阴离子有___________ 。
(2)Fe3S4能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标准状况下的密度为1.518g∙L-1),写出该反应的离子方程式___________ 。
(3)下列说法正确的是___________。
(4)写出F→G反应的化学方程式___________ 。请设计实验方案确定溶液G中的阴离子___________ 。

 的形式存在,溶液呈亮黄色。
的形式存在,溶液呈亮黄色。请回答:
(1)依据B→C→D的现象,判断Cl-、SCN-、CN-与Fe3+的配位能力由强到弱依次为
(2)Fe3S4能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标准状况下的密度为1.518g∙L-1),写出该反应的离子方程式
(3)下列说法正确的是___________。
| A.固体A中可能含有FeO | B.无色气体E能完全溶于水 |
| C.溶液C呈酸性,是由于Fe3+水解 | D.溶液B可溶解铜 |
(4)写出F→G反应的化学方程式
您最近一年使用:0次
名校
解题方法
9 . 物质的性质决定用途和保存方式,下列两者对应关系不正确 的是
A. 见光易分解,浓硝酸用棕色瓶保存 见光易分解,浓硝酸用棕色瓶保存 |
B. 具有强氧化性,可用于杀菌消毒 具有强氧化性,可用于杀菌消毒 |
C. 具有还原性,可用于漂白纸浆 具有还原性,可用于漂白纸浆 |
D. 难溶于稀盐酸,医学上常用作“钡餐” 难溶于稀盐酸,医学上常用作“钡餐” |
您最近一年使用:0次
10 . 黄铜矿的主要成份为 ,现有如下转化关系制备有关物质。
,现有如下转化关系制备有关物质。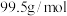 。请回答:
。请回答:
(1)尾气中 经过充分综合利用可以得到石膏,请写出石膏的化学式:
经过充分综合利用可以得到石膏,请写出石膏的化学式:___________ 。
(2)煅烧含硫量高的矿物得到高浓度的 ,干燥的
,干燥的 气体与氯气在活性炭催化下可生成一种用于有机合成的常见物质A,该物质水解时发生非氧化还原反应得到两种强酸。
气体与氯气在活性炭催化下可生成一种用于有机合成的常见物质A,该物质水解时发生非氧化还原反应得到两种强酸。
①写出物质A分子的结构式:___________ 。
②一定压强下,化合物A的沸点低于硫酸的原因是___________ 。
(3)生成沉淀D的离子反应方程式___________ 。
(4)请设计实验检验溶液C中的阳离子___________ 。
 ,现有如下转化关系制备有关物质。
,现有如下转化关系制备有关物质。
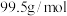 。请回答:
。请回答:(1)尾气中
 经过充分综合利用可以得到石膏,请写出石膏的化学式:
经过充分综合利用可以得到石膏,请写出石膏的化学式:(2)煅烧含硫量高的矿物得到高浓度的
 ,干燥的
,干燥的 气体与氯气在活性炭催化下可生成一种用于有机合成的常见物质A,该物质水解时发生非氧化还原反应得到两种强酸。
气体与氯气在活性炭催化下可生成一种用于有机合成的常见物质A,该物质水解时发生非氧化还原反应得到两种强酸。①写出物质A分子的结构式:
②一定压强下,化合物A的沸点低于硫酸的原因是
(3)生成沉淀D的离子反应方程式
(4)请设计实验检验溶液C中的阳离子
您最近一年使用:0次