名校
解题方法
1 . 硫酸与Cl2反应的生成物的结构如图所示。有关说法不正确的是
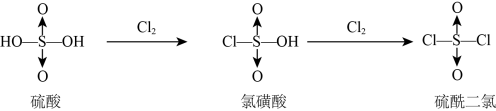
| A.氯磺酸钠NaSO3Cl与水反应:NaSO3Cl+H2O=Na++OH-+HSO3Cl- |
B.硫酰二氯与水反应的离子方程式:SO2Cl2+6H2O=4H3O++ +2Cl- +2Cl- |
| C.氯磺酸与BaCl2溶液反应的化学方程式:HSO3Cl+BaCl2+H2O=BaSO4↓+3HCl |
| D.硫酰二氯可脱去金属氯化物中的水:MgCl2·6H2O+3SO2Cl2=MgCl2+3H2SO4+6HCl |
您最近一年使用:0次
解题方法
2 . 氢溴酸是无色、易挥发的液体,在化工领域用途广泛。实验室模拟一种工业制备氢溴酸的主要流程如下:
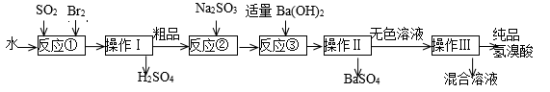
完成下列填空:
(1)写出反应①的离子方程式___________ 。该反应需要在冰水浴中进行,可能的原因是___________ 。
(2)操作I用到的玻璃仪器有蒸馏烧瓶、温度计、___________ 、接液管和锥形瓶。
(3)反应②中Na2SO3的目的是___________ 。
(4)反应③中的Ba(OH)2溶液能否用BaCl2或者Ba(NO3)2溶液代替?说明理由___________ 。
(5)工业氢溴酸往往呈淡黄色:①可能是因为像工业盐酸一样含Fe3+,②还可能是因为含___________ ,如何证明?___________ 。

完成下列填空:
(1)写出反应①的离子方程式
(2)操作I用到的玻璃仪器有蒸馏烧瓶、温度计、
(3)反应②中Na2SO3的目的是
(4)反应③中的Ba(OH)2溶液能否用BaCl2或者Ba(NO3)2溶液代替?说明理由
(5)工业氢溴酸往往呈淡黄色:①可能是因为像工业盐酸一样含Fe3+,②还可能是因为含
您最近一年使用:0次
解题方法
3 . 下列实验操作及现象均正确的是
| 选项 | 实验目的 | 实验操作 | 实验现象 |
| A | 探究硼酸和碳酸的酸性强弱 | 将足量硼酸滴入Na2CO3溶液中 | 有气泡产生 |
| B | 验证铜和浓硫酸反应的产物中有硫酸铜生成 | 直接向反应后的试管中加入蒸馏水 | 溶液变蓝 |
| C | 探究维生素C可以还原Fe3+ | 向盛有FeCl3溶液的试管中滴加适量浓维生素C溶液 | 溶液由黄色变为浅绿色 |
| D | 探究Fe3+和I-之间的反应为可逆反应 | 向氯化铁溶液中滴入少量 KI溶液,将反应后的溶液两等分,向其中一份滴入KSCN溶液,另一份滴淀粉溶液 | 一份溶液显血红色,另一份溶液显蓝色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 下列说法中不正确的有:
①氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
②测定新制氯水的pH时,先用玻璃棒蘸取液体滴在pH试纸上,再与标准比色卡对照
③用米汤直接检验食用盐中是否含有碘元素
④pH在5.6~7.0之间的降水通常称为酸雨
⑤向某溶液中加入硝酸钡溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有硫酸根的存在
⑥SO2通入紫色石蕊试液,溶液先变红后褪色
⑦沸点由高到低排序:正戊烷、异戊烷、新戊烷、正丁烷、异丁烷
⑧分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤
⑨蒸干氯化铝溶液可得纯净的无水氯化铝
①氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
②测定新制氯水的pH时,先用玻璃棒蘸取液体滴在pH试纸上,再与标准比色卡对照
③用米汤直接检验食用盐中是否含有碘元素
④pH在5.6~7.0之间的降水通常称为酸雨
⑤向某溶液中加入硝酸钡溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有硫酸根的存在
⑥SO2通入紫色石蕊试液,溶液先变红后褪色
⑦沸点由高到低排序:正戊烷、异戊烷、新戊烷、正丁烷、异丁烷
⑧分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤
⑨蒸干氯化铝溶液可得纯净的无水氯化铝
| A.5个 | B.6个 | C.7个 | D.8个 |
您最近一年使用:0次
解题方法
5 . 下列变化中,气体被还原的是
| A.将二氧化硫气体通入氢氧化钡溶液,有沉淀产生 |
| B.将氯气通入硫化钠溶液,有沉淀产生 |
| C.将硫化氢通入氯化铁溶液,有沉淀产生 |
| D.二氧化碳通过装有过氧化钠的干燥管,固体变色 |
您最近一年使用:0次
解题方法
6 . 化学与生产、生活、社会密切相关,下列有关说法正确的是
| A.河水中有许多杂质和有害细菌,加入明矾消毒杀菌后可以直接饮用 |
| B.新型冠状病毒有可能在空气中以气溶胶的形式传播,气溶胶不属于胶体 |
| C.“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量 |
| D.面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于碱性氧化物,也属于离子化合物,其阴阳离子个数比为2:1,过氧化苯甲酰属于有机物 |
您最近一年使用:0次
7 . 固体粉末X中可能含有FeO、Fe2O3、MnO2、K2SiO3、K2SO3、KAlO2、MgCl2 、K2CO3、NaNO2中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下:

根据上述实验,以下说法正确的是

根据上述实验,以下说法正确的是
| A.溶液甲中一定含有K2SiO3、NaNO2,可能含有KAlO2、K2CO3 |
| B.由于在溶液甲中加入足量稀盐酸后再加入BaCl2 溶液,因此无法判断溶液中是否有K2SO3 |
| C.气体A和气体D一定均为纯净物 |
| D.原混合物中一定含有Fe2O3 |
您最近一年使用:0次
8 . (1)化合物A、B、C、D、X之间的转化关系见下图。化合物X含三种元素,化合物D含两种元素,B是强碱、焰色反应显紫色,气体C能使湿润的红色石蕊试纸变蓝色。
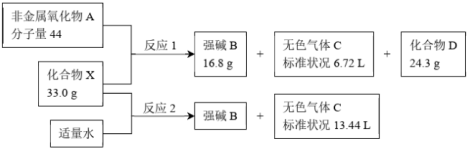
写出化合物X、D的化学式:X____ D____ 。
(2)我国科学家在金刚石压腔实验中创造出了新颖化合物X′,超过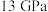 的压力下能保持稳定。5.0克X′在一定条件下完全分解为B′和0.4克A′(气体);A′的密度约为
的压力下能保持稳定。5.0克X′在一定条件下完全分解为B′和0.4克A′(气体);A′的密度约为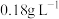 ;A′和B′物质的量之比为l:2。Y′为含有C′元素的气态氧化物,能使品红溶液褪色;C′的单质是环状分子,具有冠状结构。E′为常见无机物,将E′隔绝空气加热可得D′和F′,产生的D′和F′的物质的量之比为1:3。Y′与E′以1:1发生化合反应生成G′,假设反应过程无损耗,A′、B′、C′为单质,气体数据均为标准状况下测定:根据如下转化关系,给出A′、B′、C′、D′、E′、F′的化学式:A′
;A′和B′物质的量之比为l:2。Y′为含有C′元素的气态氧化物,能使品红溶液褪色;C′的单质是环状分子,具有冠状结构。E′为常见无机物,将E′隔绝空气加热可得D′和F′,产生的D′和F′的物质的量之比为1:3。Y′与E′以1:1发生化合反应生成G′,假设反应过程无损耗,A′、B′、C′为单质,气体数据均为标准状况下测定:根据如下转化关系,给出A′、B′、C′、D′、E′、F′的化学式:A′____ 、B′____ 、C′____ 、D′____ 、E′____ 、F′____ 。
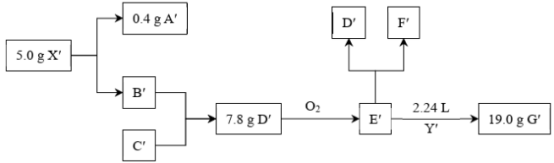
(3)已知甲、乙、丙、丁是四种常见物质,其转化关系如图所示:
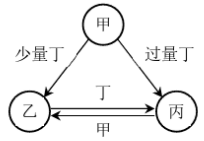
若丁和乙均为单质,且乙中所含元素的原子序数是丁的2倍。写出甲、乙、丙的化学式:甲____ 乙____ 丙____ 。

写出化合物X、D的化学式:X
(2)我国科学家在金刚石压腔实验中创造出了新颖化合物X′,超过
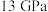 的压力下能保持稳定。5.0克X′在一定条件下完全分解为B′和0.4克A′(气体);A′的密度约为
的压力下能保持稳定。5.0克X′在一定条件下完全分解为B′和0.4克A′(气体);A′的密度约为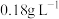 ;A′和B′物质的量之比为l:2。Y′为含有C′元素的气态氧化物,能使品红溶液褪色;C′的单质是环状分子,具有冠状结构。E′为常见无机物,将E′隔绝空气加热可得D′和F′,产生的D′和F′的物质的量之比为1:3。Y′与E′以1:1发生化合反应生成G′,假设反应过程无损耗,A′、B′、C′为单质,气体数据均为标准状况下测定:根据如下转化关系,给出A′、B′、C′、D′、E′、F′的化学式:A′
;A′和B′物质的量之比为l:2。Y′为含有C′元素的气态氧化物,能使品红溶液褪色;C′的单质是环状分子,具有冠状结构。E′为常见无机物,将E′隔绝空气加热可得D′和F′,产生的D′和F′的物质的量之比为1:3。Y′与E′以1:1发生化合反应生成G′,假设反应过程无损耗,A′、B′、C′为单质,气体数据均为标准状况下测定:根据如下转化关系,给出A′、B′、C′、D′、E′、F′的化学式:A′
(3)已知甲、乙、丙、丁是四种常见物质,其转化关系如图所示:

若丁和乙均为单质,且乙中所含元素的原子序数是丁的2倍。写出甲、乙、丙的化学式:甲
您最近一年使用:0次
9 . 化合物Ⅹ由三种常见的元素组成(X为 型,且P与Q中的原子个数比相同,X的式量为412),不溶于水,高温爆炸.某实验小组进行了如下实验(以下气体体积均为标况下体积):
型,且P与Q中的原子个数比相同,X的式量为412),不溶于水,高温爆炸.某实验小组进行了如下实验(以下气体体积均为标况下体积):
①取 固体X微热分解得到紫黑色固体A、
固体X微热分解得到紫黑色固体A、 气体B和
气体B和 气体C;
气体C;
②将①中得到的混合气体通入足量的 固体中,加热,充分反应,将反应后的混合气体通过
固体中,加热,充分反应,将反应后的混合气体通过 固体,
固体, 固体变为蓝色,同时得到
固体变为蓝色,同时得到 气体B。
气体B。
③将紫黑色固体加到足量的 溶液中,再通入足量的
溶液中,再通入足量的 ,得到
,得到 白色沉淀D已知:气体B是常见气体,可作为化学反应的保护气。
白色沉淀D已知:气体B是常见气体,可作为化学反应的保护气。
请回答以下问题:
(1)写出A的电子式_______ 。
(2)写出生成白色沉淀D的化学方程式_______ 。
(3)写出气体C通过灼热 发生反应的化学方程式
发生反应的化学方程式_______ 。
(4)固体X可由A与气体C的浓溶液反应生成,其离子方程式为_______ 。
(5)有人提出气体C在加热条件下与 反应,固体产物可能是
反应,固体产物可能是 ,也可能是
,也可能是 ,请设计实验方案验证之(用化学方法)
,请设计实验方案验证之(用化学方法)_______ 。
 型,且P与Q中的原子个数比相同,X的式量为412),不溶于水,高温爆炸.某实验小组进行了如下实验(以下气体体积均为标况下体积):
型,且P与Q中的原子个数比相同,X的式量为412),不溶于水,高温爆炸.某实验小组进行了如下实验(以下气体体积均为标况下体积):①取
 固体X微热分解得到紫黑色固体A、
固体X微热分解得到紫黑色固体A、 气体B和
气体B和 气体C;
气体C;②将①中得到的混合气体通入足量的
 固体中,加热,充分反应,将反应后的混合气体通过
固体中,加热,充分反应,将反应后的混合气体通过 固体,
固体, 固体变为蓝色,同时得到
固体变为蓝色,同时得到 气体B。
气体B。③将紫黑色固体加到足量的
 溶液中,再通入足量的
溶液中,再通入足量的 ,得到
,得到 白色沉淀D已知:气体B是常见气体,可作为化学反应的保护气。
白色沉淀D已知:气体B是常见气体,可作为化学反应的保护气。请回答以下问题:
(1)写出A的电子式
(2)写出生成白色沉淀D的化学方程式
(3)写出气体C通过灼热
 发生反应的化学方程式
发生反应的化学方程式(4)固体X可由A与气体C的浓溶液反应生成,其离子方程式为
(5)有人提出气体C在加热条件下与
 反应,固体产物可能是
反应,固体产物可能是 ,也可能是
,也可能是 ,请设计实验方案验证之(用化学方法)
,请设计实验方案验证之(用化学方法)
您最近一年使用:0次
10 . 实验室中的碘水一般是将碘单质溶于KI溶液配制而成,发生反应:I-+I2⇌I3-(主要溶质为KI3或KI·I2)。下列说法不正确 的是
| A.该溶液遇淀粉显蓝色 |
| B.该溶液见光易变质,应用棕色试剂瓶密封保存 |
| C.采用此法配制碘水的目的是为了提高碘水的浓度 |
| D.该溶液中通入SO2后,溶液由中性变为强酸性 |
您最近一年使用:0次
2020-05-29更新
|
325次组卷
|
3卷引用:2020年浙江省温州市摇篮杯高一化学竞赛试卷



