名校
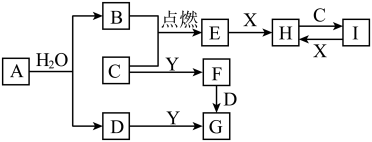
1 . 如图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系(反应中生成的水已略去)。
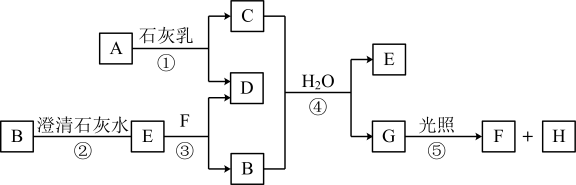
请回答以下问题:
(1)工业上常利用反应①制取漂白粉,该反应的化学方程式:_____ ,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为____ 。
(2)A中元素的原子结构示意图为____ 。
(3)F在溶液中的电离方程式为_____ 。
(4)上述反应中属于氧化还原反应的是___ (填写序号)。

请回答以下问题:
(1)工业上常利用反应①制取漂白粉,该反应的化学方程式:
(2)A中元素的原子结构示意图为
(3)F在溶液中的电离方程式为
(4)上述反应中属于氧化还原反应的是
您最近一年使用:0次
解题方法
2 . 某小组探究纯净物M(由2种短周期元素组成)的化学式,进行如图实验(气体体积均在标准状况下测定):
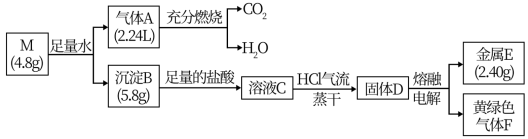
实验测定,①2.40g金属E与稀硫酸按n(E):n(H2SO4)=1:1反应能放出2.24LH2(标准状况);②金属E能在NH3中剧烈燃烧,当E和NH3按n(E):n(NH3)=1:2反应时产物的物质的量之比为1:1。
回答下列问题:
(1)A分子的结构式为___ 。
(2)M的化学式为___ 。
(3)M与水反应的化学方程式为___ 。
(4)E在氨气中燃烧的化学方程式为___ 。
(5)蒸干C溶液中HCl的作用是___ 。
(6)电解熔融D时阳极的电极反应式为__ 。

实验测定,①2.40g金属E与稀硫酸按n(E):n(H2SO4)=1:1反应能放出2.24LH2(标准状况);②金属E能在NH3中剧烈燃烧,当E和NH3按n(E):n(NH3)=1:2反应时产物的物质的量之比为1:1。
回答下列问题:
(1)A分子的结构式为
(2)M的化学式为
(3)M与水反应的化学方程式为
(4)E在氨气中燃烧的化学方程式为
(5)蒸干C溶液中HCl的作用是
(6)电解熔融D时阳极的电极反应式为
您最近一年使用:0次
名校
解题方法
3 . 某常见金属的结晶水化合物MCl3·6H2O有如下转化关系:下列推断正确的是( )


| A.固体1一定是既能与盐酸反应,又能与强碱反应 |
| B.气体1通过五水硫酸铜晶体,固体变蓝色 |
| C.常温下,溶液2能溶解铜 |
| D.固体2浊液中滴加Na2S溶液,白色固体变黄色 |
您最近一年使用:0次
2020-03-06更新
|
188次组卷
|
2卷引用:江西省吉安市2020届高三上学期期末教学质量检测化学试题
4 . 如图是一些常见元素的单质或化合物之间的转化关系。溶液中的水及部分反应物或生成物未标出。A、E是空气的两种主要成分;反应①是在1500℃隔绝空气的条件下发生的,其中生成物D是单质。C是由两种元素组成的新型材料,且和SiC具有相同的最外层子数和原子数,J是一种能引起温室效应的气体,K是两性化合物,反应③、④、⑤用于工业中生产H。
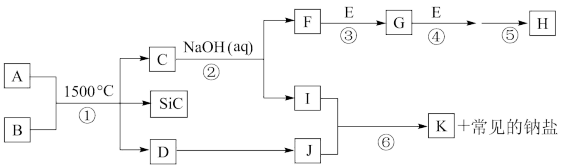
请回答下列问题。
(1)A的电子式:___________ ;I的化学式:___________ ;H的化学式:___________ 。
(2)写出反应③的化学方程式:___________ 。
(3)写出反应⑥的离子方程式(J少量):___________ 。写出反应②的离子方程式:___________ 。
(4)B和SiC的纳米级复合粉末是新一代大规模集成电路理想的散热材料,反应①是科学家研究开发制备该纳米级复合材料的最新途径。已知:B由Si及另外两种元素组成,且Si与另外两种元素的物质的量之比均为1:4.请写出反应①的化学方程式:___________ 。

请回答下列问题。
(1)A的电子式:
(2)写出反应③的化学方程式:
(3)写出反应⑥的离子方程式(J少量):
(4)B和SiC的纳米级复合粉末是新一代大规模集成电路理想的散热材料,反应①是科学家研究开发制备该纳米级复合材料的最新途径。已知:B由Si及另外两种元素组成,且Si与另外两种元素的物质的量之比均为1:4.请写出反应①的化学方程式:
您最近一年使用:0次
解题方法
5 . 兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,被广泛用作有机物的氢化反应的催化剂。以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如下图所示:
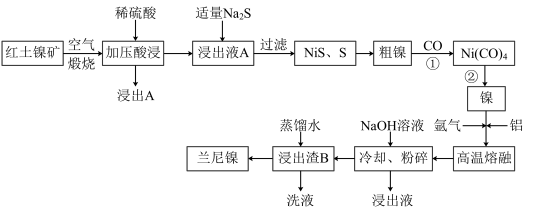
(1)煅烧时主要生成的气体产物是___________ ,浸出渣A的主要成分是____________ 。
(2)向浸出液A中加入适量Na2S,发生氧化还原的离子方程式为________________________ 。若Na2S过量时,则过滤出的固体中会混有__________ ;
(3)已知Ni(CO)4的沸点是42.2℃,Ni(S)+CO(g)⇌ Ni(CO)4(g)的平衡常数与温度的关系如下:
步骤①、步骤②的最佳温度分别是_______ 、_______ (填选项代号)
A. 25℃ B. 30℃ C. 50℃ D. 80℃ E. 230℃
(4)加氢氧化钠的目的是溶解部分铝,形成多孔结构的镍铝合金,已知红土镍矿中NiS质量分数45.5%,取1kg红土镍矿进行制备(不考虑制备过程中镍的损耗),熔融时加入270g铝,浸出时消耗800mL 5mol/LNaOH,理论上生成的兰尼镍的化学式为__________ 。

(1)煅烧时主要生成的气体产物是
(2)向浸出液A中加入适量Na2S,发生氧化还原的离子方程式为
(3)已知Ni(CO)4的沸点是42.2℃,Ni(S)+CO(g)⇌ Ni(CO)4(g)的平衡常数与温度的关系如下:
| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
A. 25℃ B. 30℃ C. 50℃ D. 80℃ E. 230℃
(4)加氢氧化钠的目的是溶解部分铝,形成多孔结构的镍铝合金,已知红土镍矿中NiS质量分数45.5%,取1kg红土镍矿进行制备(不考虑制备过程中镍的损耗),熔融时加入270g铝,浸出时消耗800mL 5mol/LNaOH,理论上生成的兰尼镍的化学式为
您最近一年使用:0次
名校
解题方法
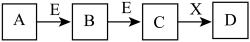
6 . 中学常见物质A、B、C、D、E、X,存在下图转化关系  部分生成物和反应条件略去
部分生成物和反应条件略去 。下列推断不正确的是
。下列推断不正确的是

 部分生成物和反应条件略去
部分生成物和反应条件略去 。下列推断不正确的是
。下列推断不正确的是


| A.若D是一种强碱,则A、C均可与X反应生成D |
| B.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C |
C.若D为NaCl,且A可与C反应生成B,则E可能是 |
| D.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁 |
您最近一年使用:0次
2020-01-28更新
|
486次组卷
|
4卷引用:2020届高三化学二轮冲刺新题专练——高考常考题型:无机化学推断题
7 . 如图是中学化学中常见物质的转化关系,部分物质和反应条件略去。
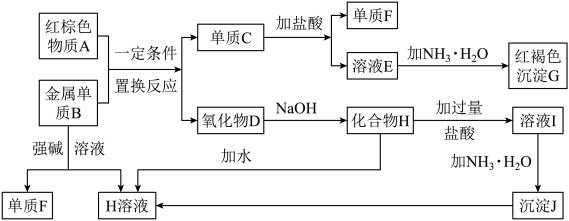
(1)单质F的化学式是___ 。
(2)写出由沉淀J生成 H溶液的离子方程式__ 。
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:__ ,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式__ 。
(4)溶液I中所含金属离子是__ 。

(1)单质F的化学式是
(2)写出由沉淀J生成 H溶液的离子方程式
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:
(4)溶液I中所含金属离子是
您最近一年使用:0次
2020-01-20更新
|
112次组卷
|
2卷引用:江西省高安中学2019-2020学年高一上学期期末考试化学(A卷)试题
8 . 现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。提示:黄绿色气体乙是氯气。
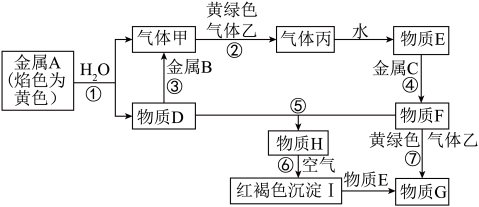
请回答下列问题:
(1)写出下列物质的化学式:B______ ,丙______ ,H______ 。
(2)根据要求回答:
①D溶液和F溶液在空气中混合的现象:_______ ;
②反应③离子方程式________ ;
③反应⑦离子方程式________ ;
④反应⑥化学方程式________ 。

请回答下列问题:
(1)写出下列物质的化学式:B
(2)根据要求回答:
①D溶液和F溶液在空气中混合的现象:
②反应③离子方程式
③反应⑦离子方程式
④反应⑥化学方程式
您最近一年使用:0次
2020-01-18更新
|
112次组卷
|
2卷引用:江西省南昌市第十中学2019-2020学年高一上学期期末考试化学试题
名校
解题方法
9 . X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W分别与Y形成的最高价化合物为甲、乙、丙。结合如图转化关系,下列判断错误的是( )
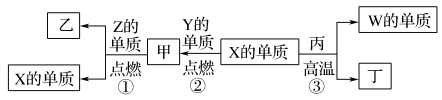

| A.反应③可用于工业上制取W的单质 | B.X位于元素周期表第二周期ⅣA族 |
| C.甲、丙、丁均为酸性化合物 | D.工业上可以用乙来作耐火材料 |
您最近一年使用:0次
2020-01-17更新
|
1249次组卷
|
6卷引用:安徽省阜阳市第三中学2019-2020学年高二上学期期末考试化学试题
解题方法
10 . 如图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和条件被略去。A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;B、C、E是常见气体,G的焰色反应呈黄色;I的溶液呈黄色。
请回答下列问题:
(1)写出下列物质的化学式A___ 、F___ 、X___ ;
(2)说出黄绿色气体C的一种用途____ ;
(3)实验室检验H中所含的金属阳离子的方法是:___ ;
(4)写出Y和D溶液反应的离子方程式___ ;
(5)写出I与X溶液反应的化学方程式___ 。

请回答下列问题:
(1)写出下列物质的化学式A
(2)说出黄绿色气体C的一种用途
(3)实验室检验H中所含的金属阳离子的方法是:
(4)写出Y和D溶液反应的离子方程式
(5)写出I与X溶液反应的化学方程式
您最近一年使用:0次



