名校
解题方法
1 . 现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙___________ 、F___________ ;
(2)说出黄绿色气体乙的一种用途___________ ;
(3)实验室检验G中所含的金属离子时,常选用的试剂是___________ ;
(4)反应③的化学方程式为___________ ;
(5)反应⑥的离子方程式 为___________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙
(2)说出黄绿色气体乙的一种用途
(3)实验室检验G中所含的金属离子时,常选用的试剂是
(4)反应③的化学方程式为
(5)反应⑥的
您最近一年使用:0次
2 . 水合肼(N2H4·H2O)是一种用途广泛的化工原料,在空气中会与CO2反应产生烟雾。利用尿素制备N2H4·H2O的实验流程如下图所示:
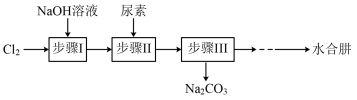
回答下列问题:
(1)步骤I制备NaClO溶液的离子方程式为___________ ;该反应为放热反应,为避免副反应发生,需控制温度不高于40°C,可采取的措施是___________ (任答一条)。
(2)由步骤II和步骤III获得N2H4·H2O的装置如图1所示,反应原理为: CO(NH2)2+ 2NaOH+ NaClO= Na2CO3+ N2H4·H2O +NaCl
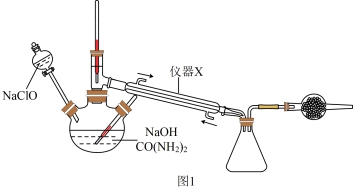
①仪器X的名称为___________ ,干燥管中盛装的试剂为___________ 。
②N2H4的电子式为___________ 。
③反应过程中,如果分液漏斗中溶液滴速过快,部分N2H4·H2O与NaClO反应产生大量氮气,该化学反应方程式为___________ 。
④蒸馏获得水合肼粗品后,剩余溶液进一步处理还可获得副产品NaCl和Na2CO3,NaCl和Na2CO3的溶解度曲线如图2所示。获得NaCl粗品的操作是___________ 、___________ 、洗涤、干燥。
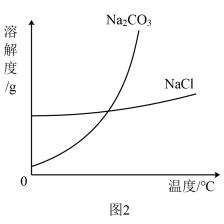
(3)馏分中水合肼含量的测定方法:称取馏分0.2500g,加入适量NaHCO3固体,配成溶液,用0.1500 mol·L-1的标准I2溶液滴定。
①滴定时,碘的标准溶液盛放在___________ (填 “酸式”或“碱式”)滴定管中。
②实验测得消耗I2溶液的体积为18.00 mL,馏分中N2H4·H2O的质量分数为___________ 。 (已知:N2H4·H2O +2I2=N2 ↑+ 4HI+H2O)

回答下列问题:
(1)步骤I制备NaClO溶液的离子方程式为
(2)由步骤II和步骤III获得N2H4·H2O的装置如图1所示,反应原理为: CO(NH2)2+ 2NaOH+ NaClO= Na2CO3+ N2H4·H2O +NaCl

①仪器X的名称为
②N2H4的电子式为
③反应过程中,如果分液漏斗中溶液滴速过快,部分N2H4·H2O与NaClO反应产生大量氮气,该化学反应方程式为
④蒸馏获得水合肼粗品后,剩余溶液进一步处理还可获得副产品NaCl和Na2CO3,NaCl和Na2CO3的溶解度曲线如图2所示。获得NaCl粗品的操作是

(3)馏分中水合肼含量的测定方法:称取馏分0.2500g,加入适量NaHCO3固体,配成溶液,用0.1500 mol·L-1的标准I2溶液滴定。
①滴定时,碘的标准溶液盛放在
②实验测得消耗I2溶液的体积为18.00 mL,馏分中N2H4·H2O的质量分数为
您最近一年使用:0次



