1 . 通过化学实验现象得出相应的结论是探究物质性质的一种重要方法,下列化学实验现象与结论对应完全正确的是
| 化学实验现象 | 解释与结论 | |
| A | 钠与水反应时浮在水面上 | 钠与水生成的气体托举钠浮在水面上 |
| B | 氯水放置数天后酸性增强 | 氯气与水反应生成的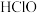 见光易分解生成 见光易分解生成 |
| C | 氯水呈黄绿色 | 氯气与水反应生成了黄绿色物质 |
| D | 氢气在氯气中燃烧时瓶口有白雾 | 氯气逸出结合空气中的水蒸气而呈白雾状 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
2 . 下列物质不能由单质和氯气直接反应制取的是
| A.NaCl | B. | C.HCl | D. |
您最近半年使用:0次
3 . 下图是化学实验室浓盐酸试剂标签上的部分内容。
(1)写出工业上制 的化学方程式
的化学方程式___________ ,在实验室中进行该反应,现象是___________ 。
(2)该盐酸的物质的量浓度为___________ 。
(3)同学计划用该浓盐酸配制 的稀盐酸,现实验需要稀盐酸
的稀盐酸,现实验需要稀盐酸 ,可供选用的仪器有:A.胶头滴管 B.烧瓶 C.烧杯 D.药匙 E.玻璃棒
,可供选用的仪器有:A.胶头滴管 B.烧瓶 C.烧杯 D.药匙 E.玻璃棒
①配制稀盐酸时,选择的仪器有:___________ (填序号),还缺少的仪器有___________ 。
②经计算,配制 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为___________ mL。
③测定所配制的稀盐酸,发现其浓度大于 ,引起误差的原因可能是
,引起误差的原因可能是___________ 。
A.量取浓盐酸时俯视刻度线
B.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶刻度线
E.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
| 盐酸 分子式:  相对分子质量:36.5 密度约   的质量分数:36.5% 的质量分数:36.5% |
 的化学方程式
的化学方程式(2)该盐酸的物质的量浓度为
(3)同学计划用该浓盐酸配制
 的稀盐酸,现实验需要稀盐酸
的稀盐酸,现实验需要稀盐酸 ,可供选用的仪器有:A.胶头滴管 B.烧瓶 C.烧杯 D.药匙 E.玻璃棒
,可供选用的仪器有:A.胶头滴管 B.烧瓶 C.烧杯 D.药匙 E.玻璃棒①配制稀盐酸时,选择的仪器有:
②经计算,配制
 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为③测定所配制的稀盐酸,发现其浓度大于
 ,引起误差的原因可能是
,引起误差的原因可能是A.量取浓盐酸时俯视刻度线
B.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶刻度线
E.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
您最近半年使用:0次
4 . 下列说法不正确 的是
A. 为白色固体,易被空气氧化 为白色固体,易被空气氧化 |
B.工业上常用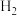 和 和 直接化合的方法生产氯化氢以制得盐酸 直接化合的方法生产氯化氢以制得盐酸 |
C.实验室常用 溶液吸收多余的 溶液吸收多余的 以避免污染 以避免污染 |
D.将废铁屑加入 溶液中,可用于除去工业废气中的 溶液中,可用于除去工业废气中的 |
您最近半年使用:0次
5 . 通过化学实验现象得出相应的结论是探究物质性质的一种重要方法,下列实验操作和现象或结论不正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向包有足量过氧化钠粉末的脱脂棉上滴加几滴水,脱脂棉燃烧 | 过氧化钠与水反应放热 |
| B | 向某未知溶液(不含 )中加入足量硝酸酸化的硝酸银溶液,无气体产生,但有白色沉淀出现 )中加入足量硝酸酸化的硝酸银溶液,无气体产生,但有白色沉淀出现 | 未知溶液中可能含有Cl-,一定不含CO 或HCO 或HCO |
| C | 氢气在氯气中燃烧时瓶口上方出现白雾 | 氯化氢与空气中的水蒸气结合而呈现雾状 |
| D | 将金属Na投入硫酸铜溶液中,有紫红色固体产生 | 说明Na比Cu活泼 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
6 . 氯气与氢气在点燃条件下反应的实验现象:____________ 。
您最近半年使用:0次
7 . 下列关于氯的单质及化合物的叙述中,不正确 的是
| A.常温常压下,Cl2是黄绿色气体 | B.氯水和液氯的成分相同 |
| C.光照能使次氯酸发生分解 | D.氢气在氯气中燃烧发出苍白色火焰 |
您最近半年使用:0次
8 . 下列化合物不能通过化合反应一步制得的是
A. | B. | C. | D. |
您最近半年使用:0次
名校
9 . 工业氯气通过电解饱和食盐水制得
(1)图(1)中,铁棒作_______ 极,电极反应式是_______ 。
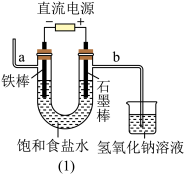
(2)检验导管b出来的气体可以用_______ ,反应的化学方程式是:_______ ;电解饱和食盐水的化学反应方程式为_______ 。
(3)图(1)方法制得的固体烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法:_______ 。
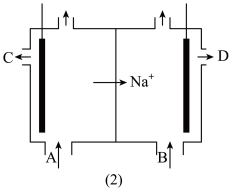
(4)下列关于图(2)的说法正确的是_______。
(5)工业上利用 与
与 反应制盐酸时使用过量的
反应制盐酸时使用过量的 ,理由是
,理由是_______ 。
A.氯气有毒 B.氯气可溶于水 C.氢气密度小
(1)图(1)中,铁棒作

(2)检验导管b出来的气体可以用
(3)图(1)方法制得的固体烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法:
(4)下列关于图(2)的说法正确的是_______。

| A.A与C、B与D溶质相同 | B.A、B通入的均为浓溶液 |
| C.理论上NaCl利用率可达100% | D.图(2)是负离子交换膜法示意图 |
(5)工业上利用
 与
与 反应制盐酸时使用过量的
反应制盐酸时使用过量的 ,理由是
,理由是A.氯气有毒 B.氯气可溶于水 C.氢气密度小
您最近半年使用:0次
名校
解题方法
10 . 铁、铝是两种常见的金属,其合金在生产、生活中扮演着重要的角色,对混合物进行如下实验:

(1)操作X是___________ ;
(2)A与Cl2混合光照可能发生爆炸,A在该反应中作___________ (填“氧化剂”或“还原剂”);
(3)合金中加入足量NaOH溶液发生反应的离子方程式___________ ;
(4)加入稀盐酸发生反应的离子方程式为___________ ;
(5)向溶液D中加入NaOH溶液,观察到产生的现象是___________ ,写出相应的化学方程式:___________ ,___________ 。

(1)操作X是
(2)A与Cl2混合光照可能发生爆炸,A在该反应中作
(3)合金中加入足量NaOH溶液发生反应的离子方程式
(4)加入稀盐酸发生反应的离子方程式为
(5)向溶液D中加入NaOH溶液,观察到产生的现象是
您最近半年使用:0次
2024-03-12更新
|
52次组卷
|
2卷引用:贵州省瓮安中学2023-2024学年高一上学期12月月考化学试题



