1 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中a为干燥的红色纸,b为湿润的红色纸。
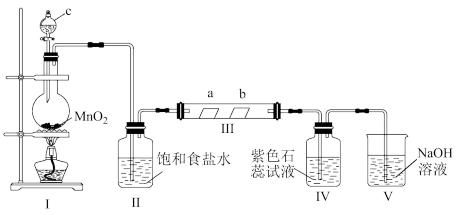
(1)装置Ⅰ 中仪器c的名称是_______ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为_______ 。
(2)装置Ⅱ的作用是_______ 。
(3)实验过程中装置Ⅳ中的实验现象_______ 。
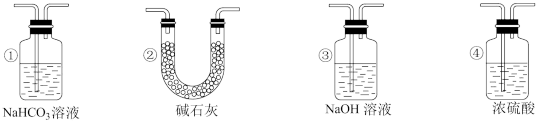
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加所给_______ 装置(填序号)。
(5)有一种“地康法”制取氯气的反应原理如图所示:
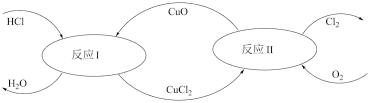
① 反应Ⅰ的化学方程式为_______ 。
② 反应Ⅱ属于_______ (填四种基本反应类型之一)。
③ 若要制得0.5mol Cl2则消耗O2(标准状况)的体积约_______ L。

(1)装置Ⅰ 中仪器c的名称是
(2)装置Ⅱ的作用是
(3)实验过程中装置Ⅳ中的实验现象
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加所给

(5)有一种“地康法”制取氯气的反应原理如图所示:

① 反应Ⅰ的化学方程式为
② 反应Ⅱ属于
③ 若要制得0.5mol Cl2则消耗O2(标准状况)的体积约
您最近一年使用:0次
解题方法
2 . 氯气是一种重要的化工原料,大量用于制造盐酸、漂白剂、农药、染料和药品等。
(1)1774年,瑞典化学家舍勒将浓盐酸与软锰矿(主要成分为 )混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
)混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
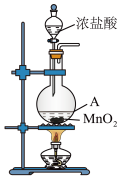
盛放浓盐酸的仪器名称是_______ 。
(2)下图所示制取氯气的净化、收集、尾气处理的装置能达到实验目的的是_______ 。(填序号)
(3)已知:常温下用 和市售浓盐酸(11.9
和市售浓盐酸(11.9 )反应制取Cl2难以进行。但若用漂白粉(有效成分
)反应制取Cl2难以进行。但若用漂白粉(有效成分 )、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。
)、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。
①已知,如图装置A是氯气的发生装置。加入适量的浓盐酸充分反应有黄绿色气体生成,写出发生反应的化学方程式,并用单线桥标明电子转移的方向和数目 :_______ 。

②装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅲ处应放入的是_______ (填序号)。
a.干燥的有色布条 b.湿润的有色布条 c.湿润的淀粉 试纸
试纸
装置C的Ⅱ处的试剂是_______ (填序号)。
a.碱石灰(氢氧化钠和氧化钙的固体混合物) b.无水氯化钙 c.浓硫酸
③装置D中一般不用 澄清石灰水吸收多余的氯气。理由是_______ 。
(4)84消毒液是一种常见的含氯消毒剂,其有效成分为次氯酸钠。
资料:84消毒液中含氯微粒主要有 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;
; 是反映水溶液中所有物质表现出来的氧化—还原性,
是反映水溶液中所有物质表现出来的氧化—还原性, 值越大,氧化性越强。
值越大,氧化性越强。
某兴趣小组同学研究84消毒液的漂白性,实验如下。
I.向2 84消毒液中加入2
84消毒液中加入2 水后,放入红色纸片,观察到纸片慢慢褪色。
水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.向2 84消毒液中加入2
84消毒液中加入2 白醋后,放入红色纸片,观察到纸片迅速褪色。
白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.测得84消毒液在不同温度时 随时间的变化曲线如
随时间的变化曲线如图 。
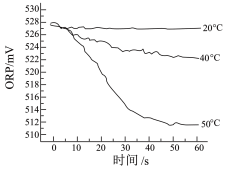
①已知白醋显酸性,不具有漂白性。实验I、Ⅱ现象不同的原因是_______ 。
②由实验Ⅲ可得出的结论是_______ 。
(1)1774年,瑞典化学家舍勒将浓盐酸与软锰矿(主要成分为
 )混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
)混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
盛放浓盐酸的仪器名称是
(2)下图所示制取氯气的净化、收集、尾气处理的装置能达到实验目的的是
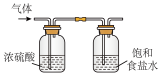 | 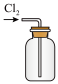 |  |
| A.净化Cl2 | B.收集Cl2 | C.尾气处理 |
(3)已知:常温下用
 和市售浓盐酸(11.9
和市售浓盐酸(11.9 )反应制取Cl2难以进行。但若用漂白粉(有效成分
)反应制取Cl2难以进行。但若用漂白粉(有效成分 )、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。
)、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。①已知,如图装置A是氯气的发生装置。加入适量的浓盐酸充分反应有黄绿色气体生成,写出发生反应的化学方程式,并用

②装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅲ处应放入的是
a.干燥的有色布条 b.湿润的有色布条 c.湿润的淀粉
 试纸
试纸装置C的Ⅱ处的试剂是
a.碱石灰(氢氧化钠和氧化钙的固体混合物) b.无水氯化钙 c.浓硫酸
③装置D中一般
(4)84消毒液是一种常见的含氯消毒剂,其有效成分为次氯酸钠。
资料:84消毒液中含氯微粒主要有
 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;
; 是反映水溶液中所有物质表现出来的氧化—还原性,
是反映水溶液中所有物质表现出来的氧化—还原性, 值越大,氧化性越强。
值越大,氧化性越强。某兴趣小组同学研究84消毒液的漂白性,实验如下。
I.向2
 84消毒液中加入2
84消毒液中加入2 水后,放入红色纸片,观察到纸片慢慢褪色。
水后,放入红色纸片,观察到纸片慢慢褪色。Ⅱ.向2
 84消毒液中加入2
84消毒液中加入2 白醋后,放入红色纸片,观察到纸片迅速褪色。
白醋后,放入红色纸片,观察到纸片迅速褪色。Ⅲ.测得84消毒液在不同温度时
 随时间的变化曲线如
随时间的变化曲线如
①已知白醋显酸性,不具有漂白性。实验I、Ⅱ现象不同的原因是
②由实验Ⅲ可得出的结论是
您最近一年使用:0次
解题方法
3 . 实验室制取Cl2时,下列装置能达到相应实验目的的是
A.制备Cl2 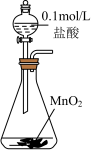 | B.净化Cl2 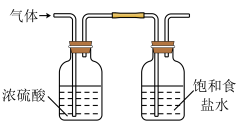 |
C.收集Cl2 | D.尾气处理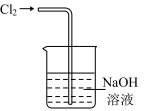 |
您最近一年使用:0次
名校
4 .  熔点为
熔点为 ,沸点为
,沸点为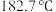 ,在
,在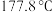 升华。某同学利用如下装置(部分夹持仪器已略)制备无水
升华。某同学利用如下装置(部分夹持仪器已略)制备无水 ,其中能达到相应实验目的的是
,其中能达到相应实验目的的是
 熔点为
熔点为 ,沸点为
,沸点为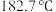 ,在
,在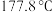 升华。某同学利用如下装置(部分夹持仪器已略)制备无水
升华。某同学利用如下装置(部分夹持仪器已略)制备无水 ,其中能达到相应实验目的的是
,其中能达到相应实验目的的是| A.制取氯气 | B.干燥氯气 | C.制取并收集AlCl3 | D.吸收尾气 |
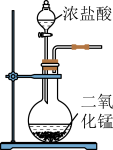 | 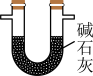 | 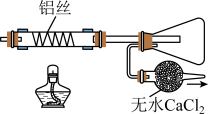 | 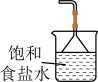 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-16更新
|
318次组卷
|
4卷引用:江苏省苏州八校联盟2021-2022学年高三上学期第二次适应性检化学试题
江苏省苏州八校联盟2021-2022学年高三上学期第二次适应性检化学试题(已下线)题型33 铝及其化合物的性质(已下线)专题卷19 仪器的使用与实验装置分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)重庆市第一中学校2023-2024学年高一上学期期末化学模拟试卷
名校
5 . 某实验小组进行Cl2的制备和性质探究,下列装置和药品能实现相应实验目的的是
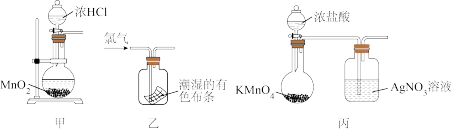
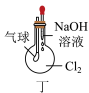


| A.利用甲制备Cl2 |
| B.利用乙证明氯气具有漂白性 |
| C.利用丙的AgNO3溶液中产生白色沉淀,说明氯气与水反应生成Cl- |
| D.利用丁中气球膨胀,证明Cl2可与NaOH反应 |
您最近一年使用:0次
2022-11-08更新
|
356次组卷
|
4卷引用:江苏省靖江高级中学2022-2023学年高一上学期第三次阶段测试化学试题
名校
解题方法
6 . 海洋是一个十分巨大的资源宝库。海水中含量最多的是H、O两种元素,还含有Na、Cl、Mg、Br、Ca、K、S等元素。以海水为原料可制备氯气、氯化钠和溴等。实验室制取氯气的原理或装置能达到实验目的的是
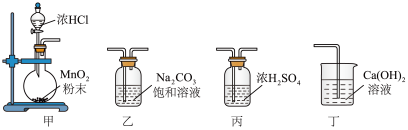

| A.用装置甲制备氯气 | B.用装置乙除去Cl2中的HCl气体 |
| C.用装置丙干燥氯气 | D.用装置丁吸收多余的氯气 |
您最近一年使用:0次
2023-01-10更新
|
423次组卷
|
4卷引用:江苏省苏州市2022-2023学年高一上学期学业质量阳光指标调研化学试题
江苏省苏州市2022-2023学年高一上学期学业质量阳光指标调研化学试题(已下线)专题03 研究物质的实验方法 一定物质的量浓度溶液的配制-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)江苏省扬州市新华中学2023-2024学年高一上学期12月阶段检测化学试题山东省曹县第一中学2022-2023学年高一上学期期末考试化学试题
7 . 下列用Cl2氧化K2MnO4制备KMnO4的实验原理和装置能达到实验目的的是
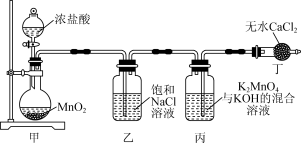

| A.用装置甲制取Cl2 | B.用装置乙除去HCl杂质 |
| C.用装置丙制备KMnO4 | D.用装置丁处理尾气 |
您最近一年使用:0次
2022-11-17更新
|
204次组卷
|
2卷引用:江苏省南通市通州区2022-2023学年高三上学期期中质量监测化学试题
名校
8 . 氯化氢和氯气在生产生活中具有广泛应用。舍勒发现将软锰矿和浓盐酸混合加热可产生氯气,该方法仍是当今实验室制备氯气的主要方法之一。Deacon曾提在催化剂作用下,通过氧气直接氧化氯化氢制备氯气。该反应为可逆反应,热化学方程式为4HCl(g)+O2(g)=2Cl2(g)+H2O(g) ΔH=-116 kJ-mol-1。实验室制取Cl2时,下列装置能达到相应实验目的的是
| A | B | C | D |
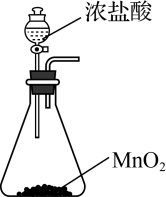 | 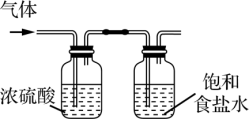 | 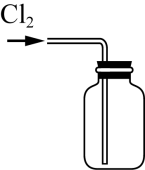 | 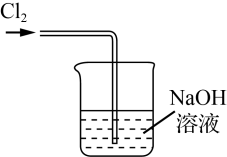 |
| 制备Cl2 | 净化Cl2 | 收集Cl2 | 尾气处理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-05-08更新
|
369次组卷
|
3卷引用:江苏省七市(南通、扬州、泰州、淮安、徐州、宿迁、连云港)2021届高三第三次调研考试化学试题
江苏省七市(南通、扬州、泰州、淮安、徐州、宿迁、连云港)2021届高三第三次调研考试化学试题(已下线)第12讲 富集在海水中的元素——卤素(精练)-2022年高考化学一轮复习讲练测湖南省常德市汉寿县第一中学2022届高三下学期第三次模考化学试题
名校
9 . 某同学用以下装置制备并检验 的性质。按要求回答问题。
的性质。按要求回答问题。
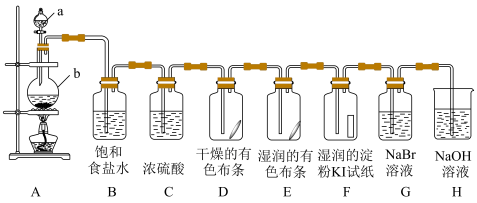
(1)a中加入浓盐酸、b中加入 ,A中制备氯气的化学反应方程式为:
,A中制备氯气的化学反应方程式为:__________ 。
(2)若用含有 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得
,制得 的物质的量总是小于
的物质的量总是小于 的原因是
的原因是__________ 、__________ 。
(3)①装置D和E中现象不同,说明具有漂白性的物质是__________ 。(写化学式)
②装置F中可观察到的现象是_____________________________ 。
③实验结束后,取装置G中少许溶液于试管中,加入苯,充分振荡、静置,观察到的现象是__________ 。
④装置H中发生反应的化学方程式为_______________________ 。
 的性质。按要求回答问题。
的性质。按要求回答问题。
(1)a中加入浓盐酸、b中加入
 ,A中制备氯气的化学反应方程式为:
,A中制备氯气的化学反应方程式为:(2)若用含有
 的浓盐酸与足量的
的浓盐酸与足量的 反应制
反应制 ,制得
,制得 的物质的量总是小于
的物质的量总是小于 的原因是
的原因是(3)①装置D和E中现象不同,说明具有漂白性的物质是
②装置F中可观察到的现象是
③实验结束后,取装置G中少许溶液于试管中,加入苯,充分振荡、静置,观察到的现象是
④装置H中发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
10 .  是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或浓度较大时加热会发生燃烧并爆炸。制取
是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或浓度较大时加热会发生燃烧并爆炸。制取 的装置如下图所示。(已知:氨气易液化)
的装置如下图所示。(已知:氨气易液化)

已知: 的熔点为
的熔点为 ℃,沸点为3.8℃,
℃,沸点为3.8℃, 的沸点为
的沸点为 ℃;
℃; 。
。
根据题给信息,请回答下列问题:
(1)装置②盛装的试剂是__________ ,装置③的作用__________ 。
(2)过程中通入干燥空气的目的是__________ ,装置④与⑤之间不用橡皮管连接,目的是__________ 。
(3)写出工业制备 的化学方程式
的化学方程式__________ 。
(4)工业上常以 为原料制备“84”消毒液,现设计以下实验探究消毒液的性质:
为原料制备“84”消毒液,现设计以下实验探究消毒液的性质:
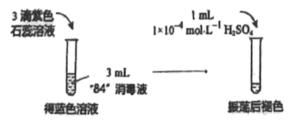
根据实验现象,可得“84”消毒液呈__________ (填“酸性”或“碱性”);
溶液褪色的原因是__________ (用离子方程式和必要文字说明)。
 是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或浓度较大时加热会发生燃烧并爆炸。制取
是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或浓度较大时加热会发生燃烧并爆炸。制取 的装置如下图所示。(已知:氨气易液化)
的装置如下图所示。(已知:氨气易液化)
已知:
 的熔点为
的熔点为 ℃,沸点为3.8℃,
℃,沸点为3.8℃, 的沸点为
的沸点为 ℃;
℃; 。
。根据题给信息,请回答下列问题:
(1)装置②盛装的试剂是
(2)过程中通入干燥空气的目的是
(3)写出工业制备
 的化学方程式
的化学方程式(4)工业上常以
 为原料制备“84”消毒液,现设计以下实验探究消毒液的性质:
为原料制备“84”消毒液,现设计以下实验探究消毒液的性质:
根据实验现象,可得“84”消毒液呈
溶液褪色的原因是
您最近一年使用:0次
2024-01-06更新
|
52次组卷
|
3卷引用:江苏省盐城市第一中学2023-2024学年高一上学期第二次校标考试化学试题



