1 . 某化学兴趣小组为探究Cl2的性质并制备氯水,用如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

回答下列问题:
(1)盛装浓盐酸的仪器的名称为___________ 。
(2)装置Ⅰ中发生反应的化学方程式为___________ 。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在___________ 和___________ (填装置序号)之间添加洗气装置,该装置的作用是___________ 。
(4)装置Ⅴ中NaOH溶液的作用是___________ ,相关反应的离子方程式为___________ 。
(5)工业上可用氢氧化钠与氯气反应制取84消毒液,在生活中84消毒液不可与洁厕灵(HCl)混用,否则会产生一种黄绿色有毒气体,其原因是___________ (用离子方程式解释)。
(6)氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强,氯水中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。
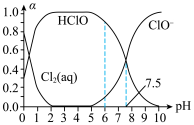
①用氯处理饮用水,pH=7.5时的杀菌效果比pH=6.5时的杀菌效果___________ (填“好”或“差”)。
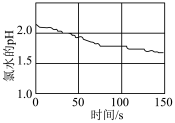
②利用数字化实验测定光照氯水得到光照过程中氯水的pH变化情况如图所示,变化原因是___________ (用方程式或必要的文字说明)。

回答下列问题:
(1)盛装浓盐酸的仪器的名称为
(2)装置Ⅰ中发生反应的化学方程式为
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在
(4)装置Ⅴ中NaOH溶液的作用是
(5)工业上可用氢氧化钠与氯气反应制取84消毒液,在生活中84消毒液不可与洁厕灵(HCl)混用,否则会产生一种黄绿色有毒气体,其原因是
(6)氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强,氯水中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。

①用氯处理饮用水,pH=7.5时的杀菌效果比pH=6.5时的杀菌效果
②利用数字化实验测定光照氯水得到光照过程中氯水的pH变化情况如图所示,变化原因是

您最近一年使用:0次
解题方法
2 . 浓盐酸和高锰酸钾在室温下即可制备氯气,用如图装置制备少量的氯气并探究其性质。下列实验装置和操作能达到实验目的的是
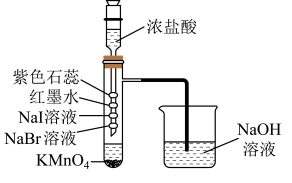

| A.根据溴化钠和碘化钠中的现象可证明氧化性:Br2<I2 |
| B.红墨水褪色,说明氯水具有漂白性 |
| C.紫色石蕊试液先变红后褪色,说明氯气具有酸性和强氧化性 |
| D.可用饱和食盐水代替NaOH溶液吸收多余的氯气 |
您最近一年使用:0次
3 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
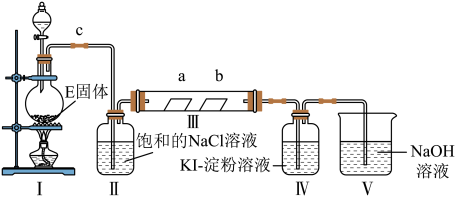
(1)实验室以二氧化锰和浓盐酸制备氯气的离子方程式是___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)实验过程中,装置IV中的实验现象为___________ ;发生反应的化学方程式为___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的___________ 装置(填序号),
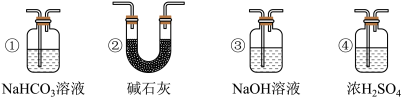
(5)装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式___________ 。

(1)实验室以二氧化锰和浓盐酸制备氯气的离子方程式是
(2)装置Ⅱ的作用是
(3)实验过程中,装置IV中的实验现象为
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的

(5)装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式
您最近一年使用:0次
4 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中a为干燥的红色纸,b为湿润的红色纸。
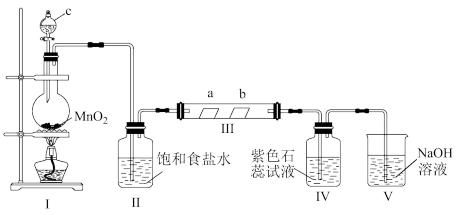
(1)装置Ⅰ 中仪器c的名称是_______ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为_______ 。
(2)装置Ⅱ的作用是_______ 。
(3)实验过程中装置Ⅳ中的实验现象_______ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加所给_______ 装置(填序号)。
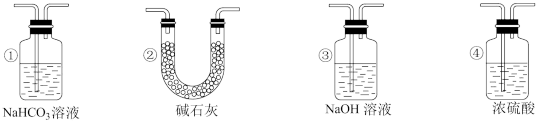
(5)有一种“地康法”制取氯气的反应原理如图所示:
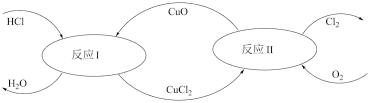
① 反应Ⅰ的化学方程式为_______ 。
② 反应Ⅱ属于_______ (填四种基本反应类型之一)。
③ 若要制得0.5mol Cl2则消耗O2(标准状况)的体积约_______ L。

(1)装置Ⅰ 中仪器c的名称是
(2)装置Ⅱ的作用是
(3)实验过程中装置Ⅳ中的实验现象
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加所给

(5)有一种“地康法”制取氯气的反应原理如图所示:

① 反应Ⅰ的化学方程式为
② 反应Ⅱ属于
③ 若要制得0.5mol Cl2则消耗O2(标准状况)的体积约
您最近一年使用:0次
5 . 下列设计的实验方案不能达到实验目的的是
| 选项 | 实验现象和操作 | 实验目的 |
| A | 向2mL0.1mol·L-1Na2S溶液中滴加0.1mol·L-1ZnSO4溶液至不再有沉淀产生,再滴加几滴0.1mol·L-1CuSO4溶液,出现黑色沉淀 | 验证Ksp(ZnS)>Ksp(CuS) |
| B | 向含有0.1mol的FeI2溶液中通入0.1molCl2,再加入淀粉溶液,溶液变蓝色 | 还原性:I->Fe2+ |
| C | 以Zn、Fe为电极,以酸化的3%NaCl溶液作电解质溶液,连接成原电池装置。过一段时间,从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴K3[Fe(CN)6]溶液,观察现象 | 探究金属的牺牲阳极保护法 |
| D | 向盛有2mL0.1mol·L-1K2Cr2O7溶液的试管中滴加5~10滴NaOH溶液,再继续滴加5~10滴6mol·L-1H2SO4溶液,观察现象 | 探究浓度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列设计的实验方案不能 达到实验目的是
| 选项 | 实验现象和操作 | 实验目的 |
| A | 向2 mL 0.1mol·L-1 Na2S溶液中滴加0.1 mol·L-1 ZnSO4溶液至不再有沉淀产生,再滴加几滴0.1 mol·L-1 CuSO4溶液,出现黑色沉淀 | 验证Ksp(ZnS)>Ksp(CuS) |
| B | 向装有电石的圆底烧瓶中逐滴加入适量饱和NaCl溶液,将产生的气体通入酸性高锰酸钾溶液中,溶液紫色褪去 | 检验乙炔中含有碳碳三键 |
| C | 以Zn、Fe为电极,以酸化的3% NaCl 溶液作电解质溶液,连接成原电池装置。过一段时间,从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴K3[Fe(CN)6]溶液,观察现象 | 探究金属的牺牲阳极保护法 |
| D | 取5mL0.1 mol·L-1 KI溶液和1mL 0.1mol·L-1 FeCl3溶液充分反应后,加2 mL CCl4振荡、静置后取上层清液滴加少量KSCN溶液,溶液变为红色 | Fe3+与I-的化学反应存在一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 硫酸亚铁可用于治疗缺铁性贫血症。某兴趣小组为探究硫酸亚铁的分解产物,设计实验方案如下:
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有 的硬质玻璃管;
的硬质玻璃管;
③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。

(1)根据B、C装置中的实验现象可推测分解产物中含有___________ 和___________ 。
(2)将装置B、C顺序颠倒能否达到原来的实验目的___________ (填“能”或“不能”),原因是___________ 。
(3)D装置中发生的主要反应的离子方程式是___________ 。
(4)通过计算确定已分解的FeSO4物质的量(写出计算过程)___________ 。
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有
 的硬质玻璃管;
的硬质玻璃管;③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。

(1)根据B、C装置中的实验现象可推测分解产物中含有
(2)将装置B、C顺序颠倒能否达到原来的实验目的
(3)D装置中发生的主要反应的离子方程式是
(4)通过计算确定已分解的FeSO4物质的量(写出计算过程)
您最近一年使用:0次
2024-03-15更新
|
151次组卷
|
2卷引用:江苏省盐城市建湖高级中学2023-2024学年高一下学期期初测试(2月)化学试题
解题方法
8 . 氯气是一种重要的化工原料,大量用于制造盐酸、漂白剂、农药、染料和药品等。
(1)1774年,瑞典化学家舍勒将浓盐酸与软锰矿(主要成分为 )混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
)混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
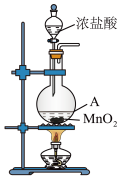
盛放浓盐酸的仪器名称是_______ 。
(2)下图所示制取氯气的净化、收集、尾气处理的装置能达到实验目的的是_______ 。(填序号)
(3)已知:常温下用 和市售浓盐酸(11.9
和市售浓盐酸(11.9 )反应制取Cl2难以进行。但若用漂白粉(有效成分
)反应制取Cl2难以进行。但若用漂白粉(有效成分 )、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。
)、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。
①已知,如图装置A是氯气的发生装置。加入适量的浓盐酸充分反应有黄绿色气体生成,写出发生反应的化学方程式,并用单线桥标明电子转移的方向和数目 :_______ 。

②装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅲ处应放入的是_______ (填序号)。
a.干燥的有色布条 b.湿润的有色布条 c.湿润的淀粉 试纸
试纸
装置C的Ⅱ处的试剂是_______ (填序号)。
a.碱石灰(氢氧化钠和氧化钙的固体混合物) b.无水氯化钙 c.浓硫酸
③装置D中一般不用 澄清石灰水吸收多余的氯气。理由是_______ 。
(4)84消毒液是一种常见的含氯消毒剂,其有效成分为次氯酸钠。
资料:84消毒液中含氯微粒主要有 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;
; 是反映水溶液中所有物质表现出来的氧化—还原性,
是反映水溶液中所有物质表现出来的氧化—还原性, 值越大,氧化性越强。
值越大,氧化性越强。
某兴趣小组同学研究84消毒液的漂白性,实验如下。
I.向2 84消毒液中加入2
84消毒液中加入2 水后,放入红色纸片,观察到纸片慢慢褪色。
水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.向2 84消毒液中加入2
84消毒液中加入2 白醋后,放入红色纸片,观察到纸片迅速褪色。
白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.测得84消毒液在不同温度时 随时间的变化曲线如
随时间的变化曲线如图 。
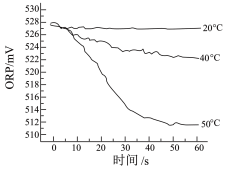
①已知白醋显酸性,不具有漂白性。实验I、Ⅱ现象不同的原因是_______ 。
②由实验Ⅲ可得出的结论是_______ 。
(1)1774年,瑞典化学家舍勒将浓盐酸与软锰矿(主要成分为
 )混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
)混合加热,发现了氯气。下图为实验室制取Cl2的装置,请回答:
盛放浓盐酸的仪器名称是
(2)下图所示制取氯气的净化、收集、尾气处理的装置能达到实验目的的是
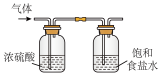 | 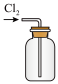 |  |
| A.净化Cl2 | B.收集Cl2 | C.尾气处理 |
(3)已知:常温下用
 和市售浓盐酸(11.9
和市售浓盐酸(11.9 )反应制取Cl2难以进行。但若用漂白粉(有效成分
)反应制取Cl2难以进行。但若用漂白粉(有效成分 )、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。
)、高锰酸钾等与浓盐酸反应,常温下很容易制取Cl2。①已知,如图装置A是氯气的发生装置。加入适量的浓盐酸充分反应有黄绿色气体生成,写出发生反应的化学方程式,并用

②装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅲ处应放入的是
a.干燥的有色布条 b.湿润的有色布条 c.湿润的淀粉
 试纸
试纸装置C的Ⅱ处的试剂是
a.碱石灰(氢氧化钠和氧化钙的固体混合物) b.无水氯化钙 c.浓硫酸
③装置D中一般
(4)84消毒液是一种常见的含氯消毒剂,其有效成分为次氯酸钠。
资料:84消毒液中含氯微粒主要有
 、
、 、
、 ;相同浓度时,
;相同浓度时, 的氧化性强于
的氧化性强于 ;
; 是反映水溶液中所有物质表现出来的氧化—还原性,
是反映水溶液中所有物质表现出来的氧化—还原性, 值越大,氧化性越强。
值越大,氧化性越强。某兴趣小组同学研究84消毒液的漂白性,实验如下。
I.向2
 84消毒液中加入2
84消毒液中加入2 水后,放入红色纸片,观察到纸片慢慢褪色。
水后,放入红色纸片,观察到纸片慢慢褪色。Ⅱ.向2
 84消毒液中加入2
84消毒液中加入2 白醋后,放入红色纸片,观察到纸片迅速褪色。
白醋后,放入红色纸片,观察到纸片迅速褪色。Ⅲ.测得84消毒液在不同温度时
 随时间的变化曲线如
随时间的变化曲线如
①已知白醋显酸性,不具有漂白性。实验I、Ⅱ现象不同的原因是
②由实验Ⅲ可得出的结论是
您最近一年使用:0次
名校
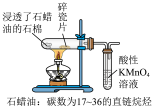
9 . 下列实验方案不能达到实验目的的是
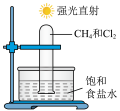
| A.证明石蜡裂解产物中含有烯烃 | B.观察甲烷取代反应的现象 |
|
|
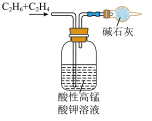
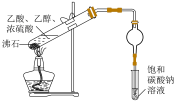
| C.除乙烷中乙烯,并得到纯净干燥的乙烷 | D.实验室制备乙酸乙酯 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 下列实验设计能达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 探究反应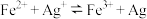 存在限度 存在限度 | 将0.1mol·L-1AgNO3溶液与0.21mol·L-1 溶液等体积混合后,取出两份混合液分别滴加KSCN溶液和 溶液等体积混合后,取出两份混合液分别滴加KSCN溶液和 溶液 溶液 |
| B | 探究浓度对反应速率的影响 | 向两支盛有5mL不同浓度KMnO4溶液的试管中分别加入同浓度同体积的足量草酸溶液,观察实验现象 |
| C | 检验某卤代烃中的是否含有氯元素 | 取卤代烃少许与NaOH乙醇溶液共热后,加入稀硝酸酸化,再加入AgNO3溶液,观察是否有白色沉淀生成 |
| D | 制备 晶体 晶体 | 向4mL0.1mol·L-1CuSO4溶液中滴加1mol·L-1氨水至沉淀溶解,再加入8mL95%乙醇,过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次