21-22高一上·广东深圳·期中
名校
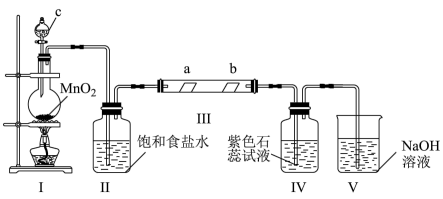
1 . 某校化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
(1)实验室以二氧化锰和浓盐酸制备氯气的化学方程式为_______ 。
(2)装置Ⅱ的作用是_______ 。
(3)若产生 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象_______ 。
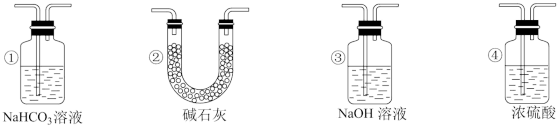
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的_______ 装置(填序号)。
(5)有一种“地康法”制取氯气的反应原理如图所示:
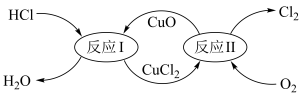
①反应Ⅰ属于_______ 反应。(填四种基本反应类型之一)
②在450℃条件下,反应Ⅱ的化学方程式为_______ 。
③工业生产中常用氨气检查输送氯气的管道是否有 泄漏。若
泄漏。若 有泄漏,可以观察到有大量的白烟生成(为
有泄漏,可以观察到有大量的白烟生成(为 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:_______ 。
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
(1)实验室以二氧化锰和浓盐酸制备氯气的化学方程式为
(2)装置Ⅱ的作用是
(3)若产生
 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)有一种“地康法”制取氯气的反应原理如图所示:

①反应Ⅰ属于
②在450℃条件下,反应Ⅱ的化学方程式为
③工业生产中常用氨气检查输送氯气的管道是否有
 泄漏。若
泄漏。若 有泄漏,可以观察到有大量的白烟生成(为
有泄漏,可以观察到有大量的白烟生成(为 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
您最近一年使用:0次
2021-11-21更新
|
591次组卷
|
4卷引用:甘肃省金昌市永昌县第一高级中学2022-2023学年高一上学期期末考试化学试题
甘肃省金昌市永昌县第一高级中学2022-2023学年高一上学期期末考试化学试题(已下线)广东省深圳市深圳中学2021-2022学年高一上学期期中考试化学试题江西省吉安市峡江中学2021-2022学年高二上学期开学考试化学(理科)试题湖南省长沙市实验中学2023-2024学年高一上学期期中考试化学试题
名校
2 . 实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2、水蒸气等无机物。某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型。回答下列问题:
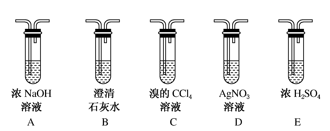
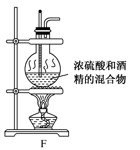
(1)写出制备乙烯反应的化学方程式___ 。加热F装置时必须使液体温度___ 。
(2)为实现上述实验目的,装置的连接顺序为F→___ →D。(各装置限用一次);其中B装置的作用___ 。
(3)当C中观察到___ 时,表明单质溴能与乙烯反应;当D中___ 时,表明C中发生的是取代反应;若D没有出现前面所描述的现象时,表明C中发生的是___ 反应。


(1)写出制备乙烯反应的化学方程式
(2)为实现上述实验目的,装置的连接顺序为F→
(3)当C中观察到
您最近一年使用:0次
2021-06-22更新
|
94次组卷
|
2卷引用:甘肃省天水市第一中学2021-2022学年高二下学期第一阶段考试化学试题
名校
3 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。 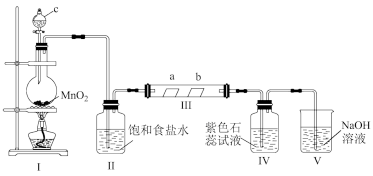
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸制备氯气的离子方程式为___________ ,HCl在反应中体现的性质为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
(5)工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:___________ 。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
您最近一年使用:0次
4 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
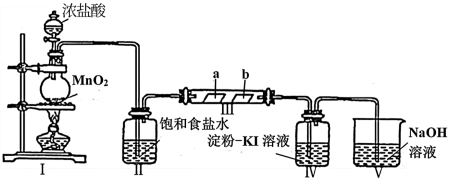
(1)实验室用MnO2和浓盐酸制备Cl2的化学方程式为___________ 。
(2)实验过程中装置Ⅳ中的实验现象为___________ 。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加如图中的___________ (填序号)装置。
(4)装置V的作用___________ ,写出装置V中发生反应的化学方程式___________

(1)实验室用MnO2和浓盐酸制备Cl2的化学方程式为
(2)实验过程中装置Ⅳ中的实验现象为
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加如图中的

(4)装置V的作用
您最近一年使用:0次
5 . 根据下列实验目的、操作及现象所得结论正确的是
| 选项 | 实验目的 | 操作及现象 | 结论 |
| A | 比较CH3COO-和HCO 的水解常数 的水解常数 | 分别测定浓度均为0.1mol•L-1的CH3COONH4和NaHCO3溶液的pH,后者大于前者 | Kh(CH3COO-)<Kh(HCO ) ) |
| B | 向FeI2溶液中滴几滴新制氯水,再加适量苯,振荡 | 溶液分层,下层呈浅绿色,上层呈紫红色 | 还原性:Fe2+>I- |
| C | 由乙二醇加酸性高锰酸酸钾溶液 | 有气泡产生 | 向乙二醇中滴加过量酸性高锰钾溶液无法制备乙二酸 |
| D | 向0.1mol•L-1ZnSO4溶液中加入过量Na2S溶液,再滴入0.1mol•L-1CuSO4溶液 | 先产生白色沉淀,后产生黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验。
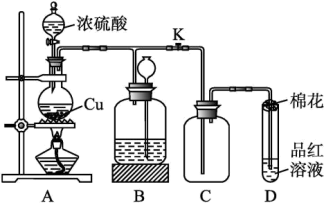
(1)装置A中发生反应的化学方程式为___________
(2)装置D中试管口放置的棉花应浸一种溶液,这种溶液是___________ 其作用是___________
(3)装置B的作用是___________ 当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是___________ B中应放置的液体是___________ (填字母)
A.水 B.酸性高锰酸钾 C.浓溴水 D.饱和NaHSO3
(4)实验中,取一定质量的铜片和一定体积18 mol•L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,下列药品能用来证明反应结束后的烧瓶中有余酸的是___________ (填字母)。
a.铁粉 b.BaCl2溶液 c.银粉 d.Na2CO3溶液
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色。为了证明蓝色只与Cu2+有关,而与其他离子无关,某同学设计了下列实验,其中对实验目的没有意义的是___________ 。(填序号)
①观察稀硫酸溶液呈无色;②观察CuSO4粉末呈白色;③稀释CuSO4溶液,溶液蓝色变浅;④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色;⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色。

(1)装置A中发生反应的化学方程式为
(2)装置D中试管口放置的棉花应浸一种溶液,这种溶液是
(3)装置B的作用是
A.水 B.酸性高锰酸钾 C.浓溴水 D.饱和NaHSO3
(4)实验中,取一定质量的铜片和一定体积18 mol•L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,下列药品能用来证明反应结束后的烧瓶中有余酸的是
a.铁粉 b.BaCl2溶液 c.银粉 d.Na2CO3溶液
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色。为了证明蓝色只与Cu2+有关,而与其他离子无关,某同学设计了下列实验,其中对实验目的没有意义的是
①观察稀硫酸溶液呈无色;②观察CuSO4粉末呈白色;③稀释CuSO4溶液,溶液蓝色变浅;④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色;⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色。
您最近一年使用:0次
2021-04-06更新
|
131次组卷
|
3卷引用:甘肃省白银市白银区大成学校2021-2022学年高一下学期期中考试化学试题
7 . 某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一:制取氯酸钾和氯水。
利用如图所示的实验装置(部分夹持装置已省略)进行实验。
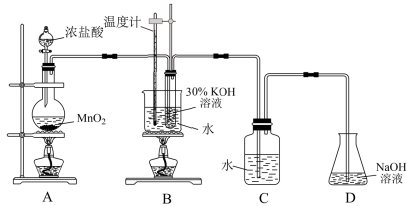
(1)写出A中发生反应的化学方程式为___________________________________ 。
(2)制取实验结束后,取出B中试管冷却结晶、过滤洗涤。过滤时需要用到的玻璃仪器有胶头滴管、烧杯、________ 、________ 。
(3)写出D装置中处理尾气的离子方程式________ 。
实验二:氯酸钾、碘化钾反应的探究
(4)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
①系列a实验的实验目的 ________________________________________
②设计1号试管实验的作用是________________________________________
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为________________________________________
实验三:比较Cl2、Br2、I2的氧化性强弱。
为比较Cl2、Br2、I2的氧化性强弱,设计了如图所示的实验步骤:
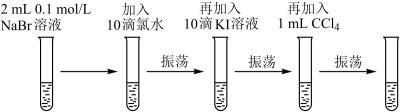
(5)加入10滴KI溶液时,溶液的颜色由橙黄色变为橙红色,说明氧化性:Br2___ I2 (填“强于”或“弱于”)
(6)加入1mL CCl4后,振荡静置,最终试管中的现象为____________
实验一:制取氯酸钾和氯水。
利用如图所示的实验装置(部分夹持装置已省略)进行实验。

(1)写出A中发生反应的化学方程式为
(2)制取实验结束后,取出B中试管冷却结晶、过滤洗涤。过滤时需要用到的玻璃仪器有胶头滴管、烧杯、
(3)写出D装置中处理尾气的离子方程式
实验二:氯酸钾、碘化钾反应的探究
(4)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
试管编号 | 1 | 2 | 3 | 4 |
0.20mol•L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0mol•L-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
实验现象 |
②设计1号试管实验的作用是
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为
实验三:比较Cl2、Br2、I2的氧化性强弱。
为比较Cl2、Br2、I2的氧化性强弱,设计了如图所示的实验步骤:

(5)加入10滴KI溶液时,溶液的颜色由橙黄色变为橙红色,说明氧化性:Br2
(6)加入1mL CCl4后,振荡静置,最终试管中的现象为
您最近一年使用:0次
名校
8 . 某兴趣小组利用下列装置进行实验,其中能达到实验目的的是
|
|
|
|
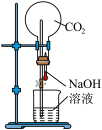
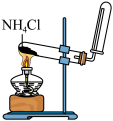
| A.喷泉实验 | B.验证压强对平衡的影响 | C.制备 | D.制取无水 固体 固体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一:制取氯酸钾和氯水。利用如图所示的实验装置(部分夹持装置已省略)进行实验。

(1)将Cl2通入B装置中得到的含氯产物为KClO3和KCl,该反应的离子方程式为_______ 。
(2)制取实验结束后,取出B中试管冷却结晶、过滤洗涤。过滤时需要用到的玻璃仪器有胶头滴管、烧杯、________ 、________ 。
(3)写出D装置中处理尾气的离子方程式_________ 。
实验二:氯酸钾碘化钾反应的探究
(4)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如图(实验在室温下进行):
①系列a实验的实验目的_______
②设计1号试管实验的作用是_____
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为________
实验三:比较Cl2、Br2、I2的氧化性强弱。为比较Cl2、Br2、I2的氧化性强弱,设计了如图所示的实验步骤:

(5)加入10滴KI溶液时,溶液的颜色由橙黄色变为橙红色,说明氧化性:Br2___ I2 (填“强于”或“弱于”)
(6)加入1mLCCl4后,振荡静置,最终试管中的现象为________
实验一:制取氯酸钾和氯水。利用如图所示的实验装置(部分夹持装置已省略)进行实验。

(1)将Cl2通入B装置中得到的含氯产物为KClO3和KCl,该反应的离子方程式为
(2)制取实验结束后,取出B中试管冷却结晶、过滤洗涤。过滤时需要用到的玻璃仪器有胶头滴管、烧杯、
(3)写出D装置中处理尾气的离子方程式
实验二:氯酸钾碘化钾反应的探究
(4)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如图(实验在室温下进行):
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol•L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol•L-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
| 实验现象 |
②设计1号试管实验的作用是
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为
实验三:比较Cl2、Br2、I2的氧化性强弱。为比较Cl2、Br2、I2的氧化性强弱,设计了如图所示的实验步骤:

(5)加入10滴KI溶液时,溶液的颜色由橙黄色变为橙红色,说明氧化性:Br2
(6)加入1mLCCl4后,振荡静置,最终试管中的现象为
您最近一年使用:0次
名校
10 . 下列实验目的、装置、现象及对应反应的离子方程式或化学方程式均正确的是
| 选项 | 目的 | 装置 | 现象 | 离子方程式或化学方程式 |
| A | 鉴别Br2(g)与NO2(g) |  | 通入NO2所得溶液呈无色;通入Br2(g)所得溶液呈黄色 | 3NO2+H2O = 2HNO3+NO Br2+H2O = 2H ++Br-+BrO- |
| B | 验证SO2的性质 | 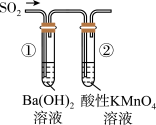 | ①中出现浑浊②中颜色变浅 | ①SO2+Ba2++2OH-=BaSO3↓+H2O ②5SO2+H2O+2MnO  =5SO =5SO +2Mn2++4H+ +2Mn2++4H+ |
| C | 实验室制取氯气 | 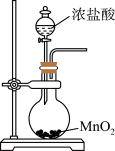 | 产生黄绿色气体 | 2Cl- + 4H+ + MnO2 = Mn2++ Cl2↑ + 2H2O |
| D | 检验NH |  | 蓝色石蕊试纸变红 | NH + OH- + OH- NH3↑ + H2O NH3↑ + H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-11-02更新
|
880次组卷
|
7卷引用:甘肃省静宁县第一中学2021届高三上学期第四次模拟考试化学试题