10. 研究二氧化硫、氮氧化物等大气污染物的治理具有重要意义,请回答下列问题:
I.为减少SO
2的排放,将煤转化为清洁气体燃料。已知:
2H
2(g)+O
2(g)=2H
2O(g) Δ
H=-483.6 kJ·mol
-1 C(s)+

O
2(g)=CO(g) Δ
H=-110.4 kJ·mol
-1 (1)写出焦炭与水蒸气反应的热化学方程式
_________________________。
(2)洗涤含SO
2的烟气,含以下物质的溶液可作洗涤剂的是
____________________。
A.NaHSO
3 B.NaHCO
3 C.BaCl
2 D.FeCl
3 II.NO
x是汽车尾气中的主要污染物之一。
(3)汽车尾气中生成NO的反应为:N
2(g)+O
2(g)
⇌2NO(g)
Δ
H>0
①T ℃时,2 L密闭气缸中充入4 mol N
2和1 mol O
2发生反应,5 min后达平衡,测得NO为1 mol。计算该温度下,N
2的平均反应速率
v(N
2)=
_______________,反应的平衡常数
K=
____________。
②如图曲线 a 表示该反应在温度T ℃下N
2的物质的量随时间的变化,曲线 b 表示该反应在某一起始条件改变时N
2的物质的量随时间的变化,则改变的条件可能是
____________ (写出一条即可)III.汽车燃油不完全燃烧时会产生CO。

(4)有人设想按2CO(g)=2C(s)+O
2(g)反应除去CO,但事实上该反应在任何温度下都不能实现,由此判断该反应的Δ
H_______0。(填写“>”、“<”或者“=”)
(5)在汽车尾气系统中安装催化转化器可降低尾气中污染物的排放,其反应为:2NO(g)+2CO(g)
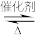
2CO
2(g)+N
2(g)。已知该反应在570 K时的平衡常数的数值为1×10
59,但反应速率极慢。为了提高尾气的净化效率在实际操作中最可行的措施是
_____。
A.升高温度
B.增大压强
C.使用高效催化剂