名校
解题方法
1 . 某校化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
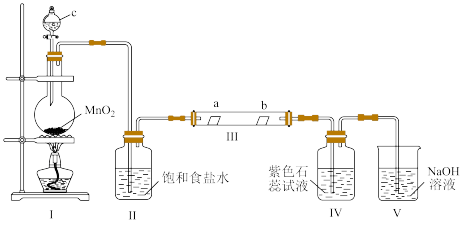
(1)装置Ⅰ中仪器c的名称是_______ ,实验室以二氧化锰和浓盐酸制备氯气的离子方程式,为_______ 。
(2)装置Ⅱ的作用是_______ 。
(3)若产生 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象_______ 。
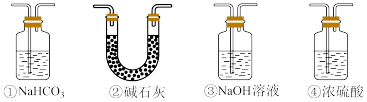
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是井未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的_______ 装置(填序号)。
(5)实验结束后,欲回收利用装置Ⅰ中未反应完的 ,除了玻璃棒还需要的玻璃仪器有
,除了玻璃棒还需要的玻璃仪器有_______ 。
(6)常温下装置Ⅴ反生反应的离子方程式为_______ 。
(7)有一种“地康法”制取氯气的反应原理如图所示:
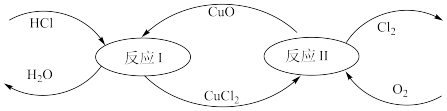
在450℃条件下,反应Ⅱ的化学方程式为_______ 。
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生
 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是井未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)实验结束后,欲回收利用装置Ⅰ中未反应完的
 ,除了玻璃棒还需要的玻璃仪器有
,除了玻璃棒还需要的玻璃仪器有(6)常温下装置Ⅴ反生反应的离子方程式为
(7)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应Ⅱ的化学方程式为
您最近一年使用:0次
2023-11-29更新
|
227次组卷
|
3卷引用:广东省惠州市惠州一中2023-2024学年高一上学期第二次阶段性考试化学试卷
2 . 实验室用 和浓盐酸反应制备
和浓盐酸反应制备 并回收
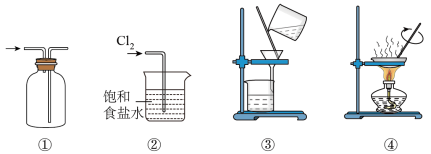
并回收 ,下列装置能达到实验目的的是
,下列装置能达到实验目的的是
 和浓盐酸反应制备
和浓盐酸反应制备 并回收
并回收 ,下列装置能达到实验目的的是
,下列装置能达到实验目的的是
A.用①收集 | B.用②吸收尾气 |
C.用③分离 和 和 溶液 溶液 | D.用④蒸干 溶液制 溶液制 |
您最近一年使用:0次
2023-03-16更新
|
1896次组卷
|
6卷引用:广东省广州市2023届高三一模考试化学试题
广东省广州市2023届高三一模考试化学试题(已下线)专题13 化学实验基础(已下线)广东省广州市天河区2023届高三二模化学试题变式题(选择题6-10)广东省广州市2022-2023学年高三普通高中毕业班综合测试(一)化学试题 上海市复旦大学附属中学2023-2024学年高一上学期期中考试化学试卷(B卷)上海市七宝中学2023-2024学年高一上学期化学12月练习卷
名校
解题方法
3 . 实验室用如图装置制备并收集干燥、纯净的 已知碳酸的酸性比次氯酸的强,回答下列问题:
已知碳酸的酸性比次氯酸的强,回答下列问题:
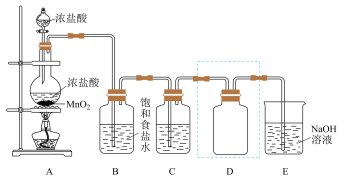
(1)装置A中发生反应的离子方程式是___________ 。
(2)装置B的作用是___________ 。
(3)装置C中盛放的物质是___________ 。
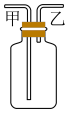
(4)装置D用于收集 ,装置D中进气方向为
,装置D中进气方向为___________ (填“甲”或“乙”),若在D中放入紫色石蕊溶液,则瓶内会出现什么现象___________ 。
(5)装置E用于吸收尾气,E中发生反应的化学方程式是___________ 。
(6)可用 和冷的石灰乳反应制备漂白粉,漂白粉有效成分是
和冷的石灰乳反应制备漂白粉,漂白粉有效成分是___________ (填化学式)。
(7)漂白粉常用于游泳池的消毒,起消毒作用的是HClO。漂白粉在水中释放HClO的途径如下:
途径一: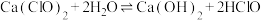
途径二: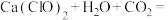
___________ (把反应补充完整)。
 已知碳酸的酸性比次氯酸的强,回答下列问题:
已知碳酸的酸性比次氯酸的强,回答下列问题:
(1)装置A中发生反应的离子方程式是
(2)装置B的作用是
(3)装置C中盛放的物质是
(4)装置D用于收集
 ,装置D中进气方向为
,装置D中进气方向为
(5)装置E用于吸收尾气,E中发生反应的化学方程式是
(6)可用
 和冷的石灰乳反应制备漂白粉,漂白粉有效成分是
和冷的石灰乳反应制备漂白粉,漂白粉有效成分是(7)漂白粉常用于游泳池的消毒,起消毒作用的是HClO。漂白粉在水中释放HClO的途径如下:
途径一:
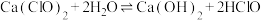
途径二:
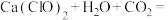
您最近一年使用:0次
名校
4 . 实验室用浓盐酸和MnO2制Cl2,并以干燥的Cl2为原料制备无水FeCl3.已知FeCl3易升华,易吸收水分而潮解, 常温下发生反应: ;
;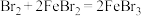 装置如下图所示。
装置如下图所示。

(1) 与浓盐酸反应的化学方程式
与浓盐酸反应的化学方程式___________ 。
(2)实验时,先点燃A处的酒精灯,让Cl2充满装置,再点燃D处酒精灯,写出D中反应的化学方程式:___________ 。
(3)有关上述实验的说法正确的是___________。
(4)F装置所起的作用是___________ 。
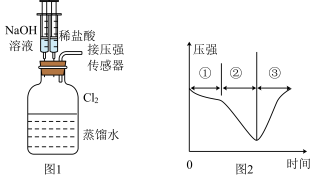
(5)用收集满氯气的D做如图1的实验:先添加适量的蒸馏水,振荡,然后用注射器滴加 溶液,再用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是___________(加入的
溶液,再用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是___________(加入的 液体和盐酸溶液的体积对压强的影响忽略不计)
液体和盐酸溶液的体积对压强的影响忽略不计)
 ;
;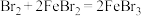 装置如下图所示。
装置如下图所示。
(1)
 与浓盐酸反应的化学方程式
与浓盐酸反应的化学方程式(2)实验时,先点燃A处的酒精灯,让Cl2充满装置,再点燃D处酒精灯,写出D中反应的化学方程式:
(3)有关上述实验的说法正确的是___________。
| A.实验开始后,D中现象:产生棕黄色烟雾 |
B.0.4mol浓盐酸与足量的 充分反应,反应中转移的电子数为 充分反应,反应中转移的电子数为 |
C.氯气可用于制漂白粉,漂白粉的有效成分为 和 和 |
D.少量氯水与 溶液反应的离子方程式为:Cl2+2Fe2+=2Fe3++ Cl- 溶液反应的离子方程式为:Cl2+2Fe2+=2Fe3++ Cl- |
(4)F装置所起的作用是
(5)用收集满氯气的D做如图1的实验:先添加适量的蒸馏水,振荡,然后用注射器滴加
 溶液,再用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是___________(加入的
溶液,再用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是___________(加入的 液体和盐酸溶液的体积对压强的影响忽略不计)
液体和盐酸溶液的体积对压强的影响忽略不计)
A.阶段①说明 溶于水,溶于水的 溶于水,溶于水的 全部与水反应 全部与水反应 |
B.阶段②的压强变小,说明 被 被 溶液完全吸收 溶液完全吸收 |
C.阶段③发生反应的离子方程式为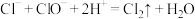 |
D.若将 换成 换成 ,所得的压强变化趋势可能与图2相似 ,所得的压强变化趋势可能与图2相似 |
您最近一年使用:0次
5 . 实验室为制备和收集少量干燥、纯净的氯气,选用如图所示仪器及药品:

(1)上述实验中,用来盛放浓盐酸的仪器的名称是____________ ,装置F的作用________________________ 。
(2)制取氯气的离子反应方程式为__________________ 。
(3)选择上述仪器并按顺序连接(填各接口处的字母):a→______ →k→g→i。
(4)如图是一组探究氯气性质的装置。现关闭活塞K,若有色布条是干燥的,溶液A为浓硫酸,则有色布条______ (填现象,下同)。

(5)现打开K,溶液A为氢氧化钠溶液,通入的氯气是湿润的,布条是干燥的,则有色布条______ 。
(6)制得的Cl2通过盛有饱和食盐水的装置,目的是________________________ 。
(7)Cl2通入双氧水(H2O2)水溶液中会产生使带有火星的木条复燃,写出在水溶液中Cl2和H2O2反应的离子方程式__________________ 。

(1)上述实验中,用来盛放浓盐酸的仪器的名称是
(2)制取氯气的离子反应方程式为
(3)选择上述仪器并按顺序连接(填各接口处的字母):a→
(4)如图是一组探究氯气性质的装置。现关闭活塞K,若有色布条是干燥的,溶液A为浓硫酸,则有色布条

(5)现打开K,溶液A为氢氧化钠溶液,通入的氯气是湿润的,布条是干燥的,则有色布条
(6)制得的Cl2通过盛有饱和食盐水的装置,目的是
(7)Cl2通入双氧水(H2O2)水溶液中会产生使带有火星的木条复燃,写出在水溶液中Cl2和H2O2反应的离子方程式
您最近一年使用:0次
名校
6 . 某小组在实验室用NaClO溶液和NH3反应制备N2H4,并进行相关的性质探究实验。
I.制备N2H4
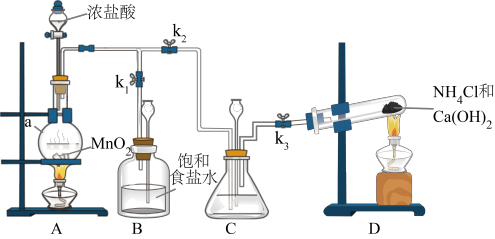
(1)装置C中盛放的试剂是___________ ,其作用是___________ 。(用离子方程式表示)
(2)装置D发生的反应的方程式为___________ 。
(3)制备N2H4的离子方程式为___________ 。
II.探究N2H4的还原性与碱性。将制得的肼分离提纯后,进行如图实验。
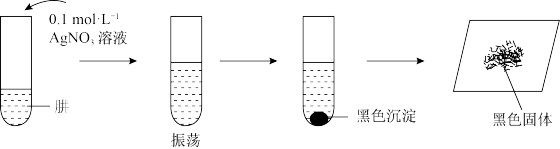
【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如表方案,进行实验。
(4)请完成表中的空白部分
(5)实验表明,黑色固体主要成分是Ag,还有少量氧化银。请解释原因:___________ 。
I.制备N2H4

(1)装置C中盛放的试剂是
(2)装置D发生的反应的方程式为
(3)制备N2H4的离子方程式为
II.探究N2H4的还原性与碱性。将制得的肼分离提纯后,进行如图实验。

【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如表方案,进行实验。
(4)请完成表中的空白部分
| 操作 | 现象 | 实验结论 |
| i. 取少量黑色固体于试管中,加入适量 | 黑色固体部分溶解 | 黑色固体有Ag2O |
| ii. 取少量黑色固体于试管中加入足量稀硝酸,振荡。 | 黑色固体是Ag和Ag2O |
您最近一年使用:0次
名校
解题方法
7 . 如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略),回答下列问题:

已知: 、
、 、
、 在苯中的溶解度大于在水中的溶解度。
在苯中的溶解度大于在水中的溶解度。 溶解在苯中为紫红色。
溶解在苯中为紫红色。
(1)用二氧化锰和浓盐酸制备氯气的离子方程式为_______ ,装置B中饱和食盐水的作用是_______ ,同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象_______ 。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处最好依次放入_______ (填序号,不能重复使用)。
①干燥的有色布条 ②湿润的有色布条 ③碱石灰 ④无水氯化钙 ⑤浓硫酸
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性,反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是E中溶液分为两层,上层(苯层)为紫红色,下层为无色,该现象_______ (填“能”或“不能”)说明溴单质的氧化性强于碘。
(4)装置F中用足量的NaOH溶液吸收余氯气,反应的离子方程式为_______ 。
(5)如果将过量二氧化锰与20mL 的浓盐酸混合加热,充分反应后生成的氯气
的浓盐酸混合加热,充分反应后生成的氯气_______ 0.06mol(填“大于”、“小于”或“等于”)。
(6)用下列方法制取氯气:
①
②
③
若要制得相同质量的氯气,上述三种方法中所转移的电子数目之比是_______ 。

已知:
 、
、 、
、 在苯中的溶解度大于在水中的溶解度。
在苯中的溶解度大于在水中的溶解度。 溶解在苯中为紫红色。
溶解在苯中为紫红色。(1)用二氧化锰和浓盐酸制备氯气的离子方程式为
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处最好依次放入
①干燥的有色布条 ②湿润的有色布条 ③碱石灰 ④无水氯化钙 ⑤浓硫酸
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性,反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是E中溶液分为两层,上层(苯层)为紫红色,下层为无色,该现象
(4)装置F中用足量的NaOH溶液吸收余氯气,反应的离子方程式为
(5)如果将过量二氧化锰与20mL
 的浓盐酸混合加热,充分反应后生成的氯气
的浓盐酸混合加热,充分反应后生成的氯气(6)用下列方法制取氯气:
①

②

③

若要制得相同质量的氯气,上述三种方法中所转移的电子数目之比是
您最近一年使用:0次
名校
8 . 某化学兴趣小组设计了如图装置制取 进行相关性质实验,并模拟工业生产无水氯化铁的过程。
进行相关性质实验,并模拟工业生产无水氯化铁的过程。

资料:①工业上向500~600℃的铁屑中通入氯气生产无水氯化铁。②无水氯化铁有强烈的吸水性,能吸收空气中的水分而潮解变质。装置G中的液体是饱和氯化钠溶液,用于储存反应后多余的氯气。
根据各小题的要求,填写下列空白:
(1)装置A中装浓盐酸的玻璃仪器名称为_______ ,A中发生反应的离子方程式为_______ 。
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①装置B中发生反应的化学方程式为_______ 。
②装置C和D中看到的实验现象分别是_______ 、_______ 。
(3)若要得到较纯净的无水氯化铁,上述装置的改进措施是:_______ 。
(4)将装置A中制备的氯气通入适量水中制备氯水,用胶头滴管将新制氯水慢慢滴入含有酚酞的氢氧化钠稀溶液中,当滴到一定量时,红色突然褪去。回答下列问题:
①红色突然褪去的原因可能是_______ 、_______ 。
②怎样用实验证明红色褪去的原因?_______ 。
 进行相关性质实验,并模拟工业生产无水氯化铁的过程。
进行相关性质实验,并模拟工业生产无水氯化铁的过程。
资料:①工业上向500~600℃的铁屑中通入氯气生产无水氯化铁。②无水氯化铁有强烈的吸水性,能吸收空气中的水分而潮解变质。装置G中的液体是饱和氯化钠溶液,用于储存反应后多余的氯气。
根据各小题的要求,填写下列空白:
(1)装置A中装浓盐酸的玻璃仪器名称为
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①装置B中发生反应的化学方程式为
②装置C和D中看到的实验现象分别是
(3)若要得到较纯净的无水氯化铁,上述装置的改进措施是:
(4)将装置A中制备的氯气通入适量水中制备氯水,用胶头滴管将新制氯水慢慢滴入含有酚酞的氢氧化钠稀溶液中,当滴到一定量时,红色突然褪去。回答下列问题:
①红色突然褪去的原因可能是
②怎样用实验证明红色褪去的原因?
您最近一年使用:0次
9 . 某学习小组欲制备氯水和漂白粉,并利用所制溶液进行相关实验探究。实验装置如图所示。回答有关问题。
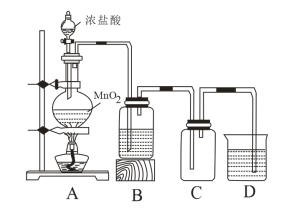
(1)装置A中生成氯气的离子方程式为___________ 。
(2)装置B的作用是吸收氯气带出的HCl气体,所装的试剂为___________ 。装置C用于制备氯水,应装入的试剂是___________ ,装置D中盛有___________ ,可以在防止___________ 的同时制备漂白粉。
(3)小组同学用上述实验中得到的氯水进行如下实验
根据该小组的实验报告,回答下列问题:
①实验i中发生反应的离子方程式为___________ 。
②实验ii的结论是否严谨?___________ (填“是”或“否”),理由是___________ 。
③实验iii中溶液红色褪去的原因,除了酸碱中和反应外,还有一种可能:___________ 。如要证明到底是什么原因使溶液褪色,还需进一步设计实验验证。

(1)装置A中生成氯气的离子方程式为
(2)装置B的作用是吸收氯气带出的HCl气体,所装的试剂为
(3)小组同学用上述实验中得到的氯水进行如下实验
| 实验序号 | 试剂和操作 | 实验现象 | 结论 |
| i | 在4mLNaBr溶液中加入1mL氯水 | 溶液变黄色 | 氯气的氧化性比溴强 |
| ii | 在4mLKI溶液中加入实验i所得黄色溶液 | 溶液变为棕黄色 | 溴的氧化性比碘强 |
| iii | 在滴有酚酞的NaOH溶液中滴加氯水 | 当氯水滴到一定量时,溶液红色突然褪去 | 氯水显酸性 |
①实验i中发生反应的离子方程式为
②实验ii的结论是否严谨?
③实验iii中溶液红色褪去的原因,除了酸碱中和反应外,还有一种可能:
您最近一年使用:0次
名校
解题方法
10 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分置省略)制备KClO3和NaClO,探究其氧化还原性质。
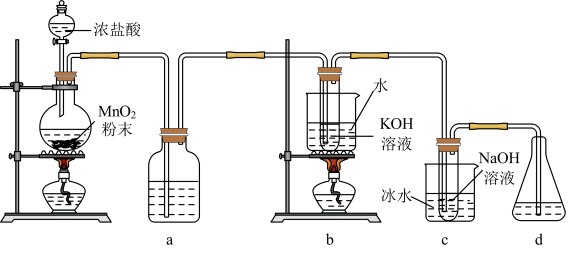
回答下列问题:
(1)制取氯气时,在圆底烧瓶里加入一定量的二氧化锰,通过___ (填写仪器名称)向烧瓶中加入适量的浓盐酸,请写出该反应的化学方程式:___ 。
(2)实验时为了除去氯气中的氯化氢气体,a装置中应加入___ (填写下列编号字母)。
(3)b中采用的加热方式是___ ,c装置用于制取NaClO,发生反应的离子方程式是___ ,采用冰水浴冷却的目的是___ 。
(4)在不同条件下KClO3可将KI氧化为I2或KClO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如表(实验在室温下进行):
①系列a实验的实验目的是___ 。
②设计1号试管实验的作用是___ 。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为:___ 。

回答下列问题:
(1)制取氯气时,在圆底烧瓶里加入一定量的二氧化锰,通过
(2)实验时为了除去氯气中的氯化氢气体,a装置中应加入
| A.碱石灰 | B.饱和食盐水 | C.浓硫酸 | D.饱和碳酸氢钠溶液 |
(4)在不同条件下KClO3可将KI氧化为I2或KClO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如表(实验在室温下进行):
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol/LKI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol/LH2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水 | 9.0 | 6.0 | 3.0 | 0 |
②设计1号试管实验的作用是
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为:
您最近一年使用:0次



