名校
1 . 氯气是一种化学性质很活泼的非金属单质,其具有较强的氧化性。下列叙述中不正确的是
| A.实验室制取氯气时,为了防止污染环境,多余的氯气可用澄清石灰水吸收 |
| B.钠在氯气中燃烧,生成白色的烟 |
| C.氯气能与水反应生成次氯酸和盐酸,久置的氯水最终变为稀盐酸 |
| D.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 |
您最近一年使用:0次
2023-11-27更新
|
161次组卷
|
2卷引用:安徽省淮北市第十二中学2023-2024学年高一上学期11月期中考试化学试题
名校
2 . “84”消毒液是常见的含氯消毒剂,其主要成分是次氯酸钠,在防控新冠疫情过程中发挥了重要作用。某化学兴趣小组设计了如图所示的制备装置。

已知: 。请回答:
。请回答:
(1)A中发生反应的化学方程式为___________ 。
(2)B中所加试剂的作用是___________ 。
(3)同学甲查阅资料后发现 与NaOH的反应会放热,由此他认为NaClO的产率会较低。为此他对装置进行了改进,其改进的措施是
与NaOH的反应会放热,由此他认为NaClO的产率会较低。为此他对装置进行了改进,其改进的措施是___________ 。
(4)同学乙认为该制备装置还存在一个较大的缺点,请你指出___________ 。
(5)为探究NaClO溶液的性质,某兴趣小组进行以下实验:
i.取C中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。
ii.将步骤i中蓝色溶液滴入浓盐酸中,蓝色迅速褪去,同时产生少量黄绿色气体。
步骤ii中产生黄绿色气体的离子方程式为___________ 。
(6)已知氯气和NaOH溶液在一定温度下能同时发生反应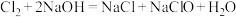 、
、 。某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和
。某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和 的混合溶液,经测定反应后的溶液中
的混合溶液,经测定反应后的溶液中 与
与 的个数比为2:3,则氯气与氢氧化钠反应时,被还原的氯原子和被氧化的氯原子的个数比为
的个数比为2:3,则氯气与氢氧化钠反应时,被还原的氯原子和被氧化的氯原子的个数比为___________ 。

已知:
 。请回答:
。请回答:(1)A中发生反应的化学方程式为
(2)B中所加试剂的作用是
(3)同学甲查阅资料后发现
 与NaOH的反应会放热,由此他认为NaClO的产率会较低。为此他对装置进行了改进,其改进的措施是
与NaOH的反应会放热,由此他认为NaClO的产率会较低。为此他对装置进行了改进,其改进的措施是(4)同学乙认为该制备装置还存在一个较大的缺点,请你指出
(5)为探究NaClO溶液的性质,某兴趣小组进行以下实验:
i.取C中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。
ii.将步骤i中蓝色溶液滴入浓盐酸中,蓝色迅速褪去,同时产生少量黄绿色气体。
步骤ii中产生黄绿色气体的离子方程式为
(6)已知氯气和NaOH溶液在一定温度下能同时发生反应
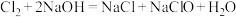 、
、 。某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和
。某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和 的混合溶液,经测定反应后的溶液中
的混合溶液,经测定反应后的溶液中 与
与 的个数比为2:3,则氯气与氢氧化钠反应时,被还原的氯原子和被氧化的氯原子的个数比为
的个数比为2:3,则氯气与氢氧化钠反应时,被还原的氯原子和被氧化的氯原子的个数比为
您最近一年使用:0次
3 . 某日,某国国家公共广播电视台报道了一起学校发生氯气泄漏的事件,该事故的起因是有人引爆了清洁游泳池用的氯片。
(1)氯气是___________ 色的有毒气体。
(2)若鲜花沾到泄漏的氯气,会褪去原来的颜色,其原因是Cl2与H2O反应生成具有漂白性的次氯酸,该反应的化学方程式为___________ 。
(3)实验室可通过如图所示的装置制备氯气。

①仪器A的名称为___________ 。
②若想除去Cl2中的HCl气体,则需要对装置进行改进,方法是___________ 。
③D装置的作用是___________ ,写出其中发生的主要反应的离子方程式:___________ 。
(1)氯气是
(2)若鲜花沾到泄漏的氯气,会褪去原来的颜色,其原因是Cl2与H2O反应生成具有漂白性的次氯酸,该反应的化学方程式为
(3)实验室可通过如图所示的装置制备氯气。

①仪器A的名称为
②若想除去Cl2中的HCl气体,则需要对装置进行改进,方法是
③D装置的作用是
您最近一年使用:0次
2023-11-08更新
|
50次组卷
|
2卷引用:安徽省六安市舒城晓天中学2023-2024学年高一上学期期中考试化学试卷
解题方法
4 . 将氯气缓慢通过内有湿润的红纸条的广口瓶(如图所示),下列说法错误的是
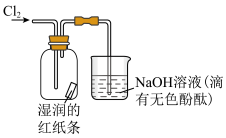

| A.常温常压下,氯气是一种密度比空气大的气体 |
| B.一段时间后,可观察到湿润的红纸条褪色 |
| C.烧杯中的溶液可换成饱和氯化钠溶液进行尾气处理 |
| D.烧杯中可能发生反应的化学方程式为3Cl2+6NaOH=5NaCl+NaClO3+3H2O |
您最近一年使用:0次
2023-11-08更新
|
123次组卷
|
3卷引用:安徽省六安市舒城晓天中学2023-2024学年高一上学期期中考试化学试卷
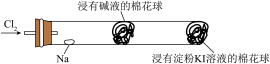
5 . “绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如下所示装置(部分装置已省略),先给钠预热,当钠熔融成圆球时,撤去酒精灯,通入氯气,即可观察到钠着火燃烧,产生大量白烟。下列叙述错误的是(已知 ,
, 遇淀粉变蓝)
遇淀粉变蓝)
 ,
, 遇淀粉变蓝)
遇淀粉变蓝)
| A.钠着火燃烧产生苍白色火焰 |
| B.反应生成的大量白烟是氯化钠晶体 |
C.塞一团浸有 溶液的棉球是用于吸收过量的氯气,以免其污染空气 溶液的棉球是用于吸收过量的氯气,以免其污染空气 |
| D.根据管右端棉球颜色的变化可判断氯气是否被碱溶液完全吸收 |
您最近一年使用:0次
2023-11-08更新
|
130次组卷
|
2卷引用:安徽省六安市舒城晓天中学2023-2024学年高一上学期期中考试化学试卷
6 . 某学习小组探究潮湿的Cl2与Na2CO3反应的产物,进行如图实验:

请回答:
(1)试剂X是________ 。
(2)请写出装置A中的化学方程式________ 。
(3)装置C中潮湿的Cl2与Na2CO3以等物质的量反应,生成NaHCO3、气体Cl2O和NaCl,试写出该反应化学方程式________ 。
(4)写出氯气进入装置E发生反应的化学方程式________ 。
(5)若将上述装置中的C、D、E部分换成如图所述装置,其中I与III是干燥的有色布条,E中盛装NaOH溶液,请回答下列问题:
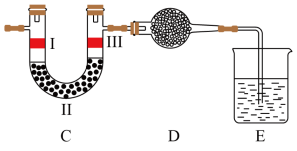
①装置C的作用是验证氯气是否具有漂白性,则装置C中II的作用是________ 。
②D中应装入的物质是________ 。
a.浓硫酸 b.生石灰 c.NaCl固体 d.NaOH固体

请回答:
(1)试剂X是
(2)请写出装置A中的化学方程式
(3)装置C中潮湿的Cl2与Na2CO3以等物质的量反应,生成NaHCO3、气体Cl2O和NaCl,试写出该反应化学方程式
(4)写出氯气进入装置E发生反应的化学方程式
(5)若将上述装置中的C、D、E部分换成如图所述装置,其中I与III是干燥的有色布条,E中盛装NaOH溶液,请回答下列问题:

①装置C的作用是验证氯气是否具有漂白性,则装置C中II的作用是
②D中应装入的物质是
a.浓硫酸 b.生石灰 c.NaCl固体 d.NaOH固体
您最近一年使用:0次
2023-10-24更新
|
508次组卷
|
5卷引用:安徽省合肥市六校联盟2023-2024学年高一上学期11月期中化学试题
名校
7 . 下图为部分含氯物质的价类二维图。下列说法错误 的是
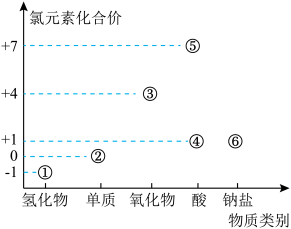

| A.⑤的化学式为HClO4 |
| B.①和⑥反应生成1mol Cl2,消耗⑥的质量为74.5g |
| C.工业上将②通入氢氧化钠溶液中制取⑥ |
| D.因③具有强还原性,常用于自来水消毒 |
您最近一年使用:0次
名校
解题方法
8 . 将一定量的氯气通入0.50 mol的氢氧化钠浓溶液中,加热少许时间后,溶液中形成NaCl、NaClO、 共存体系(不考虑氯气和水的反应)。下列说法正确的是
共存体系(不考虑氯气和水的反应)。下列说法正确的是
 共存体系(不考虑氯气和水的反应)。下列说法正确的是
共存体系(不考虑氯气和水的反应)。下列说法正确的是| A.若反应中转移的电子为n mol,则0.25<n<0.5 |
B.溶液中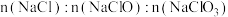 可能为4∶3∶1 可能为4∶3∶1 |
| C.与NaOH反应的氯气为0.5 mol |
D.当溶液中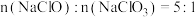 时,反应中氧化剂与还原剂的物质的量之比为5∶3 时,反应中氧化剂与还原剂的物质的量之比为5∶3 |
您最近一年使用:0次
2023-10-11更新
|
819次组卷
|
5卷引用:安徽省安庆市怀宁县高河中学2023-2024学年高一上学期第二次月考化学试题
解题方法
9 . 化学方程式是一种重要的化学语言。下列化学方程式能够正确表示对应变化的是
| A | 工业上制备漂白粉 |  |
| B | 供氢剂 与水反应 与水反应 |  |
| C | 过量铁和氯气反应 | 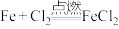 |
| D | 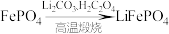 | 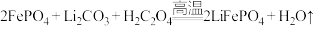  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 次氯酸盐具有强氧化性。在碱性条件下,利用 氧化
氧化 生成高铁酸钾
生成高铁酸钾 的工艺流程如下:
的工艺流程如下:
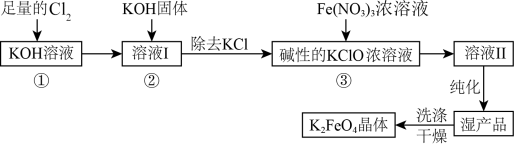
已知:①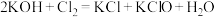 (条件:温度较低);
(条件:温度较低);
②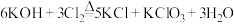 (条件:温度较高)。
(条件:温度较高)。
回答下列问题:
(1)反应①应在
(2)在溶液I中加入
 固体的目的是
固体的目的是(3)从溶液Ⅱ中分离出
 后,还会有副产品
后,还会有副产品 、
、 ,则反应③中发生的离子反应方程式为
,则反应③中发生的离子反应方程式为(4)
 可作饮用水处理剂,该反应的离子方程式:
可作饮用水处理剂,该反应的离子方程式: ,
, 处理水中悬浮颗粒物的原理是
处理水中悬浮颗粒物的原理是(5)目前,人们针对
 的稳定性进行了大量的探索,并取得了一定的进展。下列物质中有可能提高
的稳定性进行了大量的探索,并取得了一定的进展。下列物质中有可能提高 水溶液稳定性的物质是___________(填字母)。
水溶液稳定性的物质是___________(填字母)。A. | B. | C. | D. |
您最近一年使用:0次
2023-09-21更新
|
347次组卷
|
3卷引用:安徽省合肥六校联考2023-2024学年高三上学期期中联考化学试题



