名校
解题方法
1 . 某小组同学探究不同条件下氯气与二价锰化合物的反应。
资料:
i.Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ii.浓碱条件下, 可被OH-还原为
可被OH-还原为 。
。
iii. Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
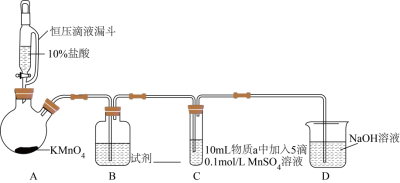
(1)A中反应的离子方程式为_______ ,B中试剂是_______ 。
(2)通入Cl2前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为_______ 。
(3)对比实验I、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是_______ 。
(4)根据资料ii,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①化学方程式表示可能导致溶液碱性减弱的原因_______ ,但通过实验测定溶液的碱性变化很小。
②取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为_______ ,溶液绿色缓慢加深,原因是MnO2被_______ (填“化学式”)氧化,可证明Ⅲ的悬浊液中氧化剂过量。
③取Ⅱ中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生的反应是_______ 。
资料:
i.Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、
 (绿色)、
(绿色)、 (紫色)。
(紫色)。ii.浓碱条件下,
 可被OH-还原为
可被OH-还原为 。
。iii. Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
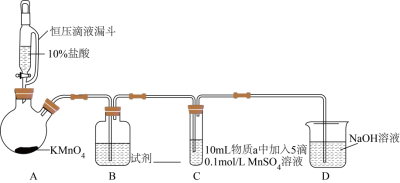
| 序号 | 物质a | C中实验现象 | |
| 通入Cl2前 | 通入Cl2后 | ||
| I | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| Ⅱ | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| Ⅲ | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(1)A中反应的离子方程式为
(2)通入Cl2前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为
(3)对比实验I、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是
(4)根据资料ii,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为 。
。①化学方程式表示可能导致溶液碱性减弱的原因
②取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
③取Ⅱ中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生的反应是
您最近一年使用:0次
名校
解题方法
2 . 次氯酸盐具有强氧化性。在碱性条件下,利用KClO氧化Fe(NO3)3生成高铁酸钾K2FeO4的工艺流程如下:
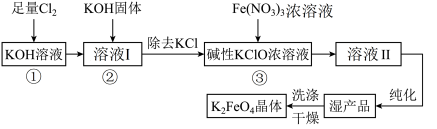
已知:6KOH+3Cl2=5KCl+KClO3+3H2O
回答下列问题:
(1)反应①应在___________ (填“温度较高”或“温度较低”)的情况下进行,该反应的离子方程式为___________ 。
(2)在溶液I中加入KOH固体的目的是___________ 。
(3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为___________ 。
(4)K2FeO4可作饮用水处理剂,该反应的离子方程式:4FeO +10H2O=4Fe(OH)3(体)+3O2↑+8OH-,K2FeO4处理水中悬浮颗粒物的原理是
+10H2O=4Fe(OH)3(体)+3O2↑+8OH-,K2FeO4处理水中悬浮颗粒物的原理是___________ ;K2FeO4可用于杀菌消毒的原因是___________ 。
(5)该工艺每得到1.98kgK2FeO4,理论上消耗Cl2物质的量为___________ mol。

已知:6KOH+3Cl2=5KCl+KClO3+3H2O
回答下列问题:
(1)反应①应在
(2)在溶液I中加入KOH固体的目的是
(3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为
(4)K2FeO4可作饮用水处理剂,该反应的离子方程式:4FeO
 +10H2O=4Fe(OH)3(体)+3O2↑+8OH-,K2FeO4处理水中悬浮颗粒物的原理是
+10H2O=4Fe(OH)3(体)+3O2↑+8OH-,K2FeO4处理水中悬浮颗粒物的原理是(5)该工艺每得到1.98kgK2FeO4,理论上消耗Cl2物质的量为
您最近一年使用:0次
2024-01-19更新
|
256次组卷
|
3卷引用:湖北省沙市中学2023-2024学年高一上学期11月月考化学试题
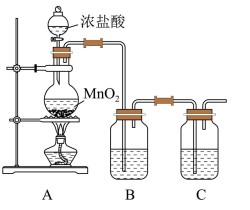
3 . 某化学兴趣小组设计了如图所示的装置制备NaClO溶液并就其性质进行探究。
已知: 。请回答:
。请回答:
(1)A中发生反应的化学方程式为___________ 。
(2)氯气溶于水的离子方程式为:___________ ,B中所加试剂的名称是___________ 。
(3)同学甲查阅资料后发现Cl2与NaOH的反应会放热,导致题干中副反应的发生。由此他预测NaClO的热稳定性___________ (填“好”或者“不好”);该方案制得的NaClO溶液粗品中含有的杂质可能有___________ 、___________ (用物质的化学式表达,下同),一定有___________ 。
(4)为探究NaClO溶液的性质,某同学进行以下实验:
取少量C中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。将该蓝色溶液滴入浓盐酸中,蓝色迅速褪去,同时产生少量黄绿色气体。产生黄绿色气体的离子方程式为___________ 。
(5)NaClO溶液露置于空气中,消毒效果先增强,而将其光照后消毒效果又降低。请用方程式表示光照后消毒效果降低的原因:___________ ;最终该溶液中的溶质变为_______ (用相应物质化学式表示)。
(6)某温度下,将氯气通入NaOH溶液中,被还原的氯原子和被氧化的氯原子的个数比为7:5,反应后生成的三种钠盐中氯元素的化合价分别为+5、+1、−1,这三种钠盐的物质的量之比为1:___:___。_______

已知:
 。请回答:
。请回答:(1)A中发生反应的化学方程式为
(2)氯气溶于水的离子方程式为:
(3)同学甲查阅资料后发现Cl2与NaOH的反应会放热,导致题干中副反应的发生。由此他预测NaClO的热稳定性
(4)为探究NaClO溶液的性质,某同学进行以下实验:
取少量C中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。将该蓝色溶液滴入浓盐酸中,蓝色迅速褪去,同时产生少量黄绿色气体。产生黄绿色气体的离子方程式为
(5)NaClO溶液露置于空气中,消毒效果先增强,而将其光照后消毒效果又降低。请用方程式表示光照后消毒效果降低的原因:
(6)某温度下,将氯气通入NaOH溶液中,被还原的氯原子和被氧化的氯原子的个数比为7:5,反应后生成的三种钠盐中氯元素的化合价分别为+5、+1、−1,这三种钠盐的物质的量之比为1:___:___。
您最近一年使用:0次
名校
4 . 下列离子方程式正确的是
| A.“84”消毒液和洁厕灵混合:ClO-+Cl-+2H+=Cl2↑+H2O |
| B.工业制漂白粉的离子方程式:2OH-+Cl2=ClO-+Cl-+H2O |
C.向酸性KMnO4溶液中滴加双氧水:2MnO +H2O2+6H+=2Mn2++3O2↑+4H2O +H2O2+6H+=2Mn2++3O2↑+4H2O |
| D.还原性I->Fe2+,FeI2与一定量Cl2反应:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
您最近一年使用:0次
解题方法
5 . 下列离子方程式正确的是
A.两种含氯物质发生化合反应: |
B.两种盐恰好发生氧化还原反应: |
C.证明氧化性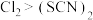 的反应: 的反应: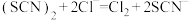 |
D.在足量烧碱溶液中氯元素发生歧化反应: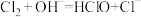 |
您最近一年使用:0次
2023-04-27更新
|
256次组卷
|
2卷引用:湖北省十堰市2023届高三下学期调研考试化学试题
22-23高一上·广东揭阳·期末
解题方法
6 . 已知实验室常用二氧化锰粉末和浓盐酸制取氯气,某实验小组用下图所示装置制取纯净干燥的氯气。
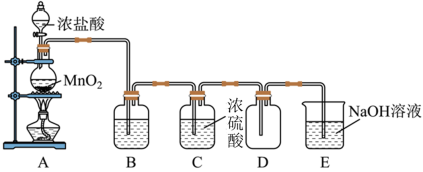
请回答下列问题:
(1)装置A中所发生反应的化学方程式为_______ ,B是除杂装置,盛放的试剂是_______ ;
(2)C装置利用了浓硫酸的_______ (填“吸水性”“脱水性”或“强氧化性”);
(3)该制取过程中,收集氯气的方法是_______ (填“A”或“B”);
A.向下排空气法 B.向上排空气法
(4)为防止Cl2污染环境,E烧杯中盛装的是_______ ,请写出该反应的化学方程式_______ ;
(5)欲制取2.24L标准状况下的Cl2,至少需要MnO2的质量为_______ g(Mn:相对原子质量为55)。

请回答下列问题:
(1)装置A中所发生反应的化学方程式为
(2)C装置利用了浓硫酸的
(3)该制取过程中,收集氯气的方法是
A.向下排空气法 B.向上排空气法
(4)为防止Cl2污染环境,E烧杯中盛装的是
(5)欲制取2.24L标准状况下的Cl2,至少需要MnO2的质量为
您最近一年使用:0次



