名校
解题方法
1 . 某小组同学探究不同条件下氯气与二价锰化合物的反应。
资料:
i.Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ii.浓碱条件下, 可被OH-还原为
可被OH-还原为 。
。
iii. Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
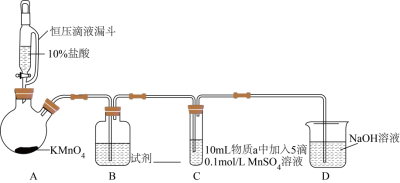
(1)A中反应的离子方程式为_______ ,B中试剂是_______ 。
(2)通入Cl2前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为_______ 。
(3)对比实验I、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是_______ 。
(4)根据资料ii,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①化学方程式表示可能导致溶液碱性减弱的原因_______ ,但通过实验测定溶液的碱性变化很小。
②取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为_______ ,溶液绿色缓慢加深,原因是MnO2被_______ (填“化学式”)氧化,可证明Ⅲ的悬浊液中氧化剂过量。
③取Ⅱ中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生的反应是_______ 。
资料:
i.Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、
 (绿色)、
(绿色)、 (紫色)。
(紫色)。ii.浓碱条件下,
 可被OH-还原为
可被OH-还原为 。
。iii. Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
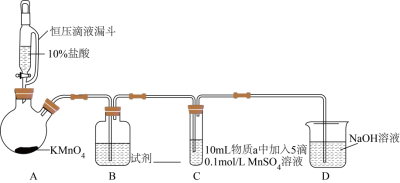
| 序号 | 物质a | C中实验现象 | |
| 通入Cl2前 | 通入Cl2后 | ||
| I | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| Ⅱ | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| Ⅲ | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(1)A中反应的离子方程式为
(2)通入Cl2前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为
(3)对比实验I、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是
(4)根据资料ii,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为 。
。①化学方程式表示可能导致溶液碱性减弱的原因
②取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
③取Ⅱ中放置后的1mL悬浊液,加入4mL水,溶液紫色缓慢加深,发生的反应是
您最近半年使用:0次
名校
解题方法
2 . 叠氮化钠( )不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(
)不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼( )并利用其进一步反应制取
)并利用其进一步反应制取 的流程如下:
的流程如下:
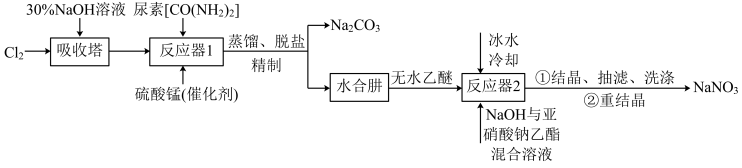
已知:① 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 ;
;
②一定条件下,碱性NaClO溶液与尿素溶液反应生成 。
。
回答下列问题:
(1)吸收塔内发生反应的离子方程式为_______ 。
(2)写出反应器1中生成水合肼反应的化学方程式:_______ 。
(3)反应器2中加入无水乙醚的作用是_______ 。
(4)已知亚硝酸乙酯的结构简式为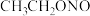 ,反应器2中生成
,反应器2中生成 和
和 。若生成39g
。若生成39g  ,则该反应中转移电子的物质的量为
,则该反应中转移电子的物质的量为_______ 。
(5)反应器1要控制NaClO溶液的用量,其主要目的是_______ 。
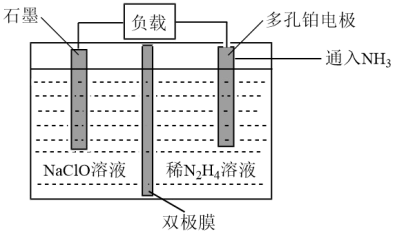
(6)某实验室设计了如图所示装置制备 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
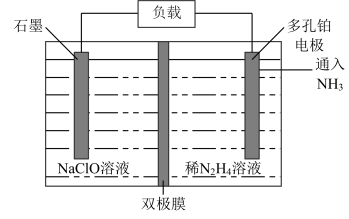
①双极膜中产生的_______ (填“ ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。
②石墨电极反应式为_______ 。
 )不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(
)不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼( )并利用其进一步反应制取
)并利用其进一步反应制取 的流程如下:
的流程如下:
已知:①
 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 ;
;②一定条件下,碱性NaClO溶液与尿素溶液反应生成
 。
。回答下列问题:
(1)吸收塔内发生反应的离子方程式为
(2)写出反应器1中生成水合肼反应的化学方程式:
(3)反应器2中加入无水乙醚的作用是
(4)已知亚硝酸乙酯的结构简式为
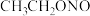 ,反应器2中生成
,反应器2中生成 和
和 。若生成39g
。若生成39g  ,则该反应中转移电子的物质的量为
,则该反应中转移电子的物质的量为(5)反应器1要控制NaClO溶液的用量,其主要目的是
(6)某实验室设计了如图所示装置制备
 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
①双极膜中产生的
 ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。②石墨电极反应式为
您最近半年使用:0次
名校
解题方法
3 . 叠氮化钠( )不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(
)不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼( )并利用其进一步反应制取
)并利用其进一步反应制取 的流程如下:
的流程如下:
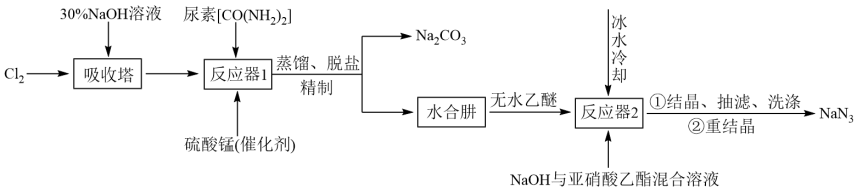
已知:① 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 ;
;
②一定条件下,碱性NaClO溶液与尿素溶液反应生成 。
。
回答下列问题:
(1)吸收塔内发生反应的离子方程式为_______ 。
(2)写出反应器1中生成水合肼反应的化学方程式:_______ 。
(3)反应器2中加入无水乙醚的作用是_______ 。
(4)已知亚硝酸乙酯的结构简式为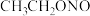 ,写出反应器2中生成
,写出反应器2中生成 和
和 的化学方程式:
的化学方程式:_______ 。若生成39g  ,则该反应中转移电子的物质的量为
,则该反应中转移电子的物质的量为_______ 。
(5)反应器1要控制NaClO溶液的用量,其主要目的是_______ 。
(6)某实验室设计了如图所示装置制备 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
①双极膜中产生的_______ (填“ ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。
②石墨电极反应式为_______ 。
 )不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(
)不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼( )并利用其进一步反应制取
)并利用其进一步反应制取 的流程如下:
的流程如下:
已知:①
 易溶于水,具有强还原性,易被氧化成
易溶于水,具有强还原性,易被氧化成 ;
;②一定条件下,碱性NaClO溶液与尿素溶液反应生成
 。
。回答下列问题:
(1)吸收塔内发生反应的离子方程式为
(2)写出反应器1中生成水合肼反应的化学方程式:
(3)反应器2中加入无水乙醚的作用是
(4)已知亚硝酸乙酯的结构简式为
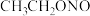 ,写出反应器2中生成
,写出反应器2中生成 和
和 的化学方程式:
的化学方程式: ,则该反应中转移电子的物质的量为
,则该反应中转移电子的物质的量为(5)反应器1要控制NaClO溶液的用量,其主要目的是
(6)某实验室设计了如图所示装置制备
 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
①双极膜中产生的
 ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。②石墨电极反应式为
您最近半年使用:0次
2022-04-16更新
|
574次组卷
|
5卷引用:湖北省九师联盟2022届高三 三模考试化学试题
湖北省九师联盟2022届高三 三模考试化学试题河北省名校联盟2021-2022学年高三下学期4月质量检测化学试题湖南省隆回县第一中学2022届高三下学期第二次模拟考试化学试题(已下线)考点13 钠及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点13 钠及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
解题方法
4 . 次氯酸盐具有强氧化性。在碱性条件下,利用KClO氧化Fe(NO3)3生成高铁酸钾K2FeO4的工艺流程如下:
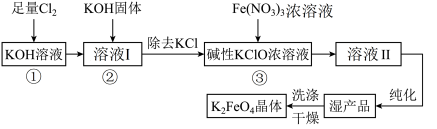
已知:6KOH+3Cl2=5KCl+KClO3+3H2O
回答下列问题:
(1)反应①应在___________ (填“温度较高”或“温度较低”)的情况下进行,该反应的离子方程式为___________ 。
(2)在溶液I中加入KOH固体的目的是___________ 。
(3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为___________ 。
(4)K2FeO4可作饮用水处理剂,该反应的离子方程式:4FeO +10H2O=4Fe(OH)3(体)+3O2↑+8OH-,K2FeO4处理水中悬浮颗粒物的原理是
+10H2O=4Fe(OH)3(体)+3O2↑+8OH-,K2FeO4处理水中悬浮颗粒物的原理是___________ ;K2FeO4可用于杀菌消毒的原因是___________ 。
(5)该工艺每得到1.98kgK2FeO4,理论上消耗Cl2物质的量为___________ mol。

已知:6KOH+3Cl2=5KCl+KClO3+3H2O
回答下列问题:
(1)反应①应在
(2)在溶液I中加入KOH固体的目的是
(3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为
(4)K2FeO4可作饮用水处理剂,该反应的离子方程式:4FeO
 +10H2O=4Fe(OH)3(体)+3O2↑+8OH-,K2FeO4处理水中悬浮颗粒物的原理是
+10H2O=4Fe(OH)3(体)+3O2↑+8OH-,K2FeO4处理水中悬浮颗粒物的原理是(5)该工艺每得到1.98kgK2FeO4,理论上消耗Cl2物质的量为
您最近半年使用:0次
2024-01-19更新
|
250次组卷
|
3卷引用:湖北省沙市中学2023-2024学年高一上学期11月月考化学试题
解题方法
5 . 氯水及氯的许多化合物是高效广谱的消毒剂,同时又是生产中重要的化工原料,根据所学知识,回答下列问题:
(1)新制的氯水呈淡黄色,向氯水中滴入几滴 溶液,现象是
溶液,现象是_______ ,说明新制氯水中有_______ 存在。
(2)某品牌的“84”消毒液含NaClO的质量分数约为6%,NaClO溶液能够杀灭新冠病毒的原因是具有_______ (填“强氧化性”或“强还原性”);为了较长时间保持NaClO溶液的杀菌能力,NaClO溶液应密闭避光保存,原因是_______ 。生活中,若不小心将“84”消毒液与洁厕剂(含有盐酸)混合,易生成_______ 气体(填化学式),能使人中毒。
(3)近些年来,科学家提出使用 对自来水进行消毒。以
对自来水进行消毒。以 和稀盐酸为原料可制备
和稀盐酸为原料可制备 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ ,在上述过程中被氧化和被还原的物质的物质的量之比为_______ 。
(1)新制的氯水呈淡黄色,向氯水中滴入几滴
 溶液,现象是
溶液,现象是(2)某品牌的“84”消毒液含NaClO的质量分数约为6%,NaClO溶液能够杀灭新冠病毒的原因是具有
(3)近些年来,科学家提出使用
 对自来水进行消毒。以
对自来水进行消毒。以 和稀盐酸为原料可制备
和稀盐酸为原料可制备 ,写出该反应的化学方程式:
,写出该反应的化学方程式:
您最近半年使用:0次
2021-12-07更新
|
184次组卷
|
2卷引用:湖北省十堰市2021-2022学年高一上学期期末调研考试化学试题
名校
解题方法
6 . 某化学实验小组同学用如图所示装置进行氯气系列实验以探究其性质,气体X是Cl2(部分仪器已略去),下列说法不正确的是( )
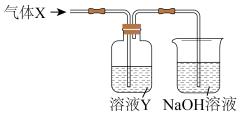

| A.若溶液Y为KI淀粉溶液,则可观察到广口瓶中溶液变蓝的实验现象 |
| B.X与NaOH溶液反应既体现其氧化性又体现其还原性 |
| C.若溶液Y为NaBr溶液,则可观察到广口瓶中溶液变蓝的实验现象 |
| D.若溶液Y为NaBr溶液,取广口瓶中反应后的溶液于试管中滴加几滴KI淀粉溶液观察到溶液变蓝,不能证明氧化性:Br2>I2 |
您最近半年使用:0次
7 . 科学家舍勒和戴维对氯气的制取和研究做出了重大贡献。某兴趣小组利用所给仪器在实验室制备纯净干燥的氯气,并模拟工业制漂白粉。请回答下列问题:
Ⅰ.实验室制备和收集氯气的常用装置如下图。
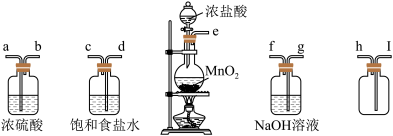
(1)利用该装置制备氯气的化学方程式为_______ 。
(2)在实验过程中饱和食盐水的作用是_______ 。
(3)实验装置接口的连接顺序为e→_______→_______→_______→_______→i→h→g→f。_______
(4)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中HCl的作用是还原性和_______ ,若反应产生0.5molCl2,则反应转移的电子数是_______ 。
II.漂白粉的制备( 装置如图所示)
查阅资料可知:①氯气与碱反应放出热量;
②6Cl2+6Ca(OH)2 CaCl2+Ca(ClO3)2+6H2O。
CaCl2+Ca(ClO3)2+6H2O。

(5)装置C中发生反应的化学方程式为_______ 。
(6)多孔球泡的作用是_______ ,使用冰水浴的目的是_______ 。
Ⅰ.实验室制备和收集氯气的常用装置如下图。

(1)利用该装置制备氯气的化学方程式为
(2)在实验过程中饱和食盐水的作用是
(3)实验装置接口的连接顺序为e→_______→_______→_______→_______→i→h→g→f。
(4)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中HCl的作用是还原性和
II.漂白粉的制备( 装置如图所示)
查阅资料可知:①氯气与碱反应放出热量;
②6Cl2+6Ca(OH)2
 CaCl2+Ca(ClO3)2+6H2O。
CaCl2+Ca(ClO3)2+6H2O。
(5)装置C中发生反应的化学方程式为
(6)多孔球泡的作用是
您最近半年使用:0次
8 . 某化学兴趣小组设计了如图所示的装置制备NaClO溶液并就其性质进行探究。
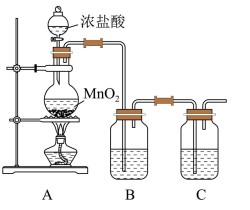
已知: 。请回答:
。请回答:
(1)A中发生反应的化学方程式为___________ 。
(2)氯气溶于水的离子方程式为:___________ ,B中所加试剂的名称是___________ 。
(3)同学甲查阅资料后发现Cl2与NaOH的反应会放热,导致题干中副反应的发生。由此他预测NaClO的热稳定性___________ (填“好”或者“不好”);该方案制得的NaClO溶液粗品中含有的杂质可能有___________ 、___________ (用物质的化学式表达,下同),一定有___________ 。
(4)为探究NaClO溶液的性质,某同学进行以下实验:
取少量C中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。将该蓝色溶液滴入浓盐酸中,蓝色迅速褪去,同时产生少量黄绿色气体。产生黄绿色气体的离子方程式为___________ 。
(5)NaClO溶液露置于空气中,消毒效果先增强,而将其光照后消毒效果又降低。请用方程式表示光照后消毒效果降低的原因:___________ ;最终该溶液中的溶质变为_______ (用相应物质化学式表示)。
(6)某温度下,将氯气通入NaOH溶液中,被还原的氯原子和被氧化的氯原子的个数比为7:5,反应后生成的三种钠盐中氯元素的化合价分别为+5、+1、−1,这三种钠盐的物质的量之比为1:___:___。_______

已知:
 。请回答:
。请回答:(1)A中发生反应的化学方程式为
(2)氯气溶于水的离子方程式为:
(3)同学甲查阅资料后发现Cl2与NaOH的反应会放热,导致题干中副反应的发生。由此他预测NaClO的热稳定性
(4)为探究NaClO溶液的性质,某同学进行以下实验:
取少量C中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。将该蓝色溶液滴入浓盐酸中,蓝色迅速褪去,同时产生少量黄绿色气体。产生黄绿色气体的离子方程式为
(5)NaClO溶液露置于空气中,消毒效果先增强,而将其光照后消毒效果又降低。请用方程式表示光照后消毒效果降低的原因:
(6)某温度下,将氯气通入NaOH溶液中,被还原的氯原子和被氧化的氯原子的个数比为7:5,反应后生成的三种钠盐中氯元素的化合价分别为+5、+1、−1,这三种钠盐的物质的量之比为1:___:___。
您最近半年使用:0次
名校
9 . 下列离子方程式正确的是
| A.“84”消毒液和洁厕灵混合:ClO-+Cl-+2H+=Cl2↑+H2O |
| B.工业制漂白粉的离子方程式:2OH-+Cl2=ClO-+Cl-+H2O |
C.向酸性KMnO4溶液中滴加双氧水:2MnO +H2O2+6H+=2Mn2++3O2↑+4H2O +H2O2+6H+=2Mn2++3O2↑+4H2O |
| D.还原性I->Fe2+,FeI2与一定量Cl2反应:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
您最近半年使用:0次
10 . 实验室利用以下反应可以快速制取少量氯气: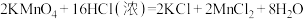
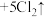 ,关于该反应的说法正确的是
,关于该反应的说法正确的是
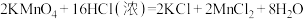
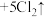 ,关于该反应的说法正确的是
,关于该反应的说法正确的是| A.由该反应判断氧化性:KMnO4>Cl2 |
| B.氧化剂与还原剂的物质的量之比为1:8 |
| C.可以用饱和NaHCO3溶液除去Cl2中混有的HCl |
| D.1 mol Cl2与足量的NaOH溶液充分反应制备“84”消毒液,转移电子的物质的量为2 mol |
您最近半年使用:0次



