1 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。

已知:①饱和食盐水可以除去氯气中混有的氯化氢气体。
②碘的 溶液显紫红色。
溶液显紫红色。
回答下列问题:
(1)写出圆底烧瓶中发生反应的离子方程式:___________ ,e装置的作用为___________ 。
(2)b中盛放的试剂为___________ 。
(3)取少量 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变;2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变;2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显紫红色。可知该条件下
层显紫红色。可知该条件下 的氧化能力
的氧化能力___________ (填“大于”或“小于”)NaClO。
(4)一定条件下,在一定量的NaOH溶液中通入一定量的氯气,二者恰好完全反应。生成物中除了含有氯离子外,还含有ClO、 两种离子,
两种离子, 、
、 两种离子的物质的量(n)与反应时间(t)的关系如图1所示。则该反应的离子方程式为
两种离子的物质的量(n)与反应时间(t)的关系如图1所示。则该反应的离子方程式为___________ 。

(5)某同学设计实验探究“84”消毒液的漂白性(已知该消毒液中存在反应: )。
)。
I.在2mL“84”消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL“84”消毒液中加入2mL盐酸后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得“84”消毒液ORP值随时间的变化关系如图2所示。
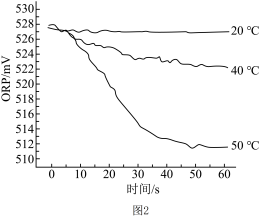
已知:ORP可以表示水溶液中物质的氧化性或还原性强弱。本实验中,ORP值越大,氧化性越强。
①实验I、Ⅱ现象不同的原因是___________ 。
②实验Ⅲ中,随温度的变化ORP值不同的原因可能是___________ 。
③针对不同物品的消毒,需将“84”消毒液稀释到不同的浓度。已知某品牌“84”消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释成8%的溶液,则需加水的质量为___________ g。
 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
已知:①饱和食盐水可以除去氯气中混有的氯化氢气体。
②碘的
 溶液显紫红色。
溶液显紫红色。回答下列问题:
(1)写出圆底烧瓶中发生反应的离子方程式:
(2)b中盛放的试剂为
(3)取少量
 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变;2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变;2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显紫红色。可知该条件下
层显紫红色。可知该条件下 的氧化能力
的氧化能力(4)一定条件下,在一定量的NaOH溶液中通入一定量的氯气,二者恰好完全反应。生成物中除了含有氯离子外,还含有ClO、
 两种离子,
两种离子, 、
、 两种离子的物质的量(n)与反应时间(t)的关系如图1所示。则该反应的离子方程式为
两种离子的物质的量(n)与反应时间(t)的关系如图1所示。则该反应的离子方程式为
(5)某同学设计实验探究“84”消毒液的漂白性(已知该消毒液中存在反应:
 )。
)。I.在2mL“84”消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL“84”消毒液中加入2mL盐酸后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得“84”消毒液ORP值随时间的变化关系如图2所示。

已知:ORP可以表示水溶液中物质的氧化性或还原性强弱。本实验中,ORP值越大,氧化性越强。
①实验I、Ⅱ现象不同的原因是
②实验Ⅲ中,随温度的变化ORP值不同的原因可能是
③针对不同物品的消毒,需将“84”消毒液稀释到不同的浓度。已知某品牌“84”消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释成8%的溶液,则需加水的质量为
您最近半年使用:0次
解题方法
2 . 钴是一种中等活泼金属,化合价为+2价和+3价,其中CoCl2易溶于水。某校同学设计实验制取(CH3COO)2Co(乙酸钴)并验证其分解产物。回答下列问题:
I.甲同学用Co2O3与盐酸反应制备CoCl2·4H2O,其实验装置如图:
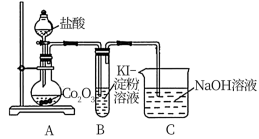
①烧瓶中发生反应的氧化剂和还原剂的物质的量之比为___________ 。
②装置B中的现象可以说明氧化性___________ >___________ ,从原子结构的角度解释___________ 。
II.乙同学利用甲同学制得的CoCl2·4H2O在醋酸氛围中制得无水(CH3COO)2Co,并利用下列装置检验(CH2COO)2Co在氮气气氛中的分解产物。已知PdCl2溶液能被CO还原为Pd。
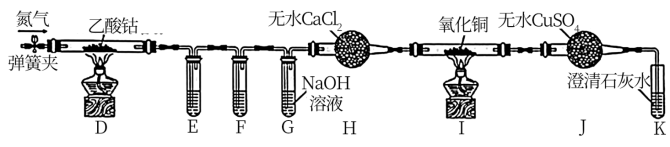
①装置E、F分别盛放___________ 和___________ 。
②E、F、G中的试剂均足量,观察到I中氧化铜变红,J中固体由白色变蓝色,K中石灰水变浑浊,则可得出的结论是___________ 。
③通入氮气的作用是___________ 。
I.甲同学用Co2O3与盐酸反应制备CoCl2·4H2O,其实验装置如图:

①烧瓶中发生反应的氧化剂和还原剂的物质的量之比为
②装置B中的现象可以说明氧化性
II.乙同学利用甲同学制得的CoCl2·4H2O在醋酸氛围中制得无水(CH3COO)2Co,并利用下列装置检验(CH2COO)2Co在氮气气氛中的分解产物。已知PdCl2溶液能被CO还原为Pd。

①装置E、F分别盛放
②E、F、G中的试剂均足量,观察到I中氧化铜变红,J中固体由白色变蓝色,K中石灰水变浑浊,则可得出的结论是
③通入氮气的作用是
您最近半年使用:0次
3 . 某小组使用下图装置制取并收集干燥、纯净的氯气,请回答下列问题:
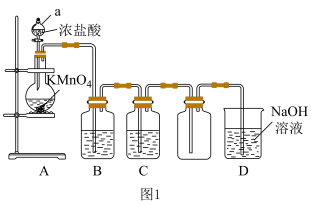
(1)①A装置中仪器a的名称是___________ ,KMnO4的作用是___________ 。
②已知KMnO4常温下即可与浓盐酸反应生成Cl2;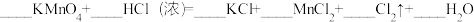 ,请配平化学方程式:
,请配平化学方程式:__________ ;其中做还原剂的HCl占参与反应的HCl的___________ (填分数)。
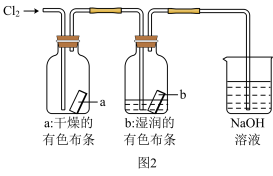
(2)B装置中盛放的试剂是___________ ,其作用是___________ 。D装置处理尾气时,使用NaOH溶液而不用澄清石灰水吸收氯气的原因是___________ 。若将图1收集到的氯气通入图2所示装置中,可观察到的现象为___________ 。
(3)查阅资料知次氯酸或氯气可被H2O2还原成Cl-,设计实验方案测定某氯水中氯元素质量:___________ 。

(1)①A装置中仪器a的名称是
②已知KMnO4常温下即可与浓盐酸反应生成Cl2;
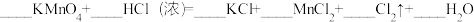 ,请配平化学方程式:
,请配平化学方程式:(2)B装置中盛放的试剂是

(3)查阅资料知次氯酸或氯气可被H2O2还原成Cl-,设计实验方案测定某氯水中氯元素质量:
您最近半年使用:0次
2023-11-06更新
|
173次组卷
|
3卷引用:山西省怀仁市第一中学校2023-2024学年高一上学期第二次月考理综化学试题
4 . 某研究性学习小组设计如下实验装置利用氯气与石灰乳反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
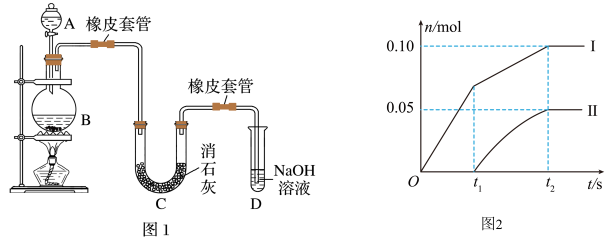
(1)A仪器的名称是_________ ,D的作用____________ 。
(2)漂白粉将在U形管中产生,其反应的化学方程式是____________________ 。
(3)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是__________ ,有同学测出了反应后溶液中ClO-、 两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为上图(不考虑氯气和水的反应)。
两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为上图(不考虑氯气和水的反应)。
a.图中曲线I表示_____________ 离子的物质的量随反应时间变化的关系。
b.所取石灰乳中含有Ca(OH)2的物质的量为______________ mol。
②试判断另一个副反应是(写出此反应方程式)__________________ ,为避免此副反应发生,可采取的措施是___________

(1)A仪器的名称是
(2)漂白粉将在U形管中产生,其反应的化学方程式是
(3)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
 两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为上图(不考虑氯气和水的反应)。
两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为上图(不考虑氯气和水的反应)。a.图中曲线I表示
b.所取石灰乳中含有Ca(OH)2的物质的量为
②试判断另一个副反应是(写出此反应方程式)
您最近半年使用:0次
名校
解题方法
5 . 下列说法正确的是
①氯气的性质活泼,它与氢气混合后立即发生爆炸
②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收
③新制氯水的氧化性强于久置氯水的
④检验HCl气体中是否混有Cl2的方法是将气体通入硝酸银溶液中
⑤除去HCl气体中的Cl2,可将气体通入饱和食盐水中
①氯气的性质活泼,它与氢气混合后立即发生爆炸
②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收
③新制氯水的氧化性强于久置氯水的
④检验HCl气体中是否混有Cl2的方法是将气体通入硝酸银溶液中
⑤除去HCl气体中的Cl2,可将气体通入饱和食盐水中
| A.①②③ | B.②③④ | C.③ | D.③⑤ |
您最近半年使用:0次
2020-08-23更新
|
1201次组卷
|
38卷引用:山西省应县第一中学校2019-2020学年高一上学期第四次月考化学试题
山西省应县第一中学校2019-2020学年高一上学期第四次月考化学试题山西省朔州市怀仁第一中学2018-2019学年高一上学期期末考试化学试题(已下线)2010年安丘中学高二暑期练习化学卷(四)(已下线)2013届江苏省灌南高级中学高三上学期期中考试化学试卷2014届河北省衡水中学高三上学期一调考试化学试卷(已下线)2014届江西省南昌二中高一下学期期中考试化学试卷(已下线)2015届福建省宁德第一中学高三上学期半期考试化学试卷2015届乌鲁木齐市高级中学高三上学期第二次月考化学卷2014-2015吉林省延边二中高一上学期期末考试化学试卷2016届新疆兵团农二师华山中学高三上学期第二次月考化学试卷2015-2016浙江宁波效实中学高一上期中考试化学试卷2015-2016学年河北省冀州中学高一上第五次月考化学试卷2015-2016学年安徽省六安一中高一上学期期末化学试卷(已下线)同步君 必修1 第4章 第2节 活泼的黄绿色气体—氯气高中化学人教版 必修1 第四章 非金属及其化合物 2.富集在海水中的元素——氯 活泼的黄绿色气体——氯气黑龙江省哈尔滨市第九中学2017-2018学年高一上学期期末考试化学试题【全国百强校】黑龙江省哈尔滨市第九中学2017-2018学年高一上学期期末考试化学试题【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高一下学期第一次月考(开学)化学试题【全国百强校】江苏省启东中学2018-2019学年高一下学期3月月考化学试题辽宁省六校协作体2019-2020学年高一上学期期中考试化学试题河北省承德第一中学2019-2020学年高一上学期期中考试化学试题2019年广东省汕头市高三第一次模拟考试化学试题(已下线)【新东方】 2020-33江西省九江市同文中学2019-2020学年度高一下学期期初考试化学试题(已下线)第02章 海水中的重要元素——钠和氯(A卷基础强化篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)(已下线)第14讲 富集在海水中的元素——卤素(精练)——2021年高考化学一轮复习讲练测(已下线)2.2.2 氯气的实验室制法-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)人教版(2019)高一必修第一册 第二章 海水中的重要元素 第二节 氯及其化合物 作业帮辽宁省黑山县黑山中学2020-2021学年高一10月月考化学试题山东省沂水县第四中学2020~2021学年高一上学期阶段检测化学试题高一必修第一册(苏教2019)专题3 第一单元 氯气及氯的化合物4甘肃省天水市第一中学2021-2022高一上学期第二次考试化学试题宁夏青铜峡市高级中学2021-2022学年高三上学期期中考试化学试题安徽省怀宁县第二中学2021-2022学年高三上学期第二次月考化学试题内蒙古赤峰市第四中学分校2021-2022学年高三上学期9月月考化学试题(已下线)【新东方】化学巩固练习56浙江省台州市路桥中学2023-2024学年高一上学期10月月考化学试题福建省“德化一中、永安一中、漳平一中”三校协作2023-2024学年高一上学期12月联考化学试题
解题方法
6 . 高铁酸盐是优良的多功能水处理剂。 为紫色固体,可溶于水,微溶于KOH浓溶液,难溶于有机物;在
为紫色固体,可溶于水,微溶于KOH浓溶液,难溶于有机物;在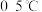 的强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出
的强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出 。某实验小组制备高铁酸钾
。某实验小组制备高铁酸钾 的装置如图所示。
的装置如图所示。
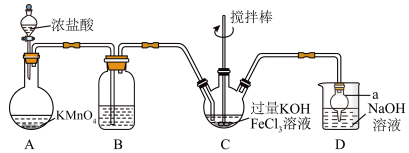
回答下列问题:
(1)仪器a的名称为_______ 。
(2)装置A中发生反应的离子方程式为_______ 。
(3)装置B中盛放的试剂为饱和氯化钠溶液,主要作用是除去挥发出来的氯化氢气体,还有一个作用是_______ 。
(4)装置C中生成 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为_______ 。C中混合物经重结晶、有机物洗涤纯化、真空干燥,得到高铁酸钾晶体。
(5)装置D中尾气处理时,除了生成 、
、 外,还有可能生成
外,还有可能生成_______ (填化学式)。
(6)往装有一定量的 晶体的试管中滴入稀硫酸,振荡。
晶体的试管中滴入稀硫酸,振荡。
①写出其发生反应的离子方程式:_______ 。
②检验生成气体为氧气的方法是_______ 。
 为紫色固体,可溶于水,微溶于KOH浓溶液,难溶于有机物;在
为紫色固体,可溶于水,微溶于KOH浓溶液,难溶于有机物;在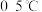 的强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出
的强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出 。某实验小组制备高铁酸钾
。某实验小组制备高铁酸钾 的装置如图所示。
的装置如图所示。
回答下列问题:
(1)仪器a的名称为
(2)装置A中发生反应的离子方程式为
(3)装置B中盛放的试剂为饱和氯化钠溶液,主要作用是除去挥发出来的氯化氢气体,还有一个作用是
(4)装置C中生成
 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为(5)装置D中尾气处理时,除了生成
 、
、 外,还有可能生成
外,还有可能生成(6)往装有一定量的
 晶体的试管中滴入稀硫酸,振荡。
晶体的试管中滴入稀硫酸,振荡。①写出其发生反应的离子方程式:
②检验生成气体为氧气的方法是
您最近半年使用:0次
2022-05-01更新
|
225次组卷
|
3卷引用:山西省长治市2021-2022学年高二下学期期末联考化学试题



