名校
解题方法
1 . 下列关系图中,A 是一种正盐,B 是气态氢化物,C 是单质,F 是强酸。当 X 无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当 X 是强碱时,过量的 B 跟 Cl2 反应除生成 C 外,另一产物是盐酸盐。
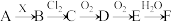
下列说法中不正确的是
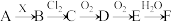
下列说法中不正确的是
| A.当 X 是强酸时,A、B、C、D、E、F 中均含同一种元素,F 可能是 H2SO4 |
| B.当 X 是强碱时,A、B、C、D、E、F 中均含同一种元素,F 是 HNO3 |
| C.用 O2 代替 Cl2, 也能与 B 反应生成 C 物质 |
| D.当 X 是强酸时,C 在常温下是一种易溶于酒精的固体 |
您最近一年使用:0次
2022-12-20更新
|
769次组卷
|
6卷引用:重庆市凤鸣山中学教育集团2021-2022学年高三上学期期中考试化学试题
2 . 氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。

(1)写出合成塔和氧化炉中发生反应的化学方程式____ ,并指出其中的氧化剂和还原剂__ 。
(2)请思考A是什么物质_______ ,以及向吸收塔中通入A的作用_________ 。
(3)工业生产中为了盛装大量浓硝酸,可选择_______ 作为罐体材料。
a.铜 b.铂 c.铝 d.镁
(4)为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。前者使用具有碱性的 溶液等吸收尾气,后者使用
溶液等吸收尾气,后者使用 或其他物质将氮氧化物还原为
或其他物质将氮氧化物还原为 。请以尾气中的
。请以尾气中的 处理为例,写出相关反应的化学方程式
处理为例,写出相关反应的化学方程式___ ,并查阅资料,了解还有哪些尾气处理方法______ 。

(1)写出合成塔和氧化炉中发生反应的化学方程式
(2)请思考A是什么物质
(3)工业生产中为了盛装大量浓硝酸,可选择
a.铜 b.铂 c.铝 d.镁
(4)为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。前者使用具有碱性的
 溶液等吸收尾气,后者使用
溶液等吸收尾气,后者使用 或其他物质将氮氧化物还原为
或其他物质将氮氧化物还原为 。请以尾气中的
。请以尾气中的 处理为例,写出相关反应的化学方程式
处理为例,写出相关反应的化学方程式
您最近一年使用:0次
2021-12-02更新
|
1394次组卷
|
2卷引用:人教2019版必修第二册第五章 化工生产中的重要非金属元素复习与提高
3 . 工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物),对生态环境和人类健康带来较大的威胁。
(1)工业上可用氨催化吸收法处理NOx,反应原理如下:4xNH3+6NOx (2x+3)N2+6xH2O。某化学兴趣小组模拟该处理过程的实验装置如图:
(2x+3)N2+6xH2O。某化学兴趣小组模拟该处理过程的实验装置如图:

①装置A中发生反应的化学方程式为___ 。
②装置D中碱石灰的作用是___ 。
(2)工业上也常用Na2CO3溶液吸收法处理NOx。
已知:NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3=2NaNO2+CO2(Ⅰ)
2NO2+Na2CO3=NaNO2+NaNO3+CO2(Ⅱ)
①当NOx被Na2CO3溶液完全吸收时,x的值不可能是___ (填字母)。
A.1.3B.1.6C.1.8
②将1molNOx通入Na2CO3溶液中,被完全吸收时,溶液中生成的NO 、NO
、NO 两种离子的物质的量随x变化关系如图所示。图中线段a表示
两种离子的物质的量随x变化关系如图所示。图中线段a表示___ 随x值变化的关系;若用溶质质量分数为21.2%的Na2CO3溶液吸收,则需要Na2CO3溶液至少___ g。

③用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则NOx中的x值为___ 。
(3)氨催化吸收法和Na2CO3溶液吸收法处理NOx尾气共同的优点是___ 。
(1)工业上可用氨催化吸收法处理NOx,反应原理如下:4xNH3+6NOx
 (2x+3)N2+6xH2O。某化学兴趣小组模拟该处理过程的实验装置如图:
(2x+3)N2+6xH2O。某化学兴趣小组模拟该处理过程的实验装置如图:
①装置A中发生反应的化学方程式为
②装置D中碱石灰的作用是
(2)工业上也常用Na2CO3溶液吸收法处理NOx。
已知:NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3=2NaNO2+CO2(Ⅰ)
2NO2+Na2CO3=NaNO2+NaNO3+CO2(Ⅱ)
①当NOx被Na2CO3溶液完全吸收时,x的值不可能是
A.1.3B.1.6C.1.8
②将1molNOx通入Na2CO3溶液中,被完全吸收时,溶液中生成的NO
 、NO
、NO 两种离子的物质的量随x变化关系如图所示。图中线段a表示
两种离子的物质的量随x变化关系如图所示。图中线段a表示
③用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则NOx中的x值为
(3)氨催化吸收法和Na2CO3溶液吸收法处理NOx尾气共同的优点是
您最近一年使用:0次
4 . 某校实验小组的同学利用如图所示实验装置探究氨与氧化铜的反应(图中夹持、固定装置部分均略去)。
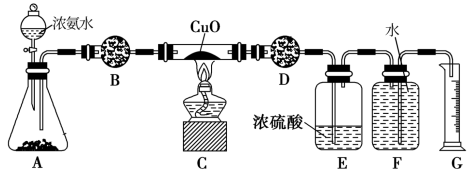
(1)A中盛放浓氨水的仪器的名称是___________ ,锥形瓶中的固体药品为一种纯净物,它是___________ 。
(2)B中固体试剂的作用为___________ 。
(3)打开分液漏斗活塞,加入试剂,点燃C处的酒精灯,一段时间后,观察到C中氧化铜全部转化成光亮的红色固体,经检验该红色固体为一种单质,F中集气瓶内收集到一种无色气态单质。写出装置C中反应的化学方程式:___________ 。
(4)E中浓硫酸的作用是___________ 。
(5)已知Cu2O也是红色的。表中数据为另一小组实验前后C装置的质量,通过计算可知反应后的产物中___________ (填“有”“无”或“无法确定”)Cu2O。

(1)A中盛放浓氨水的仪器的名称是
(2)B中固体试剂的作用为
(3)打开分液漏斗活塞,加入试剂,点燃C处的酒精灯,一段时间后,观察到C中氧化铜全部转化成光亮的红色固体,经检验该红色固体为一种单质,F中集气瓶内收集到一种无色气态单质。写出装置C中反应的化学方程式:
(4)E中浓硫酸的作用是
(5)已知Cu2O也是红色的。表中数据为另一小组实验前后C装置的质量,通过计算可知反应后的产物中
| 空玻璃管 | 实验前(样品+玻璃管) | 实验后(样品+玻璃管) |
| 59.60g | 65.60g | 64.64g |
您最近一年使用:0次
解题方法
5 . 工业上制取硝酸铵的流程图如图,请回答下列问题:
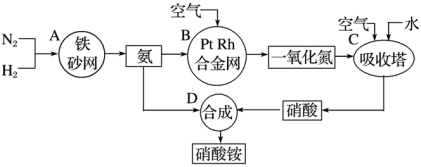
(1)在工业制硝酸的生产中,B中发生反应的化学方程式为:_______ 。
(2)在合成硝酸的吸收塔中通入空气的目的是:_______ 。
(3)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:NO+NO2+2NaOH2NaNO2+H2O
NH3还原法: NH3+ NO2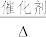 N2+ H2O
N2+ H2O
①配平NH3还原法的化学方程式_______ 。
②以上两种方法中,符合绿色化学的是_______ 。
③某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量占总耗NH3质量(不考虑其它损耗)的百分比含量为_______ (计算结果精确到0.1)。

(1)在工业制硝酸的生产中,B中发生反应的化学方程式为:
(2)在合成硝酸的吸收塔中通入空气的目的是:
(3)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:NO+NO2+2NaOH2NaNO2+H2O
NH3还原法: NH3+ NO2
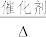 N2+ H2O
N2+ H2O①配平NH3还原法的化学方程式
②以上两种方法中,符合绿色化学的是
③某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量占总耗NH3质量(不考虑其它损耗)的百分比含量为
您最近一年使用:0次
名校
6 . 在一定温度和催化剂作用下,NO跟NH3可以发生反应生成N2和H2O。现有NO和NH3的混合物1mol,充分反应后所得产物中,经还原得到的N2比经氧化得到的N2多1.4g。已知反应的化学方程式:4NH3+6NO 5N2+6H2O,则下列说法正确的是
5N2+6H2O,则下列说法正确的是
 5N2+6H2O,则下列说法正确的是
5N2+6H2O,则下列说法正确的是| A.当转移的电子数约为3.612×1023时,则标况下有4.48L氨气被还原 |
| B.氧化产物和还原产物的物质的量比为3:2 |
| C.若以上反应进行完全,原混合物中NO与NH3的物质的量之比为可能为3:7 |
| D.若有混合物中有0.2molNH3,则参与反应的NO为0.8mol |
您最近一年使用:0次
2021-06-21更新
|
1003次组卷
|
7卷引用:内蒙古鄂尔多斯市第一中学2020-2021学年高一下学期第一次月考化学试题
内蒙古鄂尔多斯市第一中学2020-2021学年高一下学期第一次月考化学试题(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)辽宁省沈阳市三十一中学2021-2022学年高一下学期4月月考化学试题(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)3.3.2 氮循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
7 . 某实验小组对化合物X(由3种短周期主族元素组成)开展探究实验。已知无色气体可使湿润的红色石蕊试纸变蓝,且标准状况下体积为6.72L。

请回答:
(1)白色固体Y的名称是______ ;X的化学式是______ 。
(2)红棕色气体转化为无色溶液A的化学方程式是______ 。
(3)将少量无色溶液B滴入无色溶液A时发生反应的离子方程式是______ 。

请回答:
(1)白色固体Y的名称是
(2)红棕色气体转化为无色溶液A的化学方程式是
(3)将少量无色溶液B滴入无色溶液A时发生反应的离子方程式是
您最近一年使用:0次
名校
解题方法
8 . SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:

①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式为:___________ 。
②反应器中NH3还原NO2的化学方程式为___________ 。
③当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成:___________ 。
(2)NSR(NOx储存还原)工作原理:


NOx的储存和还原在不同时段交替进行,如图a所示。
①通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存NOx的物质是___________ 。
②用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是___________ 。
(1)SCR(选择性催化还原)工作原理:

①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式为:
②反应器中NH3还原NO2的化学方程式为
③当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成:
(2)NSR(NOx储存还原)工作原理:


NOx的储存和还原在不同时段交替进行,如图a所示。
①通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存NOx的物质是
②用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是
您最近一年使用:0次
9 . 固体A含有3种元素(前20号元素),是已有100余年使用历史的化学肥料,某同学为了研究其化学组成和性质,设计并完成如下实验。B是碱性气体,F溶液是实验室检验D气体常用试剂。

(1)A的化学式为___________ 。
(2)B和O2反应生成G的化学方程式___________ 。
(3)M气体溶于水生成R强酸的化学方程式____________ 。
(4)A能改良酸性土壤,原因是__________________ 。

(1)A的化学式为
(2)B和O2反应生成G的化学方程式
(3)M气体溶于水生成R强酸的化学方程式
(4)A能改良酸性土壤,原因是
您最近一年使用:0次
解题方法
10 . 氮氧化物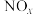 已经成为大气污染的主要污染源,其中NO的含量约占氮氧化物总含量的90%,目前选择性催化还原技术是脱除
已经成为大气污染的主要污染源,其中NO的含量约占氮氧化物总含量的90%,目前选择性催化还原技术是脱除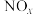 最普遍最有效的方法之一,请回答:
最普遍最有效的方法之一,请回答:
(1)实验室制取一氧化氮的化学方程式是_______ 。
(2)下列说法不正确的是_______ 。
A.上述反应的现象是铜片表面有无色气体产生,溶液由无色慢慢变蓝色
B.可通过排水法或排空气法收集一氧化氮
C.NO与 可与水反应,方程式为
可与水反应,方程式为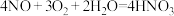 ,可用以制硝酸
,可用以制硝酸
D.工业上,氨在钯或铂催化下被氧气氧化成一氧化氮
(3)在一定温度下,利用CO为还原剂在催化剂作用下将NO脱除并转化为 和
和 ,主要的反应方程式如下:
,主要的反应方程式如下:
Ⅰ.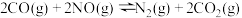
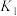
Ⅱ.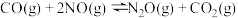
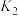
Ⅲ.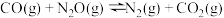

①如图是不同铈锆比例掺杂量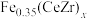 ,催化剂的催化性能结果。试分析脱除NO的最佳的催化剂样品和温度是
,催化剂的催化性能结果。试分析脱除NO的最佳的催化剂样品和温度是____ 。选择该催化剂样品的原因是____ 。


②CO、NO的起始物质的量均为1mol,反应在恒定温度和1L的密闭容器中进行,假设体系以反应Ⅰ和Ⅱ为主,达平衡时NO的转化率为80%, 的选择性为50%,则
的选择性为50%,则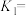
___ 。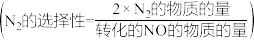
(4)已知NO可直接分解: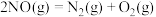 。常温常压下,该反应的平衡常数为
。常温常压下,该反应的平衡常数为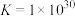 ,NO是可以分解的,但是实际上该反应是很难发生的,以碰撞理论说明原因:
,NO是可以分解的,但是实际上该反应是很难发生的,以碰撞理论说明原因:_______ 。
(5)工业上,在一定温度下,当 存在下用
存在下用 催化去除NO,会发生如下主反应:
催化去除NO,会发生如下主反应: ,
, 。下列说法不正确的是
。下列说法不正确的是_______ 。
A.通入适量 有利于主反应的发生
有利于主反应的发生
B. 量过多会限制脱除NO的活性
量过多会限制脱除NO的活性
C.当 通入过多会严重限制脱除NO的活性
通入过多会严重限制脱除NO的活性
D.气体组成中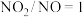 时,发生
时,发生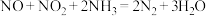
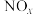 已经成为大气污染的主要污染源,其中NO的含量约占氮氧化物总含量的90%,目前选择性催化还原技术是脱除
已经成为大气污染的主要污染源,其中NO的含量约占氮氧化物总含量的90%,目前选择性催化还原技术是脱除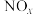 最普遍最有效的方法之一,请回答:
最普遍最有效的方法之一,请回答:(1)实验室制取一氧化氮的化学方程式是
(2)下列说法不正确的是
A.上述反应的现象是铜片表面有无色气体产生,溶液由无色慢慢变蓝色
B.可通过排水法或排空气法收集一氧化氮
C.NO与
 可与水反应,方程式为
可与水反应,方程式为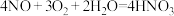 ,可用以制硝酸
,可用以制硝酸D.工业上,氨在钯或铂催化下被氧气氧化成一氧化氮
(3)在一定温度下,利用CO为还原剂在催化剂作用下将NO脱除并转化为
 和
和 ,主要的反应方程式如下:
,主要的反应方程式如下:Ⅰ.
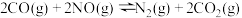
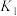
Ⅱ.
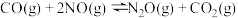
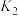
Ⅲ.
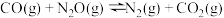

①如图是不同铈锆比例掺杂量
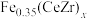 ,催化剂的催化性能结果。试分析脱除NO的最佳的催化剂样品和温度是
,催化剂的催化性能结果。试分析脱除NO的最佳的催化剂样品和温度是

②CO、NO的起始物质的量均为1mol,反应在恒定温度和1L的密闭容器中进行,假设体系以反应Ⅰ和Ⅱ为主,达平衡时NO的转化率为80%,
 的选择性为50%,则
的选择性为50%,则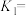
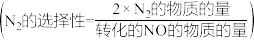
(4)已知NO可直接分解:
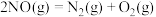 。常温常压下,该反应的平衡常数为
。常温常压下,该反应的平衡常数为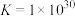 ,NO是可以分解的,但是实际上该反应是很难发生的,以碰撞理论说明原因:
,NO是可以分解的,但是实际上该反应是很难发生的,以碰撞理论说明原因:(5)工业上,在一定温度下,当
 存在下用
存在下用 催化去除NO,会发生如下主反应:
催化去除NO,会发生如下主反应: ,
, 。下列说法不正确的是
。下列说法不正确的是A.通入适量
 有利于主反应的发生
有利于主反应的发生B.
 量过多会限制脱除NO的活性
量过多会限制脱除NO的活性C.当
 通入过多会严重限制脱除NO的活性
通入过多会严重限制脱除NO的活性D.气体组成中
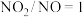 时,发生
时,发生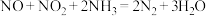
您最近一年使用:0次



