名校
解题方法
1 . 已知氮元素及其化合物的转化关系如下图所示,回答下列问题。
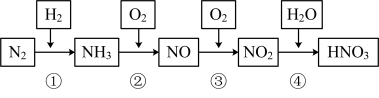
(1)①~ ④各步转化中,属于氮的固定的是_______ (填序号)。
(2)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。
①化学方程式是_______ 。
②干燥氨气不可选用的试剂是_______ (填字母)。
a.浓硫酸 b.NaOH固体 c.碱石灰
(3)工业上用氨气制备NO的化学方程式是_______ 。
(4)工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
①NaOH溶液吸收法。发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O,2NaOH+2NO2=NaNO3+NaNO2+H2O
②用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如下图:

(α表示尾气里NO、NO2中NO2的含量)
i.根据上图得知_______ (填字母)。
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.NO2含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是_______ 。
(5)电化学气敏传感器可用于监测环境中氨气的含量,其工作原理示意图如下:
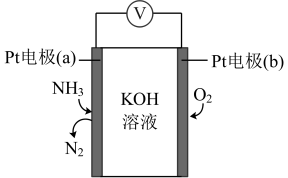
①负极的电极式为_______ 。
②反应消耗的NH3与O2的物质的量之比为_______ 。

(1)①~ ④各步转化中,属于氮的固定的是
(2)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。
①化学方程式是
②干燥氨气不可选用的试剂是
a.浓硫酸 b.NaOH固体 c.碱石灰
(3)工业上用氨气制备NO的化学方程式是
(4)工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
①NaOH溶液吸收法。发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O,2NaOH+2NO2=NaNO3+NaNO2+H2O
②用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如下图:

(α表示尾气里NO、NO2中NO2的含量)
i.根据上图得知
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.NO2含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是
(5)电化学气敏传感器可用于监测环境中氨气的含量,其工作原理示意图如下:

①负极的电极式为
②反应消耗的NH3与O2的物质的量之比为
您最近一年使用:0次
2022-11-02更新
|
339次组卷
|
2卷引用:黑龙江省佳木斯市第十二中学(佳木斯市建三江第一中学)2021-2022学年高一下学期期中考试化学试题
名校
2 . (一)实验室模拟合成氨和氨催化氧化的流程如下:
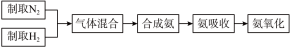
(1)N元素在周期表中位置_______________________ 。
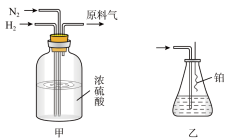
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合、干燥,还有______________ 作用。
(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热,锥形瓶中还可观察到的现象是_______________________________________ 。
(4)写出乙装置中氨氧化的化学方程式:__________________________________________ 。
(二)实验室探究铜与硝酸反应的相关问题,按下图所示装置进行实验。
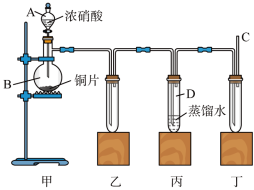
请回答下列问题:
(5)装置甲中盛放浓硝酸的仪器A的名称是_______________________ 。
(6)实验过程中,装置丙中出现的现象是:________________________________________ 。
(7)装置丙中的试管内发生反应的离子方程式为:__________________________________ 。
取下装置丙中的试管D,在其中滴加FeSO4溶液,再滴加KSCN溶液,溶液变为______________ 色。
(8)待反应停止后,Cu片有剩余,取下B,加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,离子方程式为________________________________________________________________ 。


(1)N元素在周期表中位置
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合、干燥,还有
(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热,锥形瓶中还可观察到的现象是
(4)写出乙装置中氨氧化的化学方程式:
(二)实验室探究铜与硝酸反应的相关问题,按下图所示装置进行实验。

请回答下列问题:
(5)装置甲中盛放浓硝酸的仪器A的名称是
(6)实验过程中,装置丙中出现的现象是:
(7)装置丙中的试管内发生反应的离子方程式为:
取下装置丙中的试管D,在其中滴加FeSO4溶液,再滴加KSCN溶液,溶液变为
(8)待反应停止后,Cu片有剩余,取下B,加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,离子方程式为
您最近一年使用:0次
名校
3 . 氨对人类的生产生活具有重要影响。
(1)氨的制备与利用。
① 工业合成氨的化学方程式是____________ 。
②氨催化氧化生成一氧化氮反应的化学方程式是___________ 。
(2)氨的定量检测。水体中氨气和铵根离子(统称氨氮)总量的检测备受关注。利用氨气传感器检测水体中氨氮含量的示意图如下:
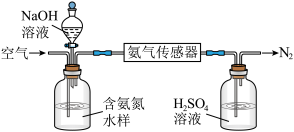
① 利用平衡原理分析含氨氮水样中加入NaOH溶液的作用:_______________ 。
② 若利用氨气传感器将1 L水样中的氨氮完全转化为N2时,转移电子的物质的量为6×10-4 mol,则水样中氨氮(以氨气计)含量为________ mg·L-1。
(3)氨的转化与去除。 微生物燃料电池(MFC)是一种现代化氨氮去除技术。下图为MFC碳氮联合同时去除的氮转化系统原理示意图。
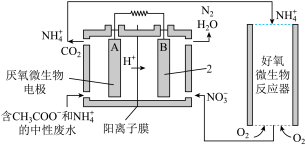
已知A、B两极生成CO2和N2的物质的量之比为5 : 2,写出A极的电极反应式:_______ 。
(1)氨的制备与利用。
① 工业合成氨的化学方程式是
②氨催化氧化生成一氧化氮反应的化学方程式是
(2)氨的定量检测。水体中氨气和铵根离子(统称氨氮)总量的检测备受关注。利用氨气传感器检测水体中氨氮含量的示意图如下:

① 利用平衡原理分析含氨氮水样中加入NaOH溶液的作用:
② 若利用氨气传感器将1 L水样中的氨氮完全转化为N2时,转移电子的物质的量为6×10-4 mol,则水样中氨氮(以氨气计)含量为
(3)氨的转化与去除。 微生物燃料电池(MFC)是一种现代化氨氮去除技术。下图为MFC碳氮联合同时去除的氮转化系统原理示意图。

已知A、B两极生成CO2和N2的物质的量之比为5 : 2,写出A极的电极反应式:
您最近一年使用:0次



