名校
解题方法
1 . 氮及其化合物的转化关系如下图所示,则下列说法不正确的是
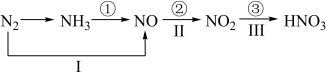
| A.路线①②③是工业生产硝酸的主要途径 | B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径 |
| C.上述所有反应都是氧化还原反应 | D.氮气可在足量的氧气中通过一步反应生成 |
您最近一年使用:0次
2024-03-12更新
|
1081次组卷
|
44卷引用:黑龙江省哈尔滨师范大学附属中学2021-2022学年高一下学期期中考试化学试题
黑龙江省哈尔滨师范大学附属中学2021-2022学年高一下学期期中考试化学试题山东省济宁市泗水县2020-2021学年高一下学期期中考试化学试题广东省珠海市第二中学2020-2021学年高一下学期期中考试化学试题河北保定市博野县实验中学2020-2021学年高一下学期期中考试化学试题黑龙江省宾县第二中学2020-2021学年高一下学期第二次月考化学试题江苏省镇江中学2020-2021学年高一下学期期中检测化学试题(已下线)【期中复习】必刷题-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)上海市晋元高级中学2021-2022学年高一下学期期中考试化学试题湖北省襄阳市第三中学2021-2022学年高一下学期期中考试化学试题黑龙江省哈尔滨市第十九中学2021-2022学年高三上学期第一次月考化学试题江苏省盐城市响水县清源高级中学2021-2022学年高一下学期期中考试化学试题广东省茂名市电白区2021-2022学年高一下学期期中(选择性)考试化学试题广东省顺德市李兆基中学2022-2023学年高一下学期4月期中考试化学试题浙江省余姚中学2022-2023学年高一下学期期中考试 (选考)化学试题广西钦州市浦北县2022-2023学年高一下学期4月期中考试化学试题(已下线)【浙江新东方】双师185高一下山西省怀仁市大地学校2020-2021学年高一下学期第三次月考化学试题吉林省长春市第二实验中学2020-2021学年高一下学期期末考试化学试题(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)河北省大名县第一中学2021-2022学年高二上学期开学考试化学试题江苏省常熟市2021-2022学年高二学生暑期自主学习调查化学试题(已下线)【期末复习】必刷题(1)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)上海市同济大学第一附属中学2021-2022学年高一下学期等级阶段性测试2化学试题(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)云南省普洱市第一中学2021-2022学年高一下学期3月份考试化学试题(已下线)第12讲 氮及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)安徽省亳州市第二中学2021-2022学年高一下学期期末考试化学试题河南省周口经济开发区黄泛区高级中学2021-2022学年高一下学期第一次月考化学试题宁夏银川外国语实验学校2023届高三上学期第二次月考化学试题(已下线)3.3.2 氮循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)广西百色民族高级中学2021-2022学年高二上学期9月月考化学试题河南省郑州市第七高级中学2022-2023 学年高一上学期期末考试化学试题(已下线)第四章 非金属及其化合物 第23练 硝酸 含氮化合物的转化关系广东省佛山市顺德区罗定邦中学2022-2023学年高一下学期3月第一次月考化学试题贵州省松桃民族中学2022-2023学年高一下学期3月月考化学试题(已下线)第6讲 硝酸 含氮化合物之间的转化陕西省安康市2023-2024学年高二上学期开学考化学试题陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题江苏省徐州市王杰中学2023-2024学年高一下学期第一次月考化学试题宁夏石嘴山市第三中学2023-2024学年高一下学期3月月考化学试题14 2024年苏州昆山柏庐高级中学高一3月月考广西南宁一中2023-2024学年高一下学期3月教学质量调研化学试卷福建省福州市闽侯县第一中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
2 . 如图是某常见非金属元素的价类二维图。下列说法正确的是
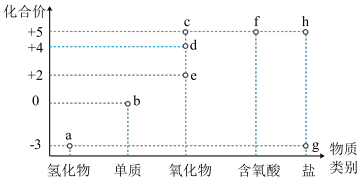

| A.c、d、e中,只有c、d是酸性氧化物 |
| B.一定条件下,a与氧气能一步反应生成d |
| C.g和h不可能是同一种物质 |
| D.一定条件下,a和e能反应生成b |
您最近一年使用:0次
3 . 下表各组物质之间通过一步反应不可以实现如下图所示转化关系的是
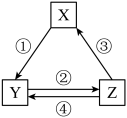

| 选项 | X | Y | Z | 对应过程的反应条件 |
| A | Fe | FeCl3 | FeCl2 | ①氯气,加热 |
| B | NaOH | NaHCO3 | Na2CO3 | ②加热 |
| C | CaO | Ca(OH)2 | CaCO3 | ①常温加水 |
| D | N2 | NO | NO2 | ③NH3、催化剂加热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 氨气催化氧化是高中化学教学中的一个重要实验,对于氨气性质和硝酸工业生产过程的教学有着非常重要的作用。某化学兴趣小组设计如下实验装置(部分装置省略)探究氨气的催化氧化。
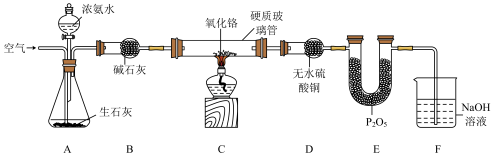
已知:氧化铬(Cr2O3)为催化剂;P2O5为酸性氧化物。
回答下列问题:
(1)在组装好装置,装入药品前,需要进行的操作是_______ ;氨气的电子式为_______ 。
(2)一段时间后无水硫酸铜变蓝,此时硬质玻璃管内氨气与氧气发生反应生成两种氧化物的化学方程式为_______ ,熄灭酒精灯,继续通入空气,此时可看到Cr2O3会持续红热,说明该反应为_______ (填“吸”或“放”)热反应。
(3)无水硫酸铜变蓝一段时间后,硬质玻璃管内会有红棕色气体产生。E装置的作用是_______ ;F装置用于吸收红棕色气体,吸收过程中生成等物质的量的两种可溶性盐,该反应的离子方程式为_______ ;若缺少F装置,排放的尾气可能造成的环境危害为_______ (填一种)。
(4)实验室也可以利用氯化铵和消石灰为原料制备氨气,该反应的化学方程式为_______ ,可以用_______ (填标号)检验有氨气生成。
a.无色酚酞溶液 b.湿润的蓝色石蕊试纸 c.浓盐酸 d.浓硫酸

已知:氧化铬(Cr2O3)为催化剂;P2O5为酸性氧化物。
回答下列问题:
(1)在组装好装置,装入药品前,需要进行的操作是
(2)一段时间后无水硫酸铜变蓝,此时硬质玻璃管内氨气与氧气发生反应生成两种氧化物的化学方程式为
(3)无水硫酸铜变蓝一段时间后,硬质玻璃管内会有红棕色气体产生。E装置的作用是
(4)实验室也可以利用氯化铵和消石灰为原料制备氨气,该反应的化学方程式为
a.无色酚酞溶液 b.湿润的蓝色石蕊试纸 c.浓盐酸 d.浓硫酸
您最近一年使用:0次
2023-08-31更新
|
242次组卷
|
2卷引用:黑龙江哈尔滨第三中学2024届高三上学期期中考试化学试题
名校
解题方法
5 . 下列化学方程式书写正确的是
A.工业制硫酸第二步为: |
B.粗硅的制备: |
C.氨的催化氧化为: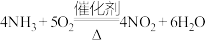 |
D.铜和浓硝酸: |
您最近一年使用:0次
6 . 氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意:
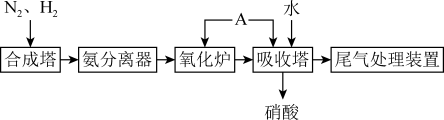
(1)合成塔中,反应开始进行时需要加热,加热的目的主要是_______ ;反应开始后停止加热,发现反应更加剧烈,由此可知该反应是_______ (填“放热”或“吸热”)反应。
(2)从合成气中分离出氨,主要利用了氨气_______ 的性质;从氨分离器中分离出的另两种气体可回到_______ (填写装置名称)中再利用。
(3)请写出氧化炉内发生反应的化学方程式_______ 。
(4)向吸收塔中通入过量A是_______ ,作用是_______ 。尾气处理装置中含有少量的NO2,可用氢氧化钠溶液吸收(已知该反应为歧化反应),该反应的化学方程式是_______ 。
(5)硝酸可氧化绝大多数金属,而工业上盛装大量浓硝酸可用铝制容器,原因是_______ 。
(6)①可利用浓氨水检验氯气管道是否泄漏,若泄漏,可观察到的现象,该反应方程式是_______ 。
②碳酸氢铵是一种常用氮肥,但因_______ (用化学方程式表达),所以必须放置阴凉处保存。

(1)合成塔中,反应开始进行时需要加热,加热的目的主要是
(2)从合成气中分离出氨,主要利用了氨气
(3)请写出氧化炉内发生反应的化学方程式
(4)向吸收塔中通入过量A是
(5)硝酸可氧化绝大多数金属,而工业上盛装大量浓硝酸可用铝制容器,原因是
(6)①可利用浓氨水检验氯气管道是否泄漏,若泄漏,可观察到的现象,该反应方程式是
②碳酸氢铵是一种常用氮肥,但因
您最近一年使用:0次
名校
解题方法
7 . 下列有关含氮化合物的实验装置和原理能达到相应实验目的的是
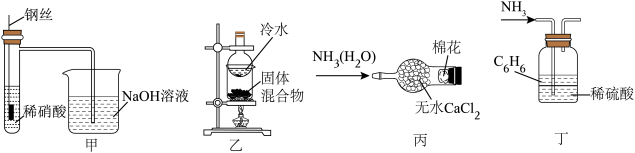

| A.实验室采用装置甲可证明NO能直接被NaOH溶液吸收 |
| B.用装置乙分离固体氯化钠和氯化铵 |
| C.用装置丙除去氨气中的H2O |
| D.用装置丁吸收氨气尾气,可有效防止倒吸 |
您最近一年使用:0次
2023-05-03更新
|
264次组卷
|
3卷引用:黑龙江省齐齐哈尔市2022-2023学年高一下学期4月期中考试化学试题
黑龙江省齐齐哈尔市2022-2023学年高一下学期4月期中考试化学试题广东省深圳市光明区高级中学、 深圳市光明书院2022-2023学年高一下学期4月期中联考化学试题(已下线)第17讲 氨的转化与生成-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)
解题方法
8 . 肼(N2H4)作为火箭发动机的燃料,可通过反应NaClO+2NH3=N2H4+NaCl+H2O制取。某化学兴趣小组尝试在实验室制取N2H4,设计了如图实验:
(1)制备NaClO溶液,装置如图所示。(已知:3Cl2+6NaOH 5NaCl+NaClO3+3H2O)
5NaCl+NaClO3+3H2O)
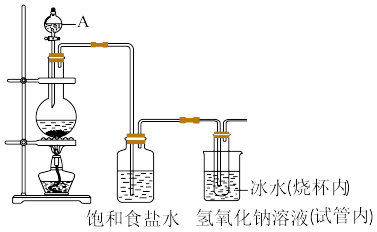
①仪器A的名称是_____ 。
②连接好装置,装药品之前,必须进行的一项操作是_____ 。
③圆底烧瓶内发生反应的化学方程式为_____ ;当生成71g氯气时,被氧化的HCl为_____ mol,试管内发生反应的离子方程式为______ 。
④饱和食盐水的作用是_____ ,冰水的作用是_____ 。
(2)将NaClO溶液倒入烧杯中,持续通入NH3制取N2H4。通常情况下,1体积水能溶解700体积的氨气,则图装置中漏斗的作用是_____ 。

(3)火箭发射时用N2H4作燃料,用N2O4助燃,燃烧生成两种可参与大气循环的物质,写出该反应的化学方程式_____ 。
(1)制备NaClO溶液,装置如图所示。(已知:3Cl2+6NaOH
 5NaCl+NaClO3+3H2O)
5NaCl+NaClO3+3H2O)
①仪器A的名称是
②连接好装置,装药品之前,必须进行的一项操作是
③圆底烧瓶内发生反应的化学方程式为
④饱和食盐水的作用是
(2)将NaClO溶液倒入烧杯中,持续通入NH3制取N2H4。通常情况下,1体积水能溶解700体积的氨气,则图装置中漏斗的作用是

(3)火箭发射时用N2H4作燃料,用N2O4助燃,燃烧生成两种可参与大气循环的物质,写出该反应的化学方程式
您最近一年使用:0次
9 . 部分含N及Cl物质的分类与相应化合价关系如图所示,下列推断不合理 的是
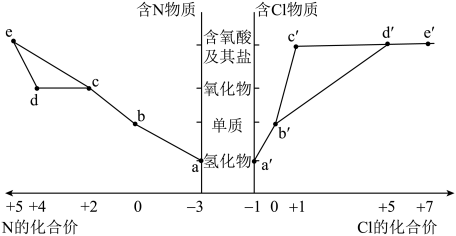

| A.工业上通过a→c→d→e来制备HNO3 |
| B.a→b的过程是氮的固定 |
| C.浓的a′溶液和浓的c′溶液反应可以得到b′ |
| D.加热d′的固态钾盐可以产生O2 |
您最近一年使用:0次
2022-11-25更新
|
97次组卷
|
2卷引用:黑龙江省绥化市第一中学2022-2023学年高三上学期期中考试化学试题
名校
解题方法
10 . 已知氮元素及其化合物的转化关系如下图所示,回答下列问题。
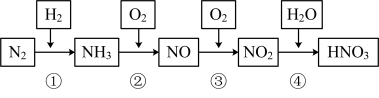
(1)①~ ④各步转化中,属于氮的固定的是_______ (填序号)。
(2)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。
①化学方程式是_______ 。
②干燥氨气不可选用的试剂是_______ (填字母)。
a.浓硫酸 b.NaOH固体 c.碱石灰
(3)工业上用氨气制备NO的化学方程式是_______ 。
(4)工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
①NaOH溶液吸收法。发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O,2NaOH+2NO2=NaNO3+NaNO2+H2O
②用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如下图:

(α表示尾气里NO、NO2中NO2的含量)
i.根据上图得知_______ (填字母)。
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.NO2含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是_______ 。
(5)电化学气敏传感器可用于监测环境中氨气的含量,其工作原理示意图如下:
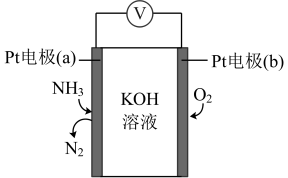
①负极的电极式为_______ 。
②反应消耗的NH3与O2的物质的量之比为_______ 。

(1)①~ ④各步转化中,属于氮的固定的是
(2)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。
①化学方程式是
②干燥氨气不可选用的试剂是
a.浓硫酸 b.NaOH固体 c.碱石灰
(3)工业上用氨气制备NO的化学方程式是
(4)工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
①NaOH溶液吸收法。发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O,2NaOH+2NO2=NaNO3+NaNO2+H2O
②用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如下图:

(α表示尾气里NO、NO2中NO2的含量)
i.根据上图得知
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.NO2含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是
(5)电化学气敏传感器可用于监测环境中氨气的含量,其工作原理示意图如下:

①负极的电极式为
②反应消耗的NH3与O2的物质的量之比为
您最近一年使用:0次
2022-11-02更新
|
336次组卷
|
2卷引用:黑龙江省佳木斯市第十二中学(佳木斯市建三江第一中学)2021-2022学年高一下学期期中考试化学试题



