名校
1 . 下列实验操作及现象与对应的结论不匹配的是
| 选项 | 操作及现象 | 结论 |
| A | 将Al粉加入强碱性的NaNO3溶液,加热,产生可使湿润的红色石蕊试纸变蓝的气体 |  在强碱性溶液具有氧化性 在强碱性溶液具有氧化性 |
| B | 将浓硫酸与NaCl(s)混合后加热,瓶口有“白雾”出现 | 挥发性:H2SO4<HCl |
| C | 向盛有浓氨水的锥形瓶中通入氧气,并将灼热的铂丝置于液面上方,铂丝保持红热,且瓶内有白烟产生 | NH3的催化氧化反应是吸热反应 |
| D | 向AlCl3溶液中逐滴加入NaOH溶液,先生成沉淀后沉淀溶解 | Al(OH)3为两性氢氧化物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 在给定条件下,下列物质间的转化均能实现的是
A.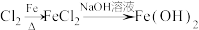 |
B.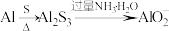 |
C. |
D. |
您最近一年使用:0次
名校
解题方法
3 . 某兴趣小组设计用铜粉将NO还原为 。
。
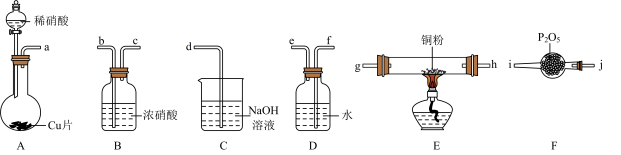
已知:①浓硝酸可氧化NO;②NaOH溶液能吸收 ,不能吸收NO。
,不能吸收NO。
(1)装置F的名称为___________ ,装置的连接顺序为a→___________ 。
(2)装置A中发生反应的离子方程式为___________ 。装置C中发生反应的离子方程式为___________ 。
(3)装置D的作用为___________ 。
(4)E装置中可观察到的现象为___________ 。
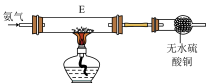
(5)反应一段时间后拆下E装置,连接为如下图装置,一段时间后无水硫酸铜变蓝色,写出通入氨气后E装置中发生反应的化学方程式:___________ ,该反应可证明氨气具有___________ 性。
 。
。
已知:①浓硝酸可氧化NO;②NaOH溶液能吸收
 ,不能吸收NO。
,不能吸收NO。(1)装置F的名称为
(2)装置A中发生反应的离子方程式为
(3)装置D的作用为
(4)E装置中可观察到的现象为
(5)反应一段时间后拆下E装置,连接为如下图装置,一段时间后无水硫酸铜变蓝色,写出通入氨气后E装置中发生反应的化学方程式:

您最近一年使用:0次
2023-10-26更新
|
679次组卷
|
6卷引用:重庆市百师联盟2024届高三一轮复习联考(二)
名校
解题方法
4 . Ⅰ.细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示。

(1)如图所示氮循环中,属于氮的固定的有_______ (填字母序号)。
A.N2转化为铵态氮 B. 硝化过程 C. 反硝化过程
(2)氮肥是水体中铵态氮的主要来源之一。
① 氨气是生产氮肥的主要原料,工业合成氨的化学方程式为_______ 。
② 检验铵态氮肥中NH 的实验方案是
的实验方案是 _______ 。
(3)硝化过程中,含氮物质发生_______ (填“氧化”或“还原”)反应。
(4)铵态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol 氮气时;转移的电子的物质的量为_______ mol。
Ⅱ.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:
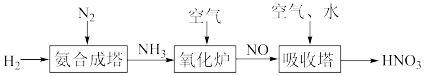
(5)写出氧化炉中发生的化学反应方程式:_______ 。
(6)实际上“吸收塔”尾部都会有含NO、NO₂等氨氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO₂的反应原理为:Na2CO3+2NO2═NaNO3+_______ +CO2(请完成化学方程式)。
②氨转化法。已知8mol氨恰好能将含NO 和NO2共7mol 的混合气体完全转化为N2,则混合气体中NO 和NO2的物质的量之比为_______ 。

(1)如图所示氮循环中,属于氮的固定的有
A.N2转化为铵态氮 B. 硝化过程 C. 反硝化过程
(2)氮肥是水体中铵态氮的主要来源之一。
① 氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
② 检验铵态氮肥中NH
 的实验方案是
的实验方案是 (3)硝化过程中,含氮物质发生
(4)铵态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol 氮气时;转移的电子的物质的量为
Ⅱ.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:

(5)写出氧化炉中发生的化学反应方程式:
(6)实际上“吸收塔”尾部都会有含NO、NO₂等氨氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO₂的反应原理为:Na2CO3+2NO2═NaNO3+
②氨转化法。已知8mol氨恰好能将含NO 和NO2共7mol 的混合气体完全转化为N2,则混合气体中NO 和NO2的物质的量之比为
您最近一年使用:0次
解题方法
5 .  和
和 是重要的工业产品,下图是合成氨和氨氧化制硝酸的工艺流程。
是重要的工业产品,下图是合成氨和氨氧化制硝酸的工艺流程。

(1)合成塔中发生反应的化学方程式是_______ 。
(2)氨分离器中压强约为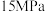 ,温度约为
,温度约为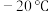 ,分离氨应用了氨
,分离氨应用了氨_______ 的性质,从氨分离器中又回到合成塔中的物质是_______ 。
(3)工业上制硝酸的关键一步便是 的催化氧化,可用下图装置模拟氧化炉中
的催化氧化,可用下图装置模拟氧化炉中 的催化氧化。玻璃管中发生
的催化氧化。玻璃管中发生 的催化氧化反应,化学反应方程式
的催化氧化反应,化学反应方程式_______ 。为保证在装置2中观察到红棕色气体,装置1应装入_______ (填试剂名称)。
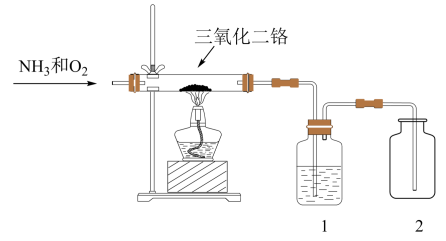
(4)氮元素在海洋中的循环,是整个海洋生态系统的基础和关键,海洋中无机氮的循环过程可用如图表示。海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是_______ (填图中数字序号)。
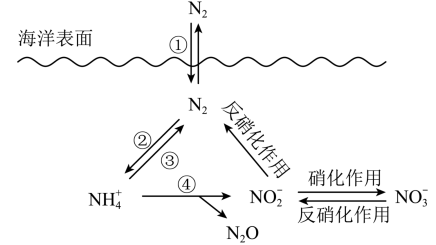
(5)有氧时,在硝化细菌作用下, 可实现过程④(如上图)的转化,将离子方程式补充完整:
可实现过程④(如上图)的转化,将离子方程式补充完整:_____  。
。
 和
和 是重要的工业产品,下图是合成氨和氨氧化制硝酸的工艺流程。
是重要的工业产品,下图是合成氨和氨氧化制硝酸的工艺流程。
(1)合成塔中发生反应的化学方程式是
(2)氨分离器中压强约为
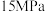 ,温度约为
,温度约为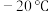 ,分离氨应用了氨
,分离氨应用了氨(3)工业上制硝酸的关键一步便是
 的催化氧化,可用下图装置模拟氧化炉中
的催化氧化,可用下图装置模拟氧化炉中 的催化氧化。玻璃管中发生
的催化氧化。玻璃管中发生 的催化氧化反应,化学反应方程式
的催化氧化反应,化学反应方程式
(4)氮元素在海洋中的循环,是整个海洋生态系统的基础和关键,海洋中无机氮的循环过程可用如图表示。海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是

(5)有氧时,在硝化细菌作用下,
 可实现过程④(如上图)的转化,将离子方程式补充完整:
可实现过程④(如上图)的转化,将离子方程式补充完整: 。
。
您最近一年使用:0次
6 . 部分含N与含Cl物质类别与相应化合价关系如图。下列推断不合理的是


| A.c可由化合反应生成 |
| B.工业上制备HNO3的途径为a →b→c→d→e |
| C.工业上可用a的浓溶液来检验b'是否泄漏 |
| D.一定条件下,向c'或d'中加入a'的浓溶液均能产生b' |
您最近一年使用:0次
2023-02-10更新
|
860次组卷
|
4卷引用:重庆市长寿中学校2022-2023学年高一下学期4月期中考试化学试题
名校
解题方法
7 . 下列关系图中,A 是一种正盐,B 是气态氢化物,C 是单质,F 是强酸。当 X 无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当 X 是强碱时,过量的 B 跟 Cl2 反应除生成 C 外,另一产物是盐酸盐。
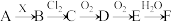
下列说法中不正确的是
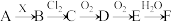
下列说法中不正确的是
| A.当 X 是强酸时,A、B、C、D、E、F 中均含同一种元素,F 可能是 H2SO4 |
| B.当 X 是强碱时,A、B、C、D、E、F 中均含同一种元素,F 是 HNO3 |
| C.用 O2 代替 Cl2, 也能与 B 反应生成 C 物质 |
| D.当 X 是强酸时,C 在常温下是一种易溶于酒精的固体 |
您最近一年使用:0次
2022-12-20更新
|
759次组卷
|
6卷引用:重庆市凤鸣山中学教育集团2021-2022学年高三上学期期中考试化学试题
名校
解题方法
8 . Ⅰ.氮及其化合物在生产生活中应用广泛,工业上制硝酸的关键一步便是 的催化氧化,可用下图装置模拟
的催化氧化,可用下图装置模拟 的催化氧化,回答下列问题:
的催化氧化,回答下列问题:
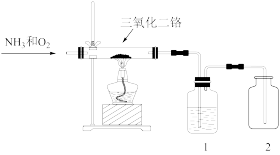
(1)玻璃管中发生反应的化学方程式是_______ ,停止加热后玻璃管内仍能保持红热,该反应是_______ 反应(填“吸热”或“放热”)。
(2)为保证在装置2中观察到红棕色气体,装置1应装入_______ ,作用是_______ 。
Ⅱ.氮元素在海洋中的循环,是整个海洋生态系统的基础和关键,海洋中无机氮的循环过程可用下图表示。

(3)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是_______ (填图中数字序号)。
(4)下列关于海洋氮循环的说法正确的是_______ (填字母序号)。
a.海洋中的氮循环起始于氮的氧化
b.海洋中存在游离态的氮
c.向海洋排放含 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量
d.海洋中的反硝化作用一定有氧气的参与
(5)有氧时,在硝化细菌作用下, 可实现过程④的转化,写出④的离子方程式并用单线桥标电子转移情况:
可实现过程④的转化,写出④的离子方程式并用单线桥标电子转移情况:_______ 。
 的催化氧化,可用下图装置模拟
的催化氧化,可用下图装置模拟 的催化氧化,回答下列问题:
的催化氧化,回答下列问题:
(1)玻璃管中发生反应的化学方程式是
(2)为保证在装置2中观察到红棕色气体,装置1应装入
Ⅱ.氮元素在海洋中的循环,是整个海洋生态系统的基础和关键,海洋中无机氮的循环过程可用下图表示。

(3)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
(4)下列关于海洋氮循环的说法正确的是
a.海洋中的氮循环起始于氮的氧化
b.海洋中存在游离态的氮
c.向海洋排放含
 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量d.海洋中的反硝化作用一定有氧气的参与
(5)有氧时,在硝化细菌作用下,
 可实现过程④的转化,写出④的离子方程式并用单线桥标电子转移情况:
可实现过程④的转化,写出④的离子方程式并用单线桥标电子转移情况:
您最近一年使用:0次
2022-05-07更新
|
212次组卷
|
2卷引用:重庆市渝高中学校2021-2022学年高一下学期期中考试化学试题
名校
9 . 以下物质间的每步转化不能都通过一步反应实现的是
A. | B. |
C. | D. |
您最近一年使用:0次
名校
10 . 氮在自然界中的转化是一个复杂的过程,氮循环是生态系统物质循环的重要组成部分。
(1)在一定条件下,NH3可用于脱除氮氧化物的烟气,其反应原理为4xNH3+6NOx (2x+3)N2+6xH2O。该反应中的还原剂为
(2x+3)N2+6xH2O。该反应中的还原剂为____ (填化学式)。
(2)氨的催化氧化是制备硝酸的重要过程,实验室按如图所示装置进行氨的催化氧化实验。

实验操作:将浓氨水倒入锥形瓶中,从导气管通入热空气,将红热的铂丝伸入锥形瓶中。
实验现象:a.红热的铂丝始终保持红热状态;b.瓶中有红棕色气体生成,瓶内还有白烟生成。回答下列问题:
①铂丝始终保持红热状态的可能原因是____ 。
②通入热空气的作用是____ 。
③请写出氨气的催化氧化反应的化学方程式:____ 。
④红棕色气体的化学式为____ ,此气体可用NaOH溶液吸收,有NaNO2和NaNO3生成,写出该反应的离子方程式:____ 。
(3)氨是氮循环中的重要物质,在人类的生产和生活中有着广泛的应用。高浓度的氨氮废水是造成河流及湖泊富营养化的主要因素,研究表明在微生物作用下,可实现NH →NO
→NO 的转化。写出在碱性条件下,NH
的转化。写出在碱性条件下,NH 被氧气氧化为NO
被氧气氧化为NO 的反应的离子方程式:
的反应的离子方程式:____ 。每生成1molNO ,转移的电子的物质的量为
,转移的电子的物质的量为____ mol。再往含NO 的废水中加入甲醇,可将NO
的废水中加入甲醇,可将NO 转化为N2,实现废水的无害化处理。
转化为N2,实现废水的无害化处理。
(1)在一定条件下,NH3可用于脱除氮氧化物的烟气,其反应原理为4xNH3+6NOx
 (2x+3)N2+6xH2O。该反应中的还原剂为
(2x+3)N2+6xH2O。该反应中的还原剂为(2)氨的催化氧化是制备硝酸的重要过程,实验室按如图所示装置进行氨的催化氧化实验。

实验操作:将浓氨水倒入锥形瓶中,从导气管通入热空气,将红热的铂丝伸入锥形瓶中。
实验现象:a.红热的铂丝始终保持红热状态;b.瓶中有红棕色气体生成,瓶内还有白烟生成。回答下列问题:
①铂丝始终保持红热状态的可能原因是
②通入热空气的作用是
③请写出氨气的催化氧化反应的化学方程式:
④红棕色气体的化学式为
(3)氨是氮循环中的重要物质,在人类的生产和生活中有着广泛的应用。高浓度的氨氮废水是造成河流及湖泊富营养化的主要因素,研究表明在微生物作用下,可实现NH
 →NO
→NO 的转化。写出在碱性条件下,NH
的转化。写出在碱性条件下,NH 被氧气氧化为NO
被氧气氧化为NO 的反应的离子方程式:
的反应的离子方程式: ,转移的电子的物质的量为
,转移的电子的物质的量为 的废水中加入甲醇,可将NO
的废水中加入甲醇,可将NO 转化为N2,实现废水的无害化处理。
转化为N2,实现废水的无害化处理。
您最近一年使用:0次
2022-03-23更新
|
222次组卷
|
3卷引用:重庆市好教育联盟2021-2022学年高一下学期期中考试化学试题



