名校
1 . 氮、硫元素的“价—类”二维图如图所示。下列有关叙述错误的是
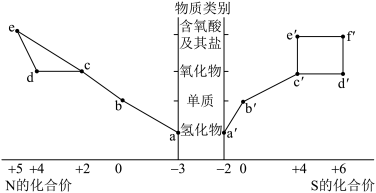
| A.b→a属于氮的固定 |
B.工业上制备 的途径为b'→c'→d'→f 的途径为b'→c'→d'→f |
| C.d或d'均可与水发生反应,生成强酸 |
| D.a'和f的浓溶液反应,产物一定有b'和c' |
您最近半年使用:0次
名校
2 . 如图所示是短周期某种非金属元素的“价-类”二维图。下列推断不正确的是
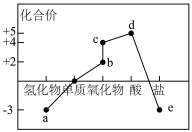
| A.a与d反应产物中有离子键 | B.可存在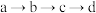 的转化 的转化 |
| C.常温下,d的浓溶液不能与铁发生反应 | D.可用与强碱的反应来检验e中的阳离子 |
您最近半年使用:0次
2024-04-25更新
|
545次组卷
|
3卷引用:福建省福州延安中学2023-2024学年高一下学期4月期中考试化学试题
名校
3 . 铬及其化合物在催化、金属防腐等方面具有重要应用。催化剂Cr2O3可由(NH4)2Cr2O7加热分解制备,反应同时生成无污染气体。
(1)完成化学方程式:_____ 。
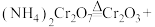 _____+_____。
_____+_____。
(2)Cr2O3催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为
过程的焓变为_____ (列式表示)。_____ (用“→”表示含氮物质间的转化);其中一个有颜色变化的反应的化学方程式为_____ 。
(1)完成化学方程式:
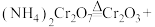 _____+_____。
_____+_____。(2)Cr2O3催化丙烷脱氢过程中,部分反应历程如图,
 过程的焓变为
过程的焓变为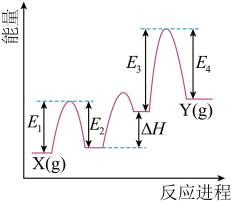
您最近半年使用:0次
4 . 自然界中的氮循环部分过程如图所示,回答下列问题:_______ (任写一种)。
②在哈伯等科学家的努力下,路径Ⅱ已实现工业大规模合成氨,反应方程式为_______ 。
(2)实验室的硝酸一般储存在棕色瓶中,涉及的化学方程式为_______ 。
(3)除反硝化作用外,铵态氮( )与亚硝态氮(
)与亚硝态氮( )也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式
)也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式_______ 。该反应中,当产生0.02mol氮气时,转移电子的物质的量为_______ 。
为探究氨的还原性,某同学设计了如图所示实验装置(其中夹持装置略去),在实验室中进行实验探究。回答下列问题
A中氧化铜全部转化成光亮的红色固体
B中U形管内物质变蓝;
(4)C中集气瓶内收集到一种无色气态单质,该气体用排水法收集的理由是_______ 。
(5)从C中水槽里取适量液体于试管内,向试管里滴入无色酚酞试液,溶液呈_______ 色,原因是_______ 。
(6)氧化铜和氨气发生反应,化学方程式是_______ 。
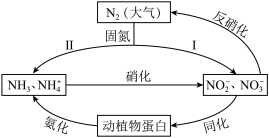
②在哈伯等科学家的努力下,路径Ⅱ已实现工业大规模合成氨,反应方程式为
(2)实验室的硝酸一般储存在棕色瓶中,涉及的化学方程式为
(3)除反硝化作用外,铵态氮(
 )与亚硝态氮(
)与亚硝态氮( )也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式
)也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式为探究氨的还原性,某同学设计了如图所示实验装置(其中夹持装置略去),在实验室中进行实验探究。回答下列问题
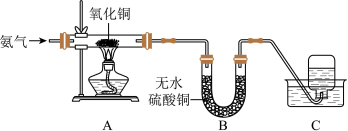
A中氧化铜全部转化成光亮的红色固体
B中U形管内物质变蓝;
(4)C中集气瓶内收集到一种无色气态单质,该气体用排水法收集的理由是
(5)从C中水槽里取适量液体于试管内,向试管里滴入无色酚酞试液,溶液呈
(6)氧化铜和氨气发生反应,化学方程式是
您最近半年使用:0次
名校
5 . 某研究性学习小组设计用如图所示实验装置(夹持仪器省略),制取干燥的NH3并验证NH3的性质。
(1)实验室用装置甲制备NH3的化学方程式为___________ 。
(2)装置乙的作用是___________ ,若装置丙用于收集NH3,应将导管___________ (填“a”或“b”)延长至集气瓶底部。
(3)装置戊所用仪器的名称为___________ 。
(4)观察到丁中红色Fe2O3粉末变黑,戊中无水硫酸铜变蓝,同时收集到一种无色无味的气体,取反应后的黑色粉末加入稀盐酸,产生气泡,证明NH3具有___________ 性,写出NH3和Fe2O3反应的化学方程式___________ 。
(5)为防止环境污染,可用以下装量(盛放的液体均为水)吸收多余NH3的是___________ (填标号)。
a.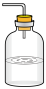 b.
b. c.
c.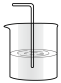 d.
d.

(1)实验室用装置甲制备NH3的化学方程式为
(2)装置乙的作用是
(3)装置戊所用仪器的名称为
(4)观察到丁中红色Fe2O3粉末变黑,戊中无水硫酸铜变蓝,同时收集到一种无色无味的气体,取反应后的黑色粉末加入稀盐酸,产生气泡,证明NH3具有
(5)为防止环境污染,可用以下装量(盛放的液体均为水)吸收多余NH3的是
a.
 b.
b. c.
c. d.
d.
您最近半年使用:0次
2023-07-11更新
|
224次组卷
|
2卷引用:福建省莆田第二十五中学2023-2024学年高一下学期期中考试化学试题
名校
6 . 氮的化合物在工业生产中有广泛的用途。
Ⅰ.实验室利用如图装置模拟工业生产制备少量硝酸。

(1)写出实验室用氯化铵和消石灰制备氨气的化学方程式___________ 。
(2)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃。下列图示能够正确表示该反应过程中能量变化的是___________ (填序号)

(3)控制氨气和氧气的比例是制备硝酸的关键。当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟,白烟的化学式是___________ 。
(4)取上述制得的硝酸100mL与9.6g铜反应,硝酸的还原产物为NO,反应后溶液中含有0.1mol ,则硝酸的物质的量浓度为
,则硝酸的物质的量浓度为___________ mol/L。
Ⅱ.已知:
①室温下,
②酸性条件下,NO或 都能与
都能与 反应生成
反应生成 和
和 。
。
现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示:
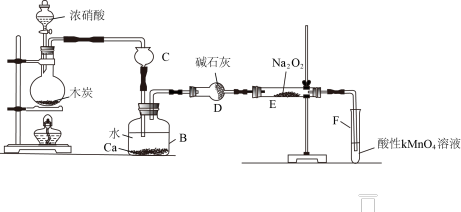
(5)装浓硝酸的仪器名称为___________ 。
(6)B中Cu参与反应的离子方程式为___________ 。
(7)装置C的作用是___________ 。
(8)若无装置D,则E中产物除亚硝酸钠外,还有副产物___________ (填化学式)。
Ⅰ.实验室利用如图装置模拟工业生产制备少量硝酸。

(1)写出实验室用氯化铵和消石灰制备氨气的化学方程式
(2)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到700℃。下列图示能够正确表示该反应过程中能量变化的是

(3)控制氨气和氧气的比例是制备硝酸的关键。当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟,白烟的化学式是
(4)取上述制得的硝酸100mL与9.6g铜反应,硝酸的还原产物为NO,反应后溶液中含有0.1mol
 ,则硝酸的物质的量浓度为
,则硝酸的物质的量浓度为Ⅱ.已知:
①室温下,

②酸性条件下,NO或
 都能与
都能与 反应生成
反应生成 和
和 。
。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示:

(5)装浓硝酸的仪器名称为
(6)B中Cu参与反应的离子方程式为
(7)装置C的作用是
(8)若无装置D,则E中产物除亚硝酸钠外,还有副产物
您最近半年使用:0次
7 . X、Y、Z、W均为两种元素组成的常见化合物,Y为淡黄色固体,W为常见液体,甲为单质,乙为红棕色气体,上述物质之间的转化关系如图所示(部分生成物已省略),则下列说法中不正确的是
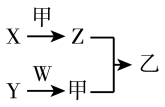

| A.沸点:W>X | B.Y中只含有离子键 |
| C.Z中混有乙可用水洗涤再干燥除去 | D.生成乙的方程式为: |
您最近半年使用:0次
名校
解题方法
8 . I.下图是某元素及其重要化合物之间的相互转化关系图(生成物中不含该元素的物质均已略去)。其中A是单质,D在常温下呈气态,F可用作氮肥。
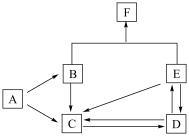
据此,请回答下列问题:
(1)写出以下物质的化学式:A_______ ,D_______ ,F_______ 。
(2)写出下列变化的化学方程式:
BC_______
EC_______
II.氢燃料电池车是北京冬奥会期间的交通服务用车,酸性氢氧燃料电池的构造如图所示。
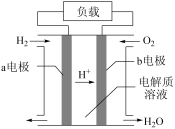
(3)若该电池中的电解质溶液是稀硫酸溶液,则a电极上发生反应的电极反应式为_______ 。
(4)b电极是该电池的_______ 极(填“正”或“负”),从氧化还原反应的角度分析,该电极发生的反应属于_______ 反应。
(5)当转移0.2mol电子时,需要消耗标况下的氢气体积是_______ L。

据此,请回答下列问题:
(1)写出以下物质的化学式:A
(2)写出下列变化的化学方程式:
BC
EC
II.氢燃料电池车是北京冬奥会期间的交通服务用车,酸性氢氧燃料电池的构造如图所示。

(3)若该电池中的电解质溶液是稀硫酸溶液,则a电极上发生反应的电极反应式为
(4)b电极是该电池的
(5)当转移0.2mol电子时,需要消耗标况下的氢气体积是
您最近半年使用:0次
9 . 实验室制取氨气、收集、验证其还原性并进行尾气处理的装置和原理能达到实验目的的是
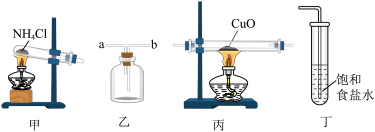

| A.用装置甲制取氨气 |
| B.用装置乙收集氨气时气体应该从a口进b口出 |
| C.装置丙中黑色固体变成红色时氧化产物为铜 |
| D.可以用装置丁吸收氨气,进行尾气处理 |
您最近半年使用:0次
2023-05-06更新
|
330次组卷
|
2卷引用:福建省福州第八中学2022-2023学年高一下学期期中考试化学试题
10 . 某研究性学习小组利用以下装置探究氯气和氨气之间的反应情况。其中A、F分别为氨气和氯气的制取发生装置,C为纯净干燥的氯气与干燥的氨气发生反应的装置。请回答下列问题:
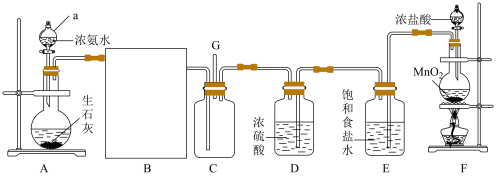
(1)仪器a的名称是___________ 。
(2)用装置F制取氯气的化学方程式为___________ 。
(3)请为B处框内选择合适的装置及相应的试剂___________(选填字母)。
(4)装置E的作用是___________ ,装置D和E的位置___________ (选填“能”或“不能”)调换。
(5)实验中可观察到装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出此反应的化学方程式:___________ ,若有1mol 被氧化,则转移的电子数目为
被氧化,则转移的电子数目为___________ 。

(1)仪器a的名称是
(2)用装置F制取氯气的化学方程式为
(3)请为B处框内选择合适的装置及相应的试剂___________(选填字母)。
| A.球形干燥管装碱石灰 | B.洗气瓶装浓硫酸 |
| C.球形干燥管装氧化钙 | D.球形干燥管装 |
(5)实验中可观察到装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出此反应的化学方程式:
 被氧化,则转移的电子数目为
被氧化,则转移的电子数目为
您最近半年使用:0次
2023-05-05更新
|
416次组卷
|
3卷引用:福建省南平市高级中学2022-2023学年高一下学期期中考试化学试题



