1 . 对下列事实的解释错误的是
| A.浓硝酸在光照下颜色变黄,说明浓硝酸的不稳定性 |
| B.常温下,铝制品可盛放浓硝酸,说明浓硝酸与铝不反应 |
| C.蓝色石蕊试纸上滴入浓硝酸,试纸先变红再褪色,说明浓硝酸有酸性和强氧化性 |
| D.从氨气喷泉实验可知氨气易溶于水且其水溶液显碱性 |
您最近一年使用:0次
2 . 某同学在实验室中设计两个关于NO的探究实验。
Ⅰ.工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,探究NO和NH3能否反应。
(1)氨气的制备
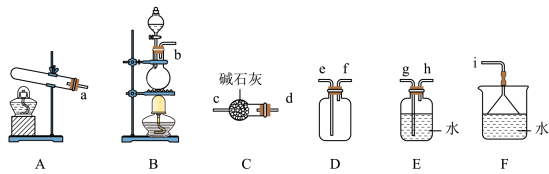
氨气的发生装置可以选择上图中的___________ 装置(填字母),实验室制备氨气反应的化学方程式为___________ 。
(2)将上述收集到的NH3加入少量催化剂,充入NO充分混合,冷却到室温,观察到管中有少量水珠,说明NO和NH3能反应,则氧化剂和还原剂的物质的量之比为___________ 。
Ⅱ.探究NO能否被Na2O2完全吸收,设计了如下实验。装置如图(加热装置省略):
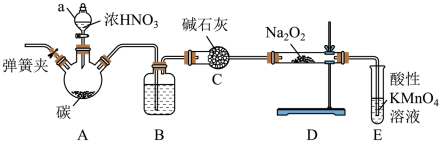
查阅资料知:①2NO+Na2O2=2NaNO2;
②酸性条件下,NO或NO2都能与KMnO4溶液反应生成 。回答下列问题:
。回答下列问题:
(3)装有碱石灰的仪器名称:___________ 。
(4)B瓶内装的物质是___________ 。
(5)若NO能被Na2O2完全吸收,E装置中的现象为___________ 。
(6)三颈烧瓶A中反应的化学方程式为___________ 。
(7)C装置的作用是___________ 。
Ⅰ.工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,探究NO和NH3能否反应。
(1)氨气的制备

氨气的发生装置可以选择上图中的
(2)将上述收集到的NH3加入少量催化剂,充入NO充分混合,冷却到室温,观察到管中有少量水珠,说明NO和NH3能反应,则氧化剂和还原剂的物质的量之比为
Ⅱ.探究NO能否被Na2O2完全吸收,设计了如下实验。装置如图(加热装置省略):

查阅资料知:①2NO+Na2O2=2NaNO2;
②酸性条件下,NO或NO2都能与KMnO4溶液反应生成
 。回答下列问题:
。回答下列问题:(3)装有碱石灰的仪器名称:
(4)B瓶内装的物质是
(5)若NO能被Na2O2完全吸收,E装置中的现象为
(6)三颈烧瓶A中反应的化学方程式为
(7)C装置的作用是
您最近一年使用:0次
解题方法
3 . 某校化学实验小组,为验证氯单质的氧化性强于硫和氮气,设计了一套实验装置:(部分夹持装置已略去)

(1)写出A中反应的离子方程式_________ 。
(2)实验中证明氧化性Cl2>S的实验现象为___________ 。
(3)D干燥管中产生大量白烟,该反应的化学方程式为____________________ 。
(4)有同学认为从C排出的Cl2可能含有某杂质气体,影响D中现象的判断,该杂质气体是__________ ,若除去该杂质气体可以用___________ 溶液。
(5)E装置中反应的化学方程式为_______________________ 。

(1)写出A中反应的离子方程式
(2)实验中证明氧化性Cl2>S的实验现象为
(3)D干燥管中产生大量白烟,该反应的化学方程式为
(4)有同学认为从C排出的Cl2可能含有某杂质气体,影响D中现象的判断,该杂质气体是
(5)E装置中反应的化学方程式为
您最近一年使用:0次
12-13高二上·广西桂林·期中
4 . 实验室中可用如图装置来制取干燥的氨气。


C D
(1)写出A处发生反应的化学方程式_____________________________________ 。
(2)U形管B中所放的药品是__________________ 。
(3)实验室制取下列气体时,与实验室制取氨气的气体发生装置相同的是______________ (填字母)。
A. 氢气 B.氧气C.氯气 D.二氧化碳
(4)试管C的管口处要放置一小团棉花,放置棉花的作用是___________________________ 。
(5)资料显示:“氨气可在纯氧中点燃,反应生成氮气和水”。为验证此事实,某同学设计了一个实验方案,装置见D。请写出该反应的化学方程式__________________________ 。


C D
(1)写出A处发生反应的化学方程式
(2)U形管B中所放的药品是
(3)实验室制取下列气体时,与实验室制取氨气的气体发生装置相同的是
A. 氢气 B.氧气C.氯气 D.二氧化碳
(4)试管C的管口处要放置一小团棉花,放置棉花的作用是
(5)资料显示:“氨气可在纯氧中点燃,反应生成氮气和水”。为验证此事实,某同学设计了一个实验方案,装置见D。请写出该反应的化学方程式
您最近一年使用:0次
2016-12-09更新
|
692次组卷
|
3卷引用:贵州省剑河县二中2018-2019学年高一上学期期末考试化学试题
贵州省剑河县二中2018-2019学年高一上学期期末考试化学试题(已下线)2012-2013学年广西桂林中学高二上学期期中考试文科化学试卷黑龙江省黑河市五校2021-2022学年高一下学期期末联考化学试题
5 . 某化学实验小组同学利用如图所示装置制备氨气,并探究氨气的性质(部分仪器已略去)。请回答:

I.实验室制备氨
(1)实验室制备氨气的化学方程式为_______ ;干燥氨气常用的干燥剂是__________ 。
(2)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是______ 。
II.探究NH3的还原性。用氨气和如图所示仪器设计实验。

(3)①NH3与Na2O2反应不会生成NO、NO2的现象是__________ 。
②检验产物是否有H2O等,按气流从左至右,仪器连接顺序为__________ 。
(4)G装置的作用是____________ 。
(5)实验完毕后,D装置中收集到一定量气体;将E中得到的固体加入少量酚酞试液中,观察到溶液变红;F装置中无水CuSO4不变蓝,据此写出E中反应的化学方程式:______ 。

I.实验室制备氨
(1)实验室制备氨气的化学方程式为
(2)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是
II.探究NH3的还原性。用氨气和如图所示仪器设计实验。

(3)①NH3与Na2O2反应不会生成NO、NO2的现象是
②检验产物是否有H2O等,按气流从左至右,仪器连接顺序为
(4)G装置的作用是
(5)实验完毕后,D装置中收集到一定量气体;将E中得到的固体加入少量酚酞试液中,观察到溶液变红;F装置中无水CuSO4不变蓝,据此写出E中反应的化学方程式:
您最近一年使用:0次
2020-03-27更新
|
203次组卷
|
2卷引用:贵州省贵阳市第一中学2020届高三第五次月考理综化学试题
名校
6 . 如图所示装置能达到实验目的的是

| A.用图甲装置探究浓硫酸的吸水性 |
B.用图乙装置制备、干燥并收集 |
C.用图丙装置验证氧化性: |
| D.用图丁装置制备乙炔 |
您最近一年使用:0次
7日内更新
|
139次组卷
|
2卷引用:2024届贵州省贵阳市第一中学高三下学期三模化学试题
名校
解题方法
7 . 利用下列实验装置进行实验,操作正确且能达到实验目的的是
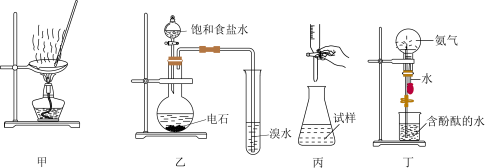

A.装置甲:蒸干 溶液制无水 溶液制无水 |
| B.装置乙:证明乙炔可使溴水褪色 |
C.装置丙:用酸性高锰酸钾溶液滴定 溶液 溶液 |
| D.装置丁:验证氨气易溶于水且其水溶液呈碱性 |
您最近一年使用:0次
2024-02-27更新
|
213次组卷
|
2卷引用:贵州省黔东南苗族侗族自治州黔东南州九校联考2023-2024学年高三下学期开学化学试题
8 . 据装置和下表内的物质(省略夹持、净化以及尾气处理装置,图1中虚线框内的装置是图2),其中能达到相应实验目的的是
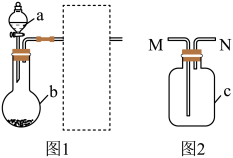

| 选项 | a中的物质 | b中的物质 | 实验目的、试剂和操作 | ||
| 实验目的 | c中的物质 | 进气口 | |||
| A | 浓硝酸 | Al | 收集贮存NO2 | 空气 | M |
| B | 浓硫酸 | Na2SO3 | 检验SO2的氧化性 | Na2S溶液 | M |
| C | 浓氨水 | 碱石灰 | 收集贮存氨气 | 饱和NH4Cl溶液 | N |
| D | 浓盐酸 | MnO2 | 检验Cl2的氧化性 | Na2S溶液 | M |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 已知氨气极易溶解于水;在加热条件下氨气可与灼热的氧化铜反应,产物为氮气、水和金属铜。用如图的装置可以实现该反应(加持装置已略去)。

回答下列问题:
(1)写出氨气的实验室制法的化学方程式_______ 。
(2)B中加入的物质的名称是_______ ,其作用是_______ 。
(3)实验时在C中观察到的现象是_______ ,发生反应的化学方程式是_______ 。
(4)实验结束后在D中收集到的物质为_______ (填“酸性”、“中性”,“碱性”),E中收集到气体的电子式为_______ 。

回答下列问题:
(1)写出氨气的实验室制法的化学方程式
(2)B中加入的物质的名称是
(3)实验时在C中观察到的现象是
(4)实验结束后在D中收集到的物质为
您最近一年使用:0次
2022-10-05更新
|
89次组卷
|
2卷引用:贵州省黔东南州从江县第一民族中学2021-2022学年高一下学期第二次月考化学试题
名校
10 . 按要求回答问题:
(1)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为__________ ;漂白粉的有效成分是____________ (填化学式)。
(2)氨气( )在工农业中应用广泛。氯化铵是常用氮肥,工厂将氨气和氯化氢混合制氯化铵的化学方程式为
)在工农业中应用广泛。氯化铵是常用氮肥,工厂将氨气和氯化氢混合制氯化铵的化学方程式为_____________________ ;实验室制取氨气选用________________ (填试剂名称)来干燥氨气。
(3)图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。硫酸具有A-D所示的性质,以下过程主要表现了浓硫酸的那些性质?请将选项字母填在下列各小题的括号内:

A强酸性 B吸水性 C 脱水性 D 强氧化性
①浓硫酸可以干燥氢气____________
②浓硫酸使木条变黑____________
③热的浓硫酸与铜片反应____________
(1)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
(2)氨气(
 )在工农业中应用广泛。氯化铵是常用氮肥,工厂将氨气和氯化氢混合制氯化铵的化学方程式为
)在工农业中应用广泛。氯化铵是常用氮肥,工厂将氨气和氯化氢混合制氯化铵的化学方程式为(3)图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。硫酸具有A-D所示的性质,以下过程主要表现了浓硫酸的那些性质?请将选项字母填在下列各小题的括号内:

A强酸性 B吸水性 C 脱水性 D 强氧化性
①浓硫酸可以干燥氢气
②浓硫酸使木条变黑
③热的浓硫酸与铜片反应
您最近一年使用:0次



