名校
解题方法
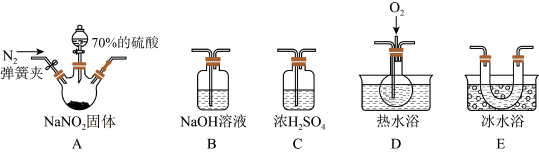
1 . 亚硝酸钠(NaNO2)在纤维纺织品的染色和漂白、照相、生产橡胶、制药等领域有广泛应用,也常用于鱼类、肉类等食品的染色和防腐。但因其有毒,所以在食品行业中的用量有严格限制。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。
已知:①NO+NO2+2OH-=2 +H2O;
+H2O;
②气体液化的温度:NO2为21℃,NO为-152℃。___________ 、___________ 、B。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是___________ 。
(3)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是___________ ;
②装置E的作用是___________ 。
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为___________ 。
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是___________ 。
已知:①NO+NO2+2OH-=2
 +H2O;
+H2O;②气体液化的温度:NO2为21℃,NO为-152℃。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是
(3)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是
②装置E的作用是
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是
您最近一年使用:0次
2023-05-11更新
|
803次组卷
|
6卷引用:广西南宁市第八中学2023-2024学年高二上学期开学考化学试题
广西南宁市第八中学2023-2024学年高二上学期开学考化学试题广西柳州铁一中学2023-2024学年高一上学期期末考试化学试卷 陕西省西安市第一中学2022-2023学年高一下学期5月月考化学试题江西省宜春市上高中学2022-2023学年高一下学期7月期末考试化学试题湖南师大附中博才实验中学2022-2023年高一下学期期末考试化学试题(已下线)重难点02 常见物质的制取与性质探究-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)
解题方法
2 . 下列实验操作对应的现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将铜片放入盛有稀硝酸的试管中 | 试管口出现红棕色气体 | 铜片与稀硝酸反应产生NO2 |
| B | 向盛有无色透明溶液的试管中滴加澄清石灰水 | 生成白色沉淀 | 溶液中一定存在 |
| C | 向盛有少量蔗糖的烧杯中加入几滴水,再加入适量浓硫酸,搅拌 | 蔗糖变黑,体积膨胀,产生有刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
| D | 加热盛有NH4Cl固体的试管 | 试管底部固体消失,试管口有晶体凝结 | NH4C1固体可以升华 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 有氧条件下,NO在催化剂作用下可被NH3还原为N2,反应机理如图。下列说法错误的是


| A.V5+=O在反应中起到催化剂的作用 |
| B.该转化过程中NO和O2均体现出了氧化性 |
| C.该转化过程中,若O2过量更有利于NO转化为N2 |
D.该转化过程的总反应为4NH3+4NO+O2 4N2+6H2O 4N2+6H2O |
您最近一年使用:0次
2022-04-24更新
|
543次组卷
|
4卷引用:广西玉林市博白县中学2023-2024学年高三上学期开学考试化学试题
解题方法
4 . 回答下列问题:
(1)X、Y、Z三种主族元素的单质在常温下都是常见的无色气体,在适当条件下,三者之间可以两两发生反应生成分别是双核、三核和四核的甲、乙、丙三种分子,且乙、丙分子中含有X元素的原子个数比为2∶3.请回答下列问题:
①元素X的名称是___________ ,丙分子的电子式为___________ 。
②若甲与Y单质在常温下混合就有明显现象,则甲的化学式为___________ 。丙在一定条件下转化为甲和乙的反应方程式为___________ 。
③化合物丁含X、Y、Z三种元素,丁是一种常见的强酸,将丁与丙按物质的量之比1∶1混合后所得物质戊的晶体结构中含有的化学键为___________ (选填序号)。
a.只含共价键 b.只含离子键 c.既含离子键,又含共价键
(2)已知反应A(g)+B(g) C(g)+D(g)。回答下列问题:
C(g)+D(g)。回答下列问题:
①830 ℃时,向一个5 L的密闭容器中充入0.20 mol的A和0.80 mol的B,若反应初始6 s内A的平均反应速率v(A)=0.003 mol·L-1·s-1,则6 s时c(A)=___________ mol·L-1,C的物质的量为___________ mol。
②判断该反应是否达到平衡的依据为___________ (填字母)。
A.压强不随时间改变 B.气体的密度不随时间改变 C.c(A)不随时间改变 D.单位时间里生成C和D的物质的量相等
(1)X、Y、Z三种主族元素的单质在常温下都是常见的无色气体,在适当条件下,三者之间可以两两发生反应生成分别是双核、三核和四核的甲、乙、丙三种分子,且乙、丙分子中含有X元素的原子个数比为2∶3.请回答下列问题:
①元素X的名称是
②若甲与Y单质在常温下混合就有明显现象,则甲的化学式为
③化合物丁含X、Y、Z三种元素,丁是一种常见的强酸,将丁与丙按物质的量之比1∶1混合后所得物质戊的晶体结构中含有的化学键为
a.只含共价键 b.只含离子键 c.既含离子键,又含共价键
(2)已知反应A(g)+B(g)
 C(g)+D(g)。回答下列问题:
C(g)+D(g)。回答下列问题:①830 ℃时,向一个5 L的密闭容器中充入0.20 mol的A和0.80 mol的B,若反应初始6 s内A的平均反应速率v(A)=0.003 mol·L-1·s-1,则6 s时c(A)=
②判断该反应是否达到平衡的依据为
A.压强不随时间改变 B.气体的密度不随时间改变 C.c(A)不随时间改变 D.单位时间里生成C和D的物质的量相等
您最近一年使用:0次
5 . 某亚硝酸钠生产厂采用硝酸为原料,其生产原理是NO+NO2+2NaOH===2NaNO2+H2O。工艺流程如下

(1)分解塔中填有大量的瓷环,其目的是:_____________________________ 。
(2)按一定计量比在反应塔中通SO2和喷入硝酸,若反应后生成的NO与NO2物质的量之比恰好1∶1,则分解塔中发生反应的化学方程式为:____________________________ 。试从产物产率的角度分析该反应中硝酸的浓度不宜过大或过小的原因是_____________________________________ ,若硝酸浓度过高,吸收塔中可能发生的副反应化学方程式为_____________________________________________ 。
(3)通入一定量的N2的目的是:___________________________________ 。
(4)吸收塔中尾气如何再利用:_______________________________________ 。

(1)分解塔中填有大量的瓷环,其目的是:
(2)按一定计量比在反应塔中通SO2和喷入硝酸,若反应后生成的NO与NO2物质的量之比恰好1∶1,则分解塔中发生反应的化学方程式为:
(3)通入一定量的N2的目的是:
(4)吸收塔中尾气如何再利用:
您最近一年使用:0次



