解题方法
1 . 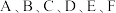 是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐
是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐 与
与 同主族,且与
同主族,且与 同周期;
同周期; 元素的最外层电子数是其次外层电子数的
元素的最外层电子数是其次外层电子数的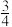 倍,
倍,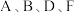 这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物.
这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物. 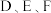 三种元素对应的最高价氧化物的水化物间两两皆能反应. 请回答下列问题:
三种元素对应的最高价氧化物的水化物间两两皆能反应. 请回答下列问题:
(1)写出题中 所代表的元素名称
所代表的元素名称_________ ,指出 所代表的元素在周期表中的位置
所代表的元素在周期表中的位置_________________________ 。
(2)写出 两种元素形成的原子个数比为
两种元素形成的原子个数比为 的物质的电子式为
的物质的电子式为_________________ , 两种元素各自形成的简单离子大小为
两种元素各自形成的简单离子大小为_________________ 
_________________ (写出相应离子符号)
(3)可以验证 和
和 两种元素非金属性强弱的结论是(填编号)
两种元素非金属性强弱的结论是(填编号)_____________ 。
①比较这两种元素常见单质的熔点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
(4)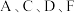 四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为
四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为_____________ 、_____________ ,这两种酸式盐相互反应的离子方程式为___________________ 。
(5) 间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为________________________________ 。
(6)写出 的单质和D的最高价氧化物的水化物间反应化学方程式:
的单质和D的最高价氧化物的水化物间反应化学方程式:_____________________ 。
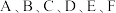 是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐
是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐 与
与 同主族,且与
同主族,且与 同周期;
同周期; 元素的最外层电子数是其次外层电子数的
元素的最外层电子数是其次外层电子数的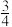 倍,
倍,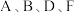 这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物.
这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物. 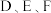 三种元素对应的最高价氧化物的水化物间两两皆能反应. 请回答下列问题:
三种元素对应的最高价氧化物的水化物间两两皆能反应. 请回答下列问题:(1)写出题中
 所代表的元素名称
所代表的元素名称 所代表的元素在周期表中的位置
所代表的元素在周期表中的位置(2)写出
 两种元素形成的原子个数比为
两种元素形成的原子个数比为 的物质的电子式为
的物质的电子式为 两种元素各自形成的简单离子大小为
两种元素各自形成的简单离子大小为
(3)可以验证
 和
和 两种元素非金属性强弱的结论是(填编号)
两种元素非金属性强弱的结论是(填编号)①比较这两种元素常见单质的熔点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
(4)
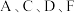 四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为
四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为(5)
 间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为(6)写出
 的单质和D的最高价氧化物的水化物间反应化学方程式:
的单质和D的最高价氧化物的水化物间反应化学方程式:
您最近一年使用:0次
名校
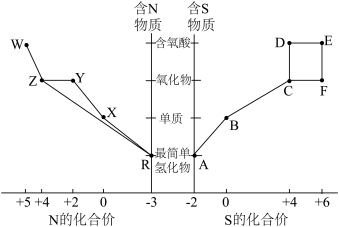
2 . 元素的“价类二维图”体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。回答下列问题: 反应的化学方程式
反应的化学方程式______
(2)下列有关图中所示含N、S物质的叙述,正确的是______ (填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠( ),从氧化还原反应的角度分析,可选择B和D反应
),从氧化还原反应的角度分析,可选择B和D反应
(3)写出B与氢氧化钠溶液反应的离子反应方程式______
(4)将物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是______ 。
(5) (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: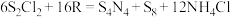 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有______ ,该反应每生成 转移电子
转移电子______ mol。
 反应的化学方程式
反应的化学方程式(2)下列有关图中所示含N、S物质的叙述,正确的是
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(
 ),从氧化还原反应的角度分析,可选择B和D反应
),从氧化还原反应的角度分析,可选择B和D反应(3)写出B与氢氧化钠溶液反应的离子反应方程式
(4)将物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是
(5)
 (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: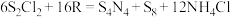 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有 转移电子
转移电子
您最近一年使用:0次
名校
3 . 部分含硫物质的类别与相应化合价及部分物质间转化关系如图。下列说法错误的是
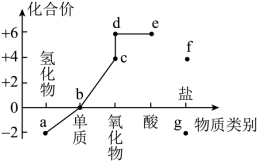
| A.c可以使滴有酚酞的NaOH溶液褪色,适量c可做食品添加剂 |
| B.b附着在试管壁上可以用热的浓NaOH溶液洗涤 |
| C.a在O2中燃烧可以生成d |
| D.e的浓溶液长时间暴露在空气中,质量增大,质量分数减小 |
您最近一年使用:0次
2024-04-17更新
|
278次组卷
|
2卷引用:广东省肇庆市四会中学、广州市广信中学2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
4 . 含硫物质的价类二维图及部分物质间转化关系如图,下列说法错误的是
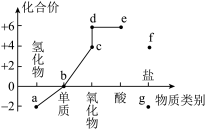
| A.工业制硫酸时将d通入水中得到浓硫酸 |
| B.b附着在试管壁上可以用热的浓NaOH溶液洗涤 |
| C.c可以使滴有酚酞的NaOH溶液褪色,适量c可做食品添加剂 |
| D.e的浓溶液长时间暴露在空气中,质量增大,质量分数减小 |
您最近一年使用:0次
名校
解题方法
5 . 为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分,请回答以下问题:
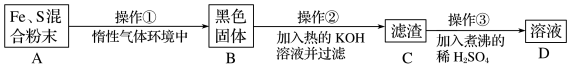
(1)混合粉末A中硫粉过量的原因是________ 。
(2)操作①使用烧热的玻璃棒点触混合粉末,反应即可持续进行,说明________ 。
(3)操作②的化学方程式是_______ ;为了实现操作②的目的,也可改用加入_______ 。
(4)操作③稀 煮沸的目的是
煮沸的目的是________ 。

(1)混合粉末A中硫粉过量的原因是
(2)操作①使用烧热的玻璃棒点触混合粉末,反应即可持续进行,说明
(3)操作②的化学方程式是
(4)操作③稀
 煮沸的目的是
煮沸的目的是
您最近一年使用:0次
名校
解题方法
6 . 洗涤附着在试管内壁上的硫黄,可选用的洗涤试剂是
| A.水 | B.酒精 | C.热的NaOH溶液 | D.饱和食盐水 |
您最近一年使用:0次
2024-02-11更新
|
1111次组卷
|
6卷引用:江苏省南京师范大学附属中学2023-2024学年高一上学期1月期末化学试题
江苏省南京师范大学附属中学2023-2024学年高一上学期1月期末化学试题(已下线)5.1.1硫和二氧化硫课后作业巩固篇(已下线)专题01 硫及其化合物(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)广西壮族自治区贵百河联考2023-2024学年高一下学期4月月考化学试题5.1.1硫和二氧化硫 课堂例题云南省大理白族自治州民族中学2023-2024学年高一下学期4月月考化学试题
名校
7 . 下列实验不能达到目的的是
| A.洗去试管壁残留的硫,可用热的NaOH溶液,再用水洗 |
| B.洗去试管壁残留的二氧化锰,可用热的浓盐酸,再用水洗 |
| C.洗去试管壁残留的碘,可用酒精,再用水洗 |
| D.电解熔融的MgCl2,加入CaCl2固体可减低MgCl2固体的熔点,节约能源 |
您最近一年使用:0次
名校
解题方法
8 . 下列化学活动所对应化学原理叙述错误的是
| 选项 | 化学活动 | 化学原理 |
| A | 将石墨电极放入 溶液中,连接小灯泡,接通电源后小灯泡变亮 溶液中,连接小灯泡,接通电源后小灯泡变亮 |  是电解质 是电解质 |
| B | 用酵母菌发酵面粉 | 催化剂可以加快反应速率 |
| C | 将铁钉分别放在有水和无水环境中观察较长时间 | 钢铁在有水存在的条件下更容易生锈 |
| D | 附着S的试管用热的烧碱溶液清洗 | 硫在碱性溶液中溶解度大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 为了证明铁与硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:
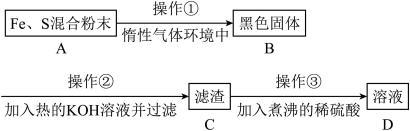
请回答以下提出的问题:
(1)混合粉末A中硫粉过量的原因是_______ 。
(2)反应在“惰性气体环境”中进行的原因是_______ 。
(3)操作①是用烧热的玻璃棒点触混合粉末,反应即可持续进行,说明_______ 。
(4)操作②的作用是_______ ,反应的化学方程式是_______ ,也可改用_______ 。
(5)操作③稀硫酸煮沸的目的是_______ 。

请回答以下提出的问题:
(1)混合粉末A中硫粉过量的原因是
(2)反应在“惰性气体环境”中进行的原因是
(3)操作①是用烧热的玻璃棒点触混合粉末,反应即可持续进行,说明
(4)操作②的作用是
(5)操作③稀硫酸煮沸的目的是
您最近一年使用:0次
名校
解题方法
10 . 元素X、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知:Y原子最外层电子数是次外层的3倍;M原子的最外层电子数与次外层电子数之比为3∶4; 、
、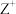 、
、 的离子半径逐渐减小;化合物XR常温下为气体。下列说法正确的是
的离子半径逐渐减小;化合物XR常温下为气体。下列说法正确的是
 、
、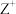 、
、 的离子半径逐渐减小;化合物XR常温下为气体。下列说法正确的是
的离子半径逐渐减小;化合物XR常温下为气体。下列说法正确的是| A.X与Y可形成10电子分子和18电子分子,且18电子分子可转化成10电子分子 |
| B.由R的非金属性强于M,可推出R的含氧酸的酸性强于M |
| C.一定条件下,R和M的单质都能与NaOH溶液反应 |
| D.在X、Y、R按原子个数之比1∶1∶1形成的化合物中,最外层均达到8电子稳定结构 |
您最近一年使用:0次
2023-04-27更新
|
312次组卷
|
3卷引用:山东省德州市2022-2023学年高一下学期4月期中考试化学试题



