名校
1 . 含SO2废气的治理可以变废为宝,使硫资源得以利用。
(1)将SO2通入以下溶液,均会发生颜色变化,其中体现SO2还原性的是_______(填字母)。
(2)“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如图所示:_______ 。
②为证明亚硫酸钠粗品含有少量Na2SO4,设计如下方案:在一支试管中加入少量亚硫酸钠粗品,用适量蒸馏水溶解,_______ 。
(3)目前NaClO溶液广泛应用于脱硫脱硝。
①某课外小组同学设计了如图喷淋吸收塔装置(如图),其中,脱硝(NO)反应的离子方程式为_______ 。_______ 。_______ 。
(1)将SO2通入以下溶液,均会发生颜色变化,其中体现SO2还原性的是_______(填字母)。
| A.使品红溶液褪色 | B.使滴有酚酞的氢氧化钠溶液褪色 |
| C.使溴水褪色 | D.使氢硫酸溶液中出现淡黄色浑浊 |
(2)“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如图所示:
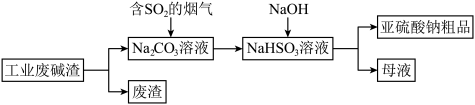
②为证明亚硫酸钠粗品含有少量Na2SO4,设计如下方案:在一支试管中加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
(3)目前NaClO溶液广泛应用于脱硫脱硝。
①某课外小组同学设计了如图喷淋吸收塔装置(如图),其中,脱硝(NO)反应的离子方程式为
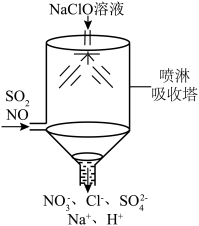
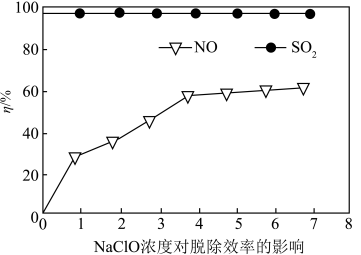
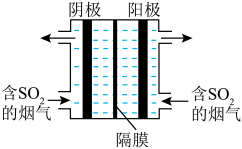
您最近一年使用:0次
名校
2 . 下列有关推理中得到的结论与事实不相符合的是
A.Cu可以还原 得到 得到 ,所以Fe也可以还原 ,所以Fe也可以还原 生成 生成 |
B.常温条件下,Cu与浓硝酸剧烈反应放出 气体,所以Fe和浓硝酸反应将更加剧烈 气体,所以Fe和浓硝酸反应将更加剧烈 |
C. 与NaOH溶液反应生成碳酸盐, 与NaOH溶液反应生成碳酸盐, 也与NaOH溶液反应生成亚硫酸盐 也与NaOH溶液反应生成亚硫酸盐 |
| D.亚硫酸的酸性强于碳酸,所以硫酸的酸性也强于碳酸 |
您最近一年使用:0次
名校
解题方法
3 . 将浓硫酸滴加到盛有 溶液的试管中,不仅可以观察到溶液中有S沉淀产生,而且在试管内壁的上方也有S单质附着。下列有关此实验的分析不正确的是
溶液的试管中,不仅可以观察到溶液中有S沉淀产生,而且在试管内壁的上方也有S单质附着。下列有关此实验的分析不正确的是
 溶液的试管中,不仅可以观察到溶液中有S沉淀产生,而且在试管内壁的上方也有S单质附着。下列有关此实验的分析不正确的是
溶液的试管中,不仅可以观察到溶液中有S沉淀产生,而且在试管内壁的上方也有S单质附着。下列有关此实验的分析不正确的是| A.试管中溶液的温度会升高 |
B.试管的溶液中产生的S沉淀应该是 的氧化产物 的氧化产物 |
C.试管内壁上方出现S的沉淀,说明浓硫酸的还原产物中应该有 |
| D.据此反应现象说明浓硫酸只具有强氧化性 |
您最近一年使用:0次
名校
4 . 室温下,下列实验探究方案能够边到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 将 溴丁烷与 溴丁烷与 的乙醇溶液混合后加热,生成的气体通入 的乙醇溶液混合后加热,生成的气体通入 的 的 溶液中,观察现象 溶液中,观察现象 |  溴丁烷能否发生消去反应生成烯烃 溴丁烷能否发生消去反应生成烯烃 |
| B | 将 气体通入紫色石蕊溶液中,观察溶液颜色变化 气体通入紫色石蕊溶液中,观察溶液颜色变化 |  是否具有漂白性 是否具有漂白性 |
| C | 向饱和 溶液中通入足量 溶液中通入足量 气体,观察现象 气体,观察现象 | 比较 与 与 在水中溶解度的大小 在水中溶解度的大小 |
| D | 向 溶液中滴加淀粉,再通入 溶液中滴加淀粉,再通入 气体,观察现象 气体,观察现象 | 比较 与 与 氧化性的强弱 氧化性的强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-01更新
|
774次组卷
|
3卷引用:江苏省泰州市靖江高级中学2023-2024学年高二下学期4月期中考试化学试题
5 . 某化学兴趣小组拟探究碳与浓 反应,并检验气体产物。下列说法正确的是
反应,并检验气体产物。下列说法正确的是
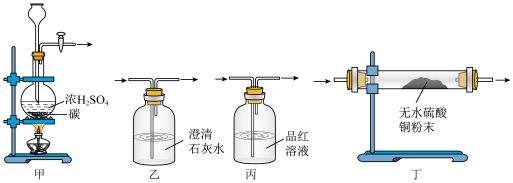
 反应,并检验气体产物。下列说法正确的是
反应,并检验气体产物。下列说法正确的是
A.用装置甲进行碳与浓 反应 反应 |
B.将检验过 后的气体再通入装置丁中检验产物 后的气体再通入装置丁中检验产物 |
C.将反应产生的气体通入装置丙,可直接检验产物 |
D.将反应产生的气体通入装置乙,可直接检验产物 |
您最近一年使用:0次
解题方法
6 . 按要求回答问题
Ⅰ.分类法是进行化学研究的重要方法。不同的标准可以把事物分为不同的类别。
现有以下物质:①固体NaHCO3 ② ③CaCO3 ④Fe(OH)3胶体 ⑤熔融的NaHSO4 ⑥干冰 ⑦稀盐酸 ⑧蔗糖
③CaCO3 ④Fe(OH)3胶体 ⑤熔融的NaHSO4 ⑥干冰 ⑦稀盐酸 ⑧蔗糖
(1)以上物质中属于混合物的是_______ (填序号);
(2)写出①在水溶液中的电离方程式_______ ;
(3)④的实验室制备方案:向沸水中滴加几滴_______ 溶液,加热至液体呈红褐色,停止加热。
Ⅱ.空气与我们的生活息息相关。 是主要的大气污染物之一,
是主要的大气污染物之一, 是主要的温室气体。双碱法脱硫过程如图所示。
是主要的温室气体。双碱法脱硫过程如图所示。

(4)SO2属于_______ (填“酸性”或“碱性”)氧化物。过程Ⅰ发生的离子方程式是_______ 。
(5)下列反应中,能用同一离子方程式表示的是_______(填序号)。
(6)用化学方程式表示过程Ⅱ发生的化学反应_______ 。
Ⅰ.分类法是进行化学研究的重要方法。不同的标准可以把事物分为不同的类别。
现有以下物质:①固体NaHCO3 ②
 ③CaCO3 ④Fe(OH)3胶体 ⑤熔融的NaHSO4 ⑥干冰 ⑦稀盐酸 ⑧蔗糖
③CaCO3 ④Fe(OH)3胶体 ⑤熔融的NaHSO4 ⑥干冰 ⑦稀盐酸 ⑧蔗糖(1)以上物质中属于混合物的是
(2)写出①在水溶液中的电离方程式
(3)④的实验室制备方案:向沸水中滴加几滴
Ⅱ.空气与我们的生活息息相关。
 是主要的大气污染物之一,
是主要的大气污染物之一, 是主要的温室气体。双碱法脱硫过程如图所示。
是主要的温室气体。双碱法脱硫过程如图所示。
(4)SO2属于
(5)下列反应中,能用同一离子方程式表示的是_______(填序号)。
A. 和稀 和稀 | B. 和稀 和稀 |
C. 与稀 与稀 | D. 与稀 与稀 |
(6)用化学方程式表示过程Ⅱ发生的化学反应
您最近一年使用:0次
解题方法
7 . 室温下,下列实验探究方案能达到探究目的的是
| 选项 | 实验探究方案 | 探究的目的 |
| A | 向 和 和 的混合溶液中滴入稀硫酸 的混合溶液中滴入稀硫酸 | 氧化性: |
| B |  通入酸性 通入酸性 溶液中 溶液中 |  具有漂白性 具有漂白性 |
| C | 向试管中加入2mL5% 和1mL2% 和1mL2% 溶液,观察气泡产生情况 溶液,观察气泡产生情况 |  可促进 可促进 分解 分解 |
| D | 向新制氯水中加入 固体 固体 | 氯水呈酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-15更新
|
264次组卷
|
2卷引用:江苏省南京市东山高级中学三校联考2023-2024学年高三上学期期中调研化学试题
名校
解题方法
8 . 二氧化硫在食品工业中可用作漂白剂、防腐剂、抗氧化剂等。某研究小组利用如图所示装置制备并检验SO2的部分性质。下列说法正确的是

A.装置甲中反应时 的硫酸表现出氧化性 的硫酸表现出氧化性 |
| B.装置乙中溶液颜色变化:先变红后褪色 |
C.装置丙中发生的最终总反应为 |
D.装置丁中酸性 溶液褪色的原理与 溶液褪色的原理与 用于食品漂白剂的原理相同 用于食品漂白剂的原理相同 |
您最近一年使用:0次
2023-10-06更新
|
1042次组卷
|
7卷引用:江苏省淮安市高中校协作体2023-2024学年高三上学期期中联考化学试题
名校
解题方法
9 .  是大气主要污染物之一,它的去除有多种方法,如碱液吸收法、电化学处理法等。
是大气主要污染物之一,它的去除有多种方法,如碱液吸收法、电化学处理法等。 在生产生活中具有广泛应用,如可生产
在生产生活中具有广泛应用,如可生产 并进而制得硫酸等,其反应原理为:
并进而制得硫酸等,其反应原理为: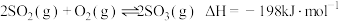 。在一定温度下,体积不变的容器中加入
。在一定温度下,体积不变的容器中加入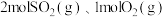 ,发生反应
,发生反应 ,下列说法正确的是
,下列说法正确的是
 是大气主要污染物之一,它的去除有多种方法,如碱液吸收法、电化学处理法等。
是大气主要污染物之一,它的去除有多种方法,如碱液吸收法、电化学处理法等。 在生产生活中具有广泛应用,如可生产
在生产生活中具有广泛应用,如可生产 并进而制得硫酸等,其反应原理为:
并进而制得硫酸等,其反应原理为: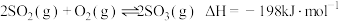 。在一定温度下,体积不变的容器中加入
。在一定温度下,体积不变的容器中加入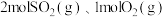 ,发生反应
,发生反应 ,下列说法正确的是
,下列说法正确的是
A.加入 不会影响反应速率 不会影响反应速率 | B.充分反应后,会放出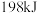 的热量 的热量 |
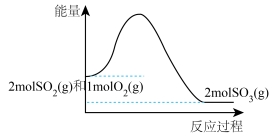
| C.该反应过程中的能量变化如图所示 | D.一段时间后,容器中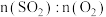 可能为 可能为 |
您最近一年使用:0次
解题方法
10 . 根据下列实验操作和现象判断结论正确的是
| 实验 | 实验操作和现象 |
| 1 | 向溶液中滴加盐酸酸化的BaCl2溶液产生白色沉淀 |
| 2 | 用洁净铂丝蘸取某溶液在火焰上灼烧,透过钴玻璃观察火焰呈紫色 |
| 3 | 在KI淀粉溶液中滴入氯水变蓝,通入SO2至蓝色褪去 |
| 4 | 向等浓度NaCl、NaI的混合液中滴加AgNO3溶液,有黄色沉淀生成 |
A.实验1溶液中一定有SO | B.实验2溶液中不可能含有Na+ |
| C.实验3说明SO2具有漂白性 | D.实验4说明Ksp(AgCl)>Ksp(AgI) |
您最近一年使用:0次



