名校
解题方法
1 . 环境保护是化学的重要任务,氮氧化物和硫氧化物是造成大气污染的主要原因之一,请完成下列问题。
(1)采用“联合脱硫脱氮技术”处理烟气(含 、
、 、NO)可获得含
、NO)可获得含 、
、 、
、 的副产品,工业流程如图所示。
的副产品,工业流程如图所示。___________ 。 转化为
转化为 反应的化学方程式为
反应的化学方程式为___________ 。
(2)烟气中的NO可在催化剂作用下用 还原。
还原。
①已知7mol氨气恰好能将含NO和 共6mol的混合气体完全转化为
共6mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比
的物质的量之比___________ 。
②其它条件相同,以一定流速分别向含催化剂A和B的反应管中通入一定比例 、
、 、NO和
、NO和 的模拟烟气,测得NO的去除率与温度的关系如图3所示。使用催化剂B,当温度高于360℃,NO的去除率下降的原因是
的模拟烟气,测得NO的去除率与温度的关系如图3所示。使用催化剂B,当温度高于360℃,NO的去除率下降的原因是___________ 。 溶液可吸收含
溶液可吸收含 、NO烟气中的
、NO烟气中的 ,其反应为
,其反应为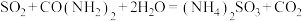 。(溶液的酸碱性会影响
。(溶液的酸碱性会影响 吸收,酸性越强
吸收,酸性越强 的溶解度越小)
的溶解度越小)
若吸收烟气时同时通入少量 ,可同时实现脱硝、脱硫。
,可同时实现脱硝、脱硫。
①脱硝的反应分为两步。第一步: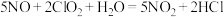 。
。
第二步: 和
和 反应生成
反应生成 和
和 。
。
第二步的化学反应方程式为___________ 。
②将含 、NO烟气以一定的流速通过10%的
、NO烟气以一定的流速通过10%的 溶液,其他条件相同,不通
溶液,其他条件相同,不通 和通少量
和通少量 时
时 的去除率如图4所示。通少量
的去除率如图4所示。通少量 时
时 的去除率较低的原因是
的去除率较低的原因是___________ 。
(1)采用“联合脱硫脱氮技术”处理烟气(含
 、
、 、NO)可获得含
、NO)可获得含 、
、 、
、 的副产品,工业流程如图所示。
的副产品,工业流程如图所示。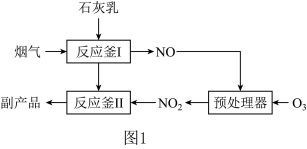

 转化为
转化为 反应的化学方程式为
反应的化学方程式为(2)烟气中的NO可在催化剂作用下用
 还原。
还原。①已知7mol氨气恰好能将含NO和
 共6mol的混合气体完全转化为
共6mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比
的物质的量之比②其它条件相同,以一定流速分别向含催化剂A和B的反应管中通入一定比例
 、
、 、NO和
、NO和 的模拟烟气,测得NO的去除率与温度的关系如图3所示。使用催化剂B,当温度高于360℃,NO的去除率下降的原因是
的模拟烟气,测得NO的去除率与温度的关系如图3所示。使用催化剂B,当温度高于360℃,NO的去除率下降的原因是
 溶液可吸收含
溶液可吸收含 、NO烟气中的
、NO烟气中的 ,其反应为
,其反应为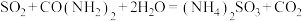 。(溶液的酸碱性会影响
。(溶液的酸碱性会影响 吸收,酸性越强
吸收,酸性越强 的溶解度越小)
的溶解度越小)若吸收烟气时同时通入少量
 ,可同时实现脱硝、脱硫。
,可同时实现脱硝、脱硫。①脱硝的反应分为两步。第一步:
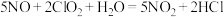 。
。第二步:
 和
和 反应生成
反应生成 和
和 。
。第二步的化学反应方程式为
②将含
 、NO烟气以一定的流速通过10%的
、NO烟气以一定的流速通过10%的 溶液,其他条件相同,不通
溶液,其他条件相同,不通 和通少量
和通少量 时
时 的去除率如图4所示。通少量
的去除率如图4所示。通少量 时
时 的去除率较低的原因是
的去除率较低的原因是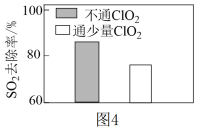
您最近一年使用:0次
名校
解题方法
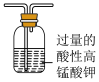
2 . 某小组用如下装置(夹持装置已略去)制备并探究 的性质。
的性质。 的化学方程式是
的化学方程式是___________ 。
(2)a中控制生成 多少的操作是
多少的操作是___________ ;反应后a中若溶液颜色无色,试管底部有灰白色固体,确定产物中有 的操作是
的操作是___________ 。
(3)b用于探究 的性质。
的性质。
①b中为___________ 溶液时,可证明 有漂白性。
有漂白性。
②b中为 和淀粉混合溶液时,溶液蓝色褪去,可证明
和淀粉混合溶液时,溶液蓝色褪去,可证明 有还原性,反应的化学方程式为
有还原性,反应的化学方程式为___________ 。
③b中为 溶液时,反应后在溶液中可检验出
溶液时,反应后在溶液中可检验出 ,说明检验
,说明检验 的方法是
的方法是___________ 。
④b中为 溶液时,出现淡黄色沉淀,迅速变为黄色溶液,经查阅资料黄色为多硫离子
溶液时,出现淡黄色沉淀,迅速变为黄色溶液,经查阅资料黄色为多硫离子 的颜色,出现淡黄色沉淀时氧化产物和还原产物的物质的量之比为
的颜色,出现淡黄色沉淀时氧化产物和还原产物的物质的量之比为___________ 。随着反应进行,又出现淡黄色沉淀,溶液黄色消失,这是由于溶液中的 与过量
与过量 又继续反应了,写出反应的离子方程式
又继续反应了,写出反应的离子方程式___________ 。
(资料: 能与S反应生成
能与S反应生成 ,
, 与酸反应生成S和
与酸反应生成S和 )。
)。
(4)c用于吸收 尾气,可选用的试剂是
尾气,可选用的试剂是___________ 。
A.NaOH溶液 B.澄清石灰水 C. 溶液
溶液
 的性质。
的性质。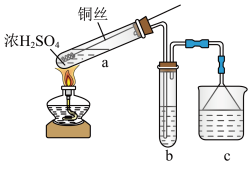
 的化学方程式是
的化学方程式是(2)a中控制生成
 多少的操作是
多少的操作是 的操作是
的操作是(3)b用于探究
 的性质。
的性质。①b中为
 有漂白性。
有漂白性。②b中为
 和淀粉混合溶液时,溶液蓝色褪去,可证明
和淀粉混合溶液时,溶液蓝色褪去,可证明 有还原性,反应的化学方程式为
有还原性,反应的化学方程式为③b中为
 溶液时,反应后在溶液中可检验出
溶液时,反应后在溶液中可检验出 ,说明检验
,说明检验 的方法是
的方法是④b中为
 溶液时,出现淡黄色沉淀,迅速变为黄色溶液,经查阅资料黄色为多硫离子
溶液时,出现淡黄色沉淀,迅速变为黄色溶液,经查阅资料黄色为多硫离子 的颜色,出现淡黄色沉淀时氧化产物和还原产物的物质的量之比为
的颜色,出现淡黄色沉淀时氧化产物和还原产物的物质的量之比为 与过量
与过量 又继续反应了,写出反应的离子方程式
又继续反应了,写出反应的离子方程式(资料:
 能与S反应生成
能与S反应生成 ,
, 与酸反应生成S和
与酸反应生成S和 )。
)。(4)c用于吸收
 尾气,可选用的试剂是
尾气,可选用的试剂是A.NaOH溶液 B.澄清石灰水 C.
 溶液
溶液
您最近一年使用:0次
名校
解题方法
3 . 硫酸是当今世界上最重要的化工产品之一,目前工业制备硫酸主要采用以硫铁矿 为原料。硫酸工业、金属冶炼产生的尾气中含有
为原料。硫酸工业、金属冶炼产生的尾气中含有 ,需经回收利用处理才能排放到空气中。下列有关化学反应表示
,需经回收利用处理才能排放到空气中。下列有关化学反应表示不正确 的是
 为原料。硫酸工业、金属冶炼产生的尾气中含有
为原料。硫酸工业、金属冶炼产生的尾气中含有 ,需经回收利用处理才能排放到空气中。下列有关化学反应表示
,需经回收利用处理才能排放到空气中。下列有关化学反应表示A.煅烧硫铁矿获得 : : |
B.接触室中 被氧化: 被氧化: |
C.用少量氨水吸收尾气中的 : : |
D. 与 与 溶液反应的离子方程式: 溶液反应的离子方程式: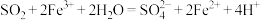 |
您最近一年使用:0次
名校
4 . 下列有关物质的性质与用途具有对应关系的是
A. 性质稳定,工业生产金属镁时,为防止其氧化,可以用 性质稳定,工业生产金属镁时,为防止其氧化,可以用 作保护气 作保护气 |
B. 易溶于水,可用作制冷剂 易溶于水,可用作制冷剂 |
C.氨水具有碱性,可用于去除烟气中的 |
D. 具有氧化性,可用于生产氮肥 具有氧化性,可用于生产氮肥 |
您最近一年使用:0次
5 . 下面是某校化学研究性学习小组探究足量锌与浓硫酸反应的实验:
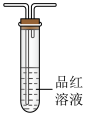
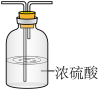
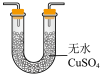
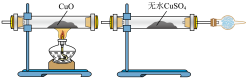
Ⅰ.甲同学设计如图实验验证该反应产生的混合气体中含有SO2、H2、H2O,已知装置C中试剂过量。
(1)写出A中生成SO2的化学方程式___________ 。
(2)若按气体从左到右的流向,气体流经的各装置连接顺序是___________ 。
(3)E中干燥管的作用是___________ 。
(4)证明混合气体中含有H2的实验现象为___________ 。
Ⅱ.乙同学设计如下实验步骤测定44.8L(标准状况下)混合气体中SO2的体积分数。___________ (填序号)。
A.H2O2溶液 B.硫酸酸化的KMnO4溶液 C.溴水
(6)该混合气体中二氧化硫的体积分数为___________ (用含m的代数式表示)。
Ⅰ.甲同学设计如图实验验证该反应产生的混合气体中含有SO2、H2、H2O,已知装置C中试剂过量。
|
|
|
| A | B | C |
|
|
|
| D | E | F |
(1)写出A中生成SO2的化学方程式
(2)若按气体从左到右的流向,气体流经的各装置连接顺序是
(3)E中干燥管的作用是
(4)证明混合气体中含有H2的实验现象为
Ⅱ.乙同学设计如下实验步骤测定44.8L(标准状况下)混合气体中SO2的体积分数。
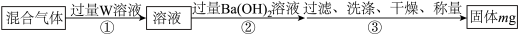
A.H2O2溶液 B.硫酸酸化的KMnO4溶液 C.溴水
(6)该混合气体中二氧化硫的体积分数为
您最近一年使用:0次
6 . 对下列事实的解释正确的是
| A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| B.浓硝酸在光照下颜色变黄,说明浓硝酸易挥发 |
| C.常温下,浓硝酸可以用铝制器皿贮存,说明铝与浓硝酸不反应 |
| D.将SO2通入BaCl2溶液至饱和,无沉淀生成,继续通入另一种气体有白色沉淀,则通入的气体一定是NH3 |
您最近一年使用:0次
解题方法
7 . 物质的性质决定用途,下列关于物质的应用中不涉及该物质的化学性质的是
| A.碳酸氢钠作膨松剂 | B.二硫化碳去除试管壁上的硫 |
| C.二氧化硫漂白草帽 | D.Vc片帮助人体吸收食物中的铁元素 |
您最近一年使用:0次
解题方法
8 . 按要求回答问题
Ⅰ.分类法是进行化学研究的重要方法。不同的标准可以把事物分为不同的类别。
现有以下物质:①固体NaHCO3 ② ③CaCO3 ④Fe(OH)3胶体 ⑤熔融的NaHSO4 ⑥干冰 ⑦稀盐酸 ⑧蔗糖
③CaCO3 ④Fe(OH)3胶体 ⑤熔融的NaHSO4 ⑥干冰 ⑦稀盐酸 ⑧蔗糖
(1)以上物质中属于混合物的是_______ (填序号);
(2)写出①在水溶液中的电离方程式_______ ;
(3)④的实验室制备方案:向沸水中滴加几滴_______ 溶液,加热至液体呈红褐色,停止加热。
Ⅱ.空气与我们的生活息息相关。 是主要的大气污染物之一,
是主要的大气污染物之一, 是主要的温室气体。双碱法脱硫过程如图所示。
是主要的温室气体。双碱法脱硫过程如图所示。

(4)SO2属于_______ (填“酸性”或“碱性”)氧化物。过程Ⅰ发生的离子方程式是_______ 。
(5)下列反应中,能用同一离子方程式表示的是_______(填序号)。
(6)用化学方程式表示过程Ⅱ发生的化学反应_______ 。
Ⅰ.分类法是进行化学研究的重要方法。不同的标准可以把事物分为不同的类别。
现有以下物质:①固体NaHCO3 ②
 ③CaCO3 ④Fe(OH)3胶体 ⑤熔融的NaHSO4 ⑥干冰 ⑦稀盐酸 ⑧蔗糖
③CaCO3 ④Fe(OH)3胶体 ⑤熔融的NaHSO4 ⑥干冰 ⑦稀盐酸 ⑧蔗糖(1)以上物质中属于混合物的是
(2)写出①在水溶液中的电离方程式
(3)④的实验室制备方案:向沸水中滴加几滴
Ⅱ.空气与我们的生活息息相关。
 是主要的大气污染物之一,
是主要的大气污染物之一, 是主要的温室气体。双碱法脱硫过程如图所示。
是主要的温室气体。双碱法脱硫过程如图所示。
(4)SO2属于
(5)下列反应中,能用同一离子方程式表示的是_______(填序号)。
A. 和稀 和稀 | B. 和稀 和稀 |
C. 与稀 与稀 | D. 与稀 与稀 |
(6)用化学方程式表示过程Ⅱ发生的化学反应
您最近一年使用:0次
解题方法
9 . 实验室制取 时,下列装置不能达到相应实验目的的是
时,下列装置不能达到相应实验目的的是
 时,下列装置不能达到相应实验目的的是
时,下列装置不能达到相应实验目的的是A.制备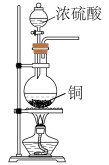 | B.检验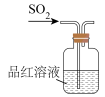 |
C.干燥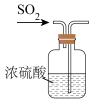 | D.收集 |
您最近一年使用:0次
2023-11-10更新
|
352次组卷
|
2卷引用:江苏省无锡市2023-2024学年高三上学期期中教学质量调研测试化学试卷题
10 . 二氧化硫是一种重要的含硫化合物,在生产、生活中应用广泛。下列说法正确的是:
| A.常温下,SO2是一种无色、有刺激性气味的气体 |
| B.SO2可以使酸性高锰钾溶液红色褪去,表现出漂白性 |
| C.SO2能使品红溶液红色褪去,表现出氧化性 |
| D.SO2在红酒中添加,是利用其强氧化性 |
您最近一年使用:0次