名校
1 . 实验室可用下列装置(部分夹持仪器略去)制取SO2并验证其性质。_______ ,则气密性良好。
(2)装置A中反应的化学方程式为_______ 。
(3)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有_______ (填“还原性”、“氧化性”或“漂白性”);经测定,产物中含有一种摩尔质量为104g/mol的盐,该盐的化学式为_______ 。
(4)试管D中反应的离子方程式为_______ 。
(5)实验结束时,关闭止水夹K,装置B的作用是_______ 。
(6)用图所示装置验证H2SO3酸性比H2CO3强。_______ ,Y为_______ ,Z为_______ 。
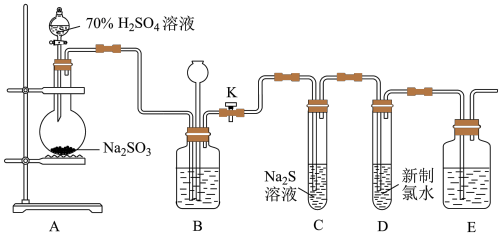
(2)装置A中反应的化学方程式为
(3)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有
(4)试管D中反应的离子方程式为
(5)实验结束时,关闭止水夹K,装置B的作用是
(6)用图所示装置验证H2SO3酸性比H2CO3强。
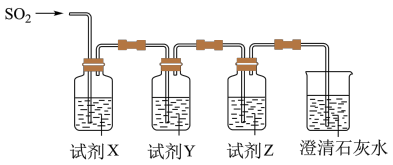
您最近半年使用:0次
解题方法
2 . 为探究某矿物X(含三种常见元素)的组成和性质,某兴趣小组设计了如下实验:已知实验中所用试剂均足量,固体B是一种单质和化合物的混合物,请回答如下问题:
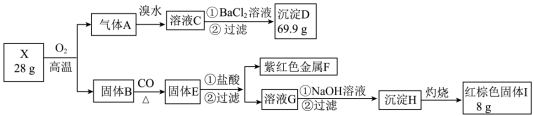
(1)X中所含元素为:___________ 。
(2)溴水是否可以用酸化的双氧水代替,若不可行,请说明理由,若可行,请写出反应的离子方程式:___________ 。
(3)检验溶液G中的金属阳离子的实验方案:___________ 。
(4)溶液G转化为沉淀H的现象___________ 。
(5)X在高温下与氧气充分反应的化学方程式:___________ 。

(1)X中所含元素为:
(2)溴水是否可以用酸化的双氧水代替,若不可行,请说明理由,若可行,请写出反应的离子方程式:
(3)检验溶液G中的金属阳离子的实验方案:
(4)溶液G转化为沉淀H的现象
(5)X在高温下与氧气充分反应的化学方程式:
您最近半年使用:0次
名校
解题方法
3 . 某化学课题小组将二氧化硫的制备与多个性质实验进行了一体化设计,实验装置如图所示。已知: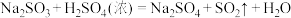 ,下列说法错误的是
,下列说法错误的是
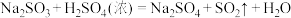 ,下列说法错误的是
,下列说法错误的是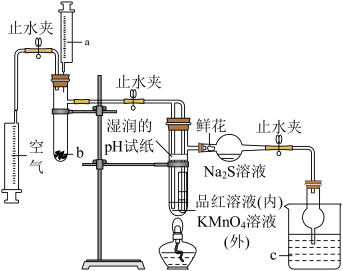
A.a、b、c中盛装物质可以分别为浓硫酸、 固体、 固体、 溶液 溶液 |
B.实验时,湿润的pH试纸、鲜花、品红溶液、酸性 溶液均褪色, 溶液均褪色, 溶液中出现淡黄色沉淀 溶液中出现淡黄色沉淀 |
C.此设计可证明 水溶液呈酸性, 水溶液呈酸性, 具有氧化性、还原性、漂白性 具有氧化性、还原性、漂白性 |
D.点燃酒精灯加热,可证明 使品红溶液褪色具有可逆性,使酸性 使品红溶液褪色具有可逆性,使酸性 溶液褪色不具有可逆性 溶液褪色不具有可逆性 |
您最近半年使用:0次
2024-02-02更新
|
439次组卷
|
3卷引用:浙江金华第一中学2023-2024学年高一下学期4月期中考试化学试题
浙江金华第一中学2023-2024学年高一下学期4月期中考试化学试题河南省南阳市2023-2024学年高一上学期1月期末化学试题(已下线)专题01 硫及其化合物(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
4 . 下列操作正确且能达到实验目的是
| 选项 | 实验操作 | 实验目的 |
| A | 向BaCO3溶液中加入饱和Na2SO4溶液 | 验证:Ksp(BaSO4)<Ksp(BaCO3) |
| B | 在相同条件下,向两份4mL0.5mol·L-1酸性KMnO4溶液中分别滴加2mL0.1mol·L-1和0.2mol·L-1草酸溶液,滴加0.2mol·L-1草酸溶液的先褪色 | 反应物浓度越大,反应速率越大 |
| C | 将产生的气体直接通入澄清石灰水中,有白色沉淀生成 | 证明碳和浓硫酸共热产生的气体中含有CO2 |
| D | 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入醋酸,红色很快褪为无色 | 证明“84”消毒液的氧化能力随溶液pH的减小而增强 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
5 . 下列表示对应化学反应的离子方程式正确的是
A.将少量 通入 通入 溶液: 溶液: |
B.室温下用稀 溶解铜: 溶解铜: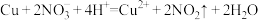 |
C.氯化铁溶液作“腐蚀液”,制作印刷电路板: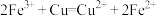 |
D.向 溶液中加入过量 溶液中加入过量 |
您最近半年使用:0次
名校
解题方法
6 . 为保障人民健康,我国制定了十分严格的SO2使用标准,《食品安全国家标准食品添加剂使用标准》(GB2760-2014)规定含硫类食品添加剂的最大使用量范围为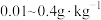 (以SO2残留量计算)。某化学兴趣小组按照如下步骤测定内黄大枣中
(以SO2残留量计算)。某化学兴趣小组按照如下步骤测定内黄大枣中 的残留量,
的残留量,
i.准确称取 去核大枣装入
去核大枣装入 圆底烧瓶中,将样品用硫酸酸化后加入
圆底烧瓶中,将样品用硫酸酸化后加入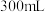 水并通入氮气,将氮气流速调至
水并通入氮气,将氮气流速调至 并低于100℃加热,蒸出的
并低于100℃加热,蒸出的 用双氧水吸收,实验装置如下图所示(夹持和加热装置已省略)。
用双氧水吸收,实验装置如下图所示(夹持和加热装置已省略)。
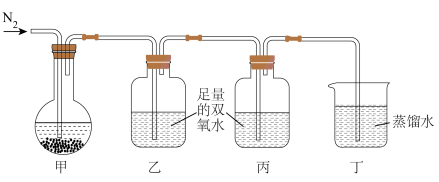
ⅱ.充分反应后,合并乙、丙中的吸收液于锥形瓶中,煮沸一段时间后,冷却。
ⅲ.滴加几滴酚酞作指示液,用 的
的 标准液滴定。重复实验四次,所得数据如表所示:
标准液滴定。重复实验四次,所得数据如表所示:
回答下列问题:
(1)双氧水吸收 时的化学方程式为
时的化学方程式为___________ 。
(2)步骤ⅱ中盛装 的
的 标准液的仪器为
标准液的仪器为___________ (填标号),该仪器使用之前需要进行的操作为___________ 。
A. B.
B. C.
C.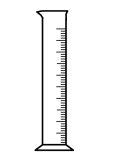 D.
D.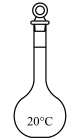
(3)步骤ⅱ中煮沸的目的可能是___________ 。
(4)步骤ⅲ的操作可分解为如下几步:
①向煮沸冷却后的吸收液锥形瓶中加入2~3滴酚酞
②用标准溶液润洗碱式滴定管2~3次
③把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴部分充满溶液
④取标准NaOH溶液注入碱式滴定管至0刻度以上2~3cm
⑤调节液面至0或0刻度以下,记下读数
⑥把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点,记下滴定管液面的刻度
正确操作的顺序是_________ (填序号)
②→___________→___________→___________→①→___________。
(5)步骤ⅲ滴定终点的现象为___________ ,下列操作会使测得的 含量偏大的是
含量偏大的是___________ (填标号)。
a.滴定前尖嘴处有气泡,滴定后消失
b.盛装 的
的 标准液的仪器未用标准液润洗
标准液的仪器未用标准液润洗
c.滴定前读数时仰视刻度线,滴定终点读数时俯视刻度线
d.氮气流速过快
(6)该大枣中 的残留量为
的残留量为___________ (保留小数点后两位) 。
。
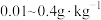 (以SO2残留量计算)。某化学兴趣小组按照如下步骤测定内黄大枣中
(以SO2残留量计算)。某化学兴趣小组按照如下步骤测定内黄大枣中 的残留量,
的残留量,i.准确称取
 去核大枣装入
去核大枣装入 圆底烧瓶中,将样品用硫酸酸化后加入
圆底烧瓶中,将样品用硫酸酸化后加入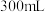 水并通入氮气,将氮气流速调至
水并通入氮气,将氮气流速调至 并低于100℃加热,蒸出的
并低于100℃加热,蒸出的 用双氧水吸收,实验装置如下图所示(夹持和加热装置已省略)。
用双氧水吸收,实验装置如下图所示(夹持和加热装置已省略)。
ⅱ.充分反应后,合并乙、丙中的吸收液于锥形瓶中,煮沸一段时间后,冷却。
ⅲ.滴加几滴酚酞作指示液,用
 的
的 标准液滴定。重复实验四次,所得数据如表所示:
标准液滴定。重复实验四次,所得数据如表所示:| 序号 | 1 | 2 | 3 | 4 |
| 标准液初始读数mL | 0.00 | 0.10 | 0.40 | 0.50 |
| 标准液滴定终点读数/mL | 8.80 | 8.95 | 10.25 | 9.25 |
(1)双氧水吸收
 时的化学方程式为
时的化学方程式为(2)步骤ⅱ中盛装
 的
的 标准液的仪器为
标准液的仪器为A.
 B.
B. C.
C. D.
D.
(3)步骤ⅱ中煮沸的目的可能是
(4)步骤ⅲ的操作可分解为如下几步:
①向煮沸冷却后的吸收液锥形瓶中加入2~3滴酚酞
②用标准溶液润洗碱式滴定管2~3次
③把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴部分充满溶液
④取标准NaOH溶液注入碱式滴定管至0刻度以上2~3cm
⑤调节液面至0或0刻度以下,记下读数
⑥把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点,记下滴定管液面的刻度
正确操作的顺序是
②→___________→___________→___________→①→___________。
(5)步骤ⅲ滴定终点的现象为
 含量偏大的是
含量偏大的是a.滴定前尖嘴处有气泡,滴定后消失
b.盛装
 的
的 标准液的仪器未用标准液润洗
标准液的仪器未用标准液润洗c.滴定前读数时仰视刻度线,滴定终点读数时俯视刻度线
d.氮气流速过快
(6)该大枣中
 的残留量为
的残留量为 。
。
您最近半年使用:0次
名校
解题方法
7 . 在硫酸工业生产中,为了有利于 的转化,且能充分利用热能,采用了中间有热交换器的接触室(见图)。下列说法
的转化,且能充分利用热能,采用了中间有热交换器的接触室(见图)。下列说法不正确 的是

 的转化,且能充分利用热能,采用了中间有热交换器的接触室(见图)。下列说法
的转化,且能充分利用热能,采用了中间有热交换器的接触室(见图)。下列说法
| A.a、b两处的混合气体成分含量相同,温度不同 |
| B.c、d两处的混合气体成分含量相同,温度不同 |
C.由题目可知 为放热反应 为放热反应 |
D.将混合气体进行两次催化氧化的目的是提高 的转化率 的转化率 |
您最近半年使用:0次
8 . 化学来源于生活,也服务于生活,下列有关生活中的化学知识叙述正确的是
A. 能与碱反应,因此可用焙制糕点的膨松剂 能与碱反应,因此可用焙制糕点的膨松剂 |
| B.常温时,铝不与浓硝酸反应,可用铝制容器盛装浓硝酸 |
C.酿酒过程中,葡萄汁中某些细菌的繁殖会影响发酵,添加适量 可起到杀菌作用 可起到杀菌作用 |
D. 是酸性氧化物,可与水反应生成 是酸性氧化物,可与水反应生成 |
您最近半年使用:0次
名校
9 . 物质的性质决定用途,下列两者对应关系正确的是
| A.Al的性质稳定,因此铝合金常用作门窗的框架 |
B. 具有漂白性,可用于葡萄酒的添加剂 具有漂白性,可用于葡萄酒的添加剂 |
C. 具有导电性,可用于制造光导纤维 具有导电性,可用于制造光导纤维 |
| D.Fe的还原性很强,可用于食品的除氧剂 |
您最近半年使用:0次
解题方法
10 . 化学与生活息息相关,下列说法不正确的是
| A.食品中添加抗氧化剂可减缓食品变质速率 |
| B.氯气常用于自来水消毒是因为氯气有杀菌作用 |
| C.二氧化硫可用作食品添加剂起到漂白、防腐和抗氧化等作用 |
| D.碳化硅俗称金刚砂,碳原子与硅原子通过共价键连接,硬度很大,可用作砂纸和砂轮的磨料 |
您最近半年使用:0次



