1 . 物质的性质决定用途,下列两者对应关系正确的是
| A.液氨汽化时吸收大量热,可用作制冷剂 |
B. 具有氧化性,葡萄酒中添加 具有氧化性,葡萄酒中添加 起到漂白作用 起到漂白作用 |
| C.钾钠合金具有还原性,用于快中子反应堆的热交换剂 |
D. 具有氧化性,可用作净水剂 具有氧化性,可用作净水剂 |
您最近一年使用:0次
2 .  是重要的化工原料,按如下流程充分利用。
是重要的化工原料,按如下流程充分利用。___________ (用化学式表示)。
②写出途径Ⅰ反应的化学方程式___________ 。
③ 是离子化合物,各原子均满足8电子稳定结构。写出
是离子化合物,各原子均满足8电子稳定结构。写出 的电子式
的电子式___________ 。
(2)下列说法不正确 的是___________。
(3)① 为二元弱碱,其在水中的电离与氨相似;25℃,
为二元弱碱,其在水中的电离与氨相似;25℃, 第一步电离平衡常数
第一步电离平衡常数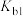 的值为
的值为___________ 。(已知: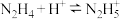
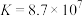 )
)
②结合 的能力:
的能力:
___________  (填“>”或“<”),理由是
(填“>”或“<”),理由是___________ 。
(4)设计实验验证混合物A中含有S元素___________ 。
 是重要的化工原料,按如下流程充分利用。
是重要的化工原料,按如下流程充分利用。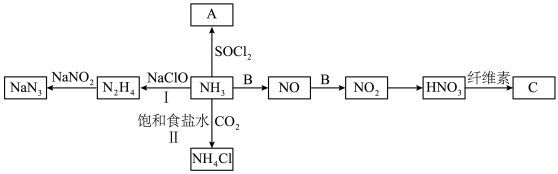
已知:①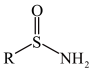 与
与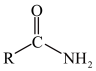 性质相似
性质相似
②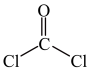 +4NH3
+4NH3
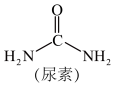 +2NH4Cl
+2NH4Cl
②写出途径Ⅰ反应的化学方程式
③
 是离子化合物,各原子均满足8电子稳定结构。写出
是离子化合物,各原子均满足8电子稳定结构。写出 的电子式
的电子式(2)下列说法
A.工业制 ,综合考虑B为空气 ,综合考虑B为空气 |
B.途径Ⅱ,向饱和食盐水中先通入 ,再通入 ,再通入 |
C.尿素 是常用的氮肥,不能与草木灰混合施用 是常用的氮肥,不能与草木灰混合施用 |
| D.物质C属于有机高分子化合物,可用于生产火药、塑料和涂料 |
(3)①
 为二元弱碱,其在水中的电离与氨相似;25℃,
为二元弱碱,其在水中的电离与氨相似;25℃, 第一步电离平衡常数
第一步电离平衡常数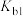 的值为
的值为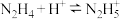
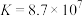 )
)②结合
 的能力:
的能力:
 (填“>”或“<”),理由是
(填“>”或“<”),理由是(4)设计实验验证混合物A中含有S元素
您最近一年使用:0次
解题方法
3 . 探究铁单质及其化合物的性质,由操作、现象能得出正确结论的是
| 选项 | 操作 | 现象 | 结论 |
| A. | 向2mL 0.1mol·L⁻¹FeCl3溶液加入 2mL 0.01mol·L⁻¹KI溶液,再滴入数滴AgNO3溶液 | 出现黄色浑浊 | 证明 FeCl3和 KI反应存在限度 |
| B. | 将Fe粉与S粉混合在惰性气体中加热,再将反应后的产物溶于稀硫酸 | 得到黑色固体,该固体溶于稀硫酸后得浅绿色溶液 | 证明Fe与S生成了FeS |
| C. | 向2mL 0.01mol·L⁻¹Fe(SCN)3溶液加入少量 Fe粉,振荡后静置 | 溶液的血红色变浅 | 证明Fe 粉与Fe3⁺反应,降低Fe3⁺浓度,使生成Fe(SCN)3平衡逆向移动 |
| D. | 将SO2气体通入 Fe(NO3)3和BaCl2的混合溶液 | 溶液的棕黄色变浅、产生白色沉淀 | 白色沉淀为 BaSO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 物质的性质决定用途,下列两者对应关系正确的是
| A.SO2具有杀菌作用,用作葡萄酒中的抗氧化剂 |
| B.SiO2具有导电性,用于制造光导纤维 |
| C.碳酸氢钠能与碱反应,用作食品的膨松剂 |
| D.Na能与水反应,用作乙醚的除水剂 |
您最近一年使用:0次
5 . 硫化氢是一种气体信号分子,人体中微量的 H2S能有效预防心脏病。下列有关说法不正确的是
| A.H2S 属于弱电解质 |
| B.H2S可以使稀酸性高锰酸钾溶液褪色 |
| C.H2S 通入 CuSO4溶液中无明显现象 |
| D.人体内 H2S 可由含硫蛋白质通过复杂反应产生 |
您最近一年使用:0次
名校
解题方法
6 . 下列“类比”不正确 的是
| A.Ba(NO3)2溶液中通入SO2生成BaSO4沉淀,则CaCl2溶液中通入CO2生成CaCO3沉淀 |
| B.乙烯能被酸性KMnO4氧化为CO2,丙烯也能被酸性KMnO4氧化生成CO2 |
| C.元素周期表中锂和镁位于对角线上,MgCO3微溶于水,则Li2CO3也微溶于水 |
| D.AgOH溶于氨水生成Ag(NH3)2OH,则Cu(OH)2溶于氨水生成Cu(NH3)4(OH)2 |
您最近一年使用:0次
2022-11-28更新
|
213次组卷
|
2卷引用:浙江省9+1高中联盟2022-2023学年高三上学期期中考试化学试题
7 . 下列说法不正确 的是
| A.氯碱工业阴极室内的产物是NaOH和H2 |
| B.石灰石可以用于制玻璃工业,是因为高温下碳酸钙与二氧化硅会发生反应 |
| C.铝热反应非常剧烈,在工业上可以炼铁 |
| D.金属冶炼时产生含二氧化硫的废气经回收后可用于制备硫酸 |
您最近一年使用:0次
2022-11-28更新
|
216次组卷
|
2卷引用:浙江省9+1高中联盟2022-2023学年高三上学期期中考试化学试题
8 . 下列说法正确的是
A.新制氯水中加入少量 固体能增强漂白能力 固体能增强漂白能力 |
| B.工业制镁用干冰做冷却剂 |
C.实验室通常用 加热分解制取 加热分解制取 |
D. 的漂白原理和氯气相同 的漂白原理和氯气相同 |
您最近一年使用:0次
2022-04-23更新
|
215次组卷
|
2卷引用:浙江省稽阳联谊学校2021-2022学年高三下学期4月联考化学试题
解题方法
9 . 某化学兴趣小组为了探究一种复盐A(含五种元素,相对分子质量小于200)的组成与性质,设计并完成如图实验:

已知:气体B为无色气体,能使品红溶液褪色;气体C能使湿润的红色石蕊试纸变蓝;溶液B中的溶质只含一种阴离子,并测得其c(H+)=0.8mol•L-1,过程中所加试剂均足量。
请回答:
(1)A的组成元素除H、O外还有____ (用元素符号表示)。
(2)写出气体C的电子式___ 。
(3)写出固体A与H2SO4反应的化学方程式___ ,反应中每生成1mol气体B,转移电子的数目为____ (用NA表示阿伏加德罗常数)。
(4)沉淀C可溶于气体C的水溶液中,可得深蓝色溶液,写出该过程的离子方程式___ 。
(5)固体D是氧化物,受灼烧温度影响,D中金属元素的化合价可能呈现不同价态,请设计简单实验验证D中金属元素是否含+1价:___ 。

已知:气体B为无色气体,能使品红溶液褪色;气体C能使湿润的红色石蕊试纸变蓝;溶液B中的溶质只含一种阴离子,并测得其c(H+)=0.8mol•L-1,过程中所加试剂均足量。
请回答:
(1)A的组成元素除H、O外还有
(2)写出气体C的电子式
(3)写出固体A与H2SO4反应的化学方程式
(4)沉淀C可溶于气体C的水溶液中,可得深蓝色溶液,写出该过程的离子方程式
(5)固体D是氧化物,受灼烧温度影响,D中金属元素的化合价可能呈现不同价态,请设计简单实验验证D中金属元素是否含+1价:
您最近一年使用:0次
名校
解题方法
10 . 下列“类比”结果正确的是
| A.适量CO2通入Ca(ClO)2溶液中可生成CaCO3和HClO,则适量SO2通入Ca(ClO)2溶液中可生成CaSO3和HClO |
| B.实验室用浓硫酸和NaCl固体共热制备HCl,则可用浓硫酸和NaBr固体共热制备HBr |
| C.Mg与CO2反应生成MgO和C,则Mg与SO2反应生成MgO和S |
| D.Fe和S反应生成FeS,则Cu和S反应生成Cu2S |
您最近一年使用:0次
2021-11-24更新
|
1062次组卷
|
5卷引用: 浙江省9+1高中联盟2021-2022学年高三上学期期中考试化学试题
浙江省9+1高中联盟2021-2022学年高三上学期期中考试化学试题(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)3.2.1 硫与二氧化硫-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)江西省宜春市奉新县第一中学2021-2022学年高一下学期第二次月考化学试题重庆第二十三中学校2021-2022学年高一下学期第一次月考化学试题



