解题方法
1 . 硫元素广泛存在于自然界中,是植物生长不可缺少的元素。回答下列问题:
(1)某小组同学设计实验实现不同价态含硫物质的转化。
可选用的实验试剂如下:
A. 溶液 B.浓硫酸 C.
溶液 B.浓硫酸 C. 溶液
溶液
D.稀硫酸 E.酸性 溶液 F.品红溶液 G.铜丝
溶液 F.品红溶液 G.铜丝
实验i选择的试剂是E和______ (填字母),证明实现转化的现象是______ 。
(2)该小组同学利用所选试剂,设计了如图所示装置研究实验ⅱ。
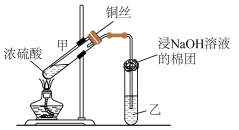
①试管甲中发生反应的化学方程式是__________ 。
②试管乙中的现象是_______ ;若实验结束后,将试管乙中的溶液加热,可以观察到的现象是______ 。
③下列关于 的说法,不正确的是
的说法,不正确的是__________ 。(填字母)
a.正常雨水的 等于7,酸雨因为溶解了
等于7,酸雨因为溶解了 ,其
,其 小于7
小于7
b.金属冶炼时产生的含 废气经回收后可用于制备硫酸
废气经回收后可用于制备硫酸
c. 在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
(1)某小组同学设计实验实现不同价态含硫物质的转化。
可选用的实验试剂如下:
A.
 溶液 B.浓硫酸 C.
溶液 B.浓硫酸 C. 溶液
溶液D.稀硫酸 E.酸性
 溶液 F.品红溶液 G.铜丝
溶液 F.品红溶液 G.铜丝实验序号 | 预期转化 | 选择试剂 | 证明实现转化的现象 |
i |
| ||
ii |
|
|
(2)该小组同学利用所选试剂,设计了如图所示装置研究实验ⅱ。

①试管甲中发生反应的化学方程式是
②试管乙中的现象是
③下列关于
 的说法,不正确的是
的说法,不正确的是a.正常雨水的
 等于7,酸雨因为溶解了
等于7,酸雨因为溶解了 ,其
,其 小于7
小于7b.金属冶炼时产生的含
 废气经回收后可用于制备硫酸
废气经回收后可用于制备硫酸c.
 在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
您最近一年使用:0次
2 . 某化学兴趣小组将制丝插入热浓硫酸中,进行如下图所示的 性质的探究实验。(a、b、c、d均为没有相应浴液的棉花,部分夹持仪器已略去)
性质的探究实验。(a、b、c、d均为没有相应浴液的棉花,部分夹持仪器已略去)_______ 。
(2)铜丝与热浓硫酸反应的化学方程式为_______ 。
(3)实验进行一段时间后:
①a处实验现象为_______ 。
②b处品红溶液褪色,原因是_______ 。
③c处酸性 溶液褪色,证明
溶液褪色,证明 具有
具有_______ 性。
④d处NaOH溶液的作用是_______ ,写出反应的离子方程式:_______ 。
(4)该实验装置中使用可抽动铜丝的优点是_______ 。
 性质的探究实验。(a、b、c、d均为没有相应浴液的棉花,部分夹持仪器已略去)
性质的探究实验。(a、b、c、d均为没有相应浴液的棉花,部分夹持仪器已略去)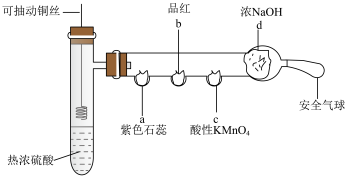
(2)铜丝与热浓硫酸反应的化学方程式为
(3)实验进行一段时间后:
①a处实验现象为
②b处品红溶液褪色,原因是
③c处酸性
 溶液褪色,证明
溶液褪色,证明 具有
具有④d处NaOH溶液的作用是
(4)该实验装置中使用可抽动铜丝的优点是
您最近一年使用:0次
2024-03-29更新
|
102次组卷
|
2卷引用:2023年6月福建省普通高中学业水平合格性考试化学试题
3 . 根据所学相关知识完成下列问题。
Ⅰ.小组Ⅰ用下图装置制取Cl2并探究性质,回答下列问题:

(1)装置①用于制取Cl2,反应的化学方程式是_____
(2)装置②的作用是_____
(3)装置③中的现象是_____
(4)装置④中发生反应的离子方程式是_____
Ⅱ.小组Ⅱ利用如图所示装置探究二氧化硫气体的性质,回答下列问题:
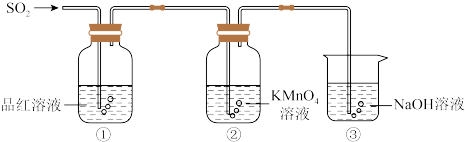
(5)实验室用铜和浓硫酸共热制取二氧化硫,反应的化学方程式是_____
(6)当观察到②中溶液颜色变浅时,①中的现象是_____
(7)装置③的作用是_____
(8)②中的现象说明二氧化硫具有的性质是_____
Ⅲ.小组Ⅲ用图1所示装置制取氨,并探究其性质,回答下列问题:
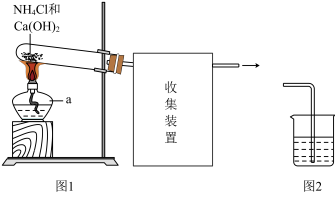
(9)仪器a的名称是_____
(10)图1试管内发生反应的化学方程式是_____
(11)图1方框中的收集装置应为_____ (填图3中字母标号)。
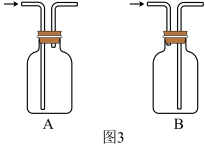
(12)将蘸有浓盐酸的棉球放入收集满NH3的集气瓶中,迅速盖上玻璃片,可观察到的实验现象是_____
(13)甲同学设计了图2所示的装置进行尾气处理,乙同学认为该设计不合理,其理由是_____
Ⅰ.小组Ⅰ用下图装置制取Cl2并探究性质,回答下列问题:

(1)装置①用于制取Cl2,反应的化学方程式是
(2)装置②的作用是
(3)装置③中的现象是
(4)装置④中发生反应的离子方程式是
Ⅱ.小组Ⅱ利用如图所示装置探究二氧化硫气体的性质,回答下列问题:

(5)实验室用铜和浓硫酸共热制取二氧化硫,反应的化学方程式是
(6)当观察到②中溶液颜色变浅时,①中的现象是
(7)装置③的作用是
(8)②中的现象说明二氧化硫具有的性质是
Ⅲ.小组Ⅲ用图1所示装置制取氨,并探究其性质,回答下列问题:

(9)仪器a的名称是
(10)图1试管内发生反应的化学方程式是
(11)图1方框中的收集装置应为

(12)将蘸有浓盐酸的棉球放入收集满NH3的集气瓶中,迅速盖上玻璃片,可观察到的实验现象是
(13)甲同学设计了图2所示的装置进行尾气处理,乙同学认为该设计不合理,其理由是
您最近一年使用:0次
解题方法
4 . 某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。
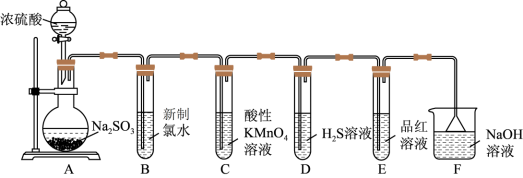
已知: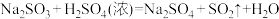 ;请回答下列问题:
;请回答下列问题:
(1)装置A中盛放亚硫酸钠溶液的仪器名称是_______ 。
(2)装置B中发生的离子方程式为_______ 。
(3)以上装置中表现了SO2氧化性的是_______ (填装置字母);
(4)装置F中倒扣漏斗的作用是_______ 。
(5)装置E的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:_______ 。

已知:
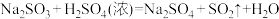 ;请回答下列问题:
;请回答下列问题:(1)装置A中盛放亚硫酸钠溶液的仪器名称是
(2)装置B中发生的离子方程式为
(3)以上装置中表现了SO2氧化性的是
(4)装置F中倒扣漏斗的作用是
(5)装置E的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:
您最近一年使用:0次
5 . 为研究二氧化硫的性质,某兴趣小组设计如下装置进行实验。

(1)a是___________ (填仪器名称)。
(2)在组装好装置装入药品前,需要进行的操作是___________ 。
(3)将少量 溶液缓慢推入
溶液缓慢推入 粉末处,发生反应。
粉末处,发生反应。
① 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
②随着反应的进行,c处实验现象为___________ ,b处实验现象为___________ 。
③几分钟后,发现d处气球变小,逐渐恢复至原样,说明二氧化硫具有的性质是___________ 。
④为证明二氧化硫与水反应具有可逆性,需要进行的实验操作是___________ 。
(4)这种实验设计的优点之一是___________ 。

(1)a是
(2)在组装好装置装入药品前,需要进行的操作是
(3)将少量
 溶液缓慢推入
溶液缓慢推入 粉末处,发生反应。
粉末处,发生反应。①
 与
与 反应的化学方程式为
反应的化学方程式为②随着反应的进行,c处实验现象为
③几分钟后,发现d处气球变小,逐渐恢复至原样,说明二氧化硫具有的性质是
④为证明二氧化硫与水反应具有可逆性,需要进行的实验操作是
(4)这种实验设计的优点之一是
您最近一年使用:0次
解题方法
6 . 某校化学兴趣小组用下图所示装置探究 的性质。请回答:
的性质。请回答:
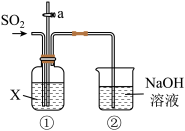
(1)装置②中发生反应的化学方程式是_______ 。
(2)若X为品红溶液,可观察到装置①中溶液_______ ,说明 具有
具有_______ 性。
(3)若X为紫色石蕊溶液,可观察到装置①中溶液_______ ,说明 的水溶液显
的水溶液显_______ (填“酸性”或“碱性”)。
(4)若X为 溶液,可观察到装置①中
溶液,可观察到装置①中_______ (填“有”或“无”)明显现象。打开活塞a,通入氧气,有白色沉淀生成,说明 最终被氧化为
最终被氧化为 ,由此可知
,由此可知 具有
具有_______ (填“氧化性”或“还原性”)。
(5)若X为 溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明
溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明 具有
具有_______ (填“氧化性”或“还原性”)。写出相应的化学方程式:_______ 。
 的性质。请回答:
的性质。请回答:
(1)装置②中发生反应的化学方程式是
(2)若X为品红溶液,可观察到装置①中溶液
 具有
具有(3)若X为紫色石蕊溶液,可观察到装置①中溶液
 的水溶液显
的水溶液显(4)若X为
 溶液,可观察到装置①中
溶液,可观察到装置①中 最终被氧化为
最终被氧化为 ,由此可知
,由此可知 具有
具有(5)若X为
 溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明
溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明 具有
具有
您最近一年使用:0次
解题方法
7 . 浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如下图所示的实验。请据此回答下列问题。
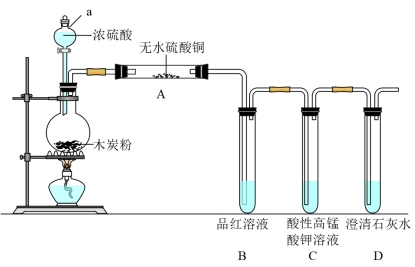
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式_______ 。
(2)仪器a的名称是_______ 。
(3)装置A中出现_______ 现象,证明气体产物中有 。
。
(4)C装置作用是_______ 。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式
(2)仪器a的名称是
(3)装置A中出现
 。
。(4)C装置作用是
您最近一年使用:0次
2022-04-15更新
|
980次组卷
|
4卷引用:陕西省2022-2023学年高二下学期化学学业水平模拟测试(二)
名校
解题方法
8 . 实验室制备CuCl:将按一定物质的量之比混合的CuSO4溶液和NaCl溶液加入到三颈烧瓶中(装置如图1所示,其中夹持仪器已省略),通入SO2,充分反应后过滤,得CuCl。CuCl的产率随NaCl和CuSO4的物质的量之比变化如图2所示。已知:CuCl是难溶于水的白色固体,能溶于浓盐酸产生[CuCl2]-。下列说法错误的是

| A.装置a中每生成1 mol CuCl,理论上至少需要通入标准状况下22.4 L SO2 |
| B.装置b的作用是安全瓶,防止倒吸 |
| C.装置c中的液体可以是NaOH浓溶液,吸收尾气 |
| D.当n(NaCl)/n(CuSO4)大于1.6时,CuCl产率减小的原因是部分CuCl转化为[CuCl2]- |
您最近一年使用:0次
2024-01-10更新
|
189次组卷
|
3卷引用:江苏省连云港市2023-2024学年高二上学期普通高中学业水平合格性考试模拟化学试题