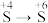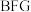解题方法
1 . 硫酸亚铁可用于治疗缺铁性贫血症。某兴趣小组为探究硫酸亚铁的分解产物,设计实验方案如下:
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有15.20g FeSO4的硬质玻璃管;
③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。
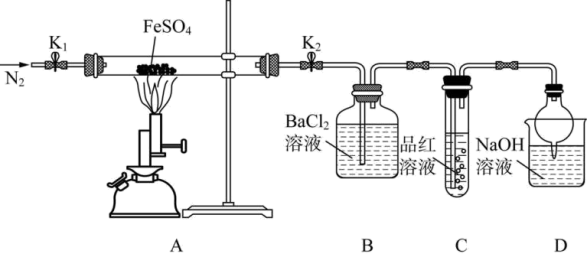
(1)根据B装置中的实验现象可推测分解产物中含有______ 。
(2)将装置B、C顺序颠倒能否达到原来的实验目的___ (填“能”或“不能”),原因是___ 。
(3)D装置中发生的主要反应的化学方程式是______ 。
(4)通过计算确定已分解的FeSO4物质的量,写出计算过程_______ 。
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有15.20g FeSO4的硬质玻璃管;
③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。

(1)根据B装置中的实验现象可推测分解产物中含有
(2)将装置B、C顺序颠倒能否达到原来的实验目的
(3)D装置中发生的主要反应的化学方程式是
(4)通过计算确定已分解的FeSO4物质的量,写出计算过程
您最近一年使用:0次
解题方法
2 . 硫元素广泛存在于自然界中,是植物生长不可缺少的元素。回答下列问题:
(1)某小组同学设计实验实现不同价态含硫物质的转化。
可选用的实验试剂如下:
A. 溶液 B.浓硫酸 C.
溶液 B.浓硫酸 C. 溶液
溶液
D.稀硫酸 E.酸性 溶液 F.品红溶液 G.铜丝
溶液 F.品红溶液 G.铜丝
实验i选择的试剂是E和______ (填字母),证明实现转化的现象是______ 。
(2)该小组同学利用所选试剂,设计了如图所示装置研究实验ⅱ。
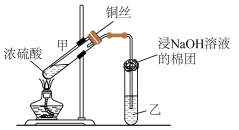
①试管甲中发生反应的化学方程式是__________ 。
②试管乙中的现象是_______ ;若实验结束后,将试管乙中的溶液加热,可以观察到的现象是______ 。
③下列关于 的说法,不正确的是
的说法,不正确的是__________ 。(填字母)
a.正常雨水的 等于7,酸雨因为溶解了
等于7,酸雨因为溶解了 ,其
,其 小于7
小于7
b.金属冶炼时产生的含 废气经回收后可用于制备硫酸
废气经回收后可用于制备硫酸
c. 在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
(1)某小组同学设计实验实现不同价态含硫物质的转化。
可选用的实验试剂如下:
A.
 溶液 B.浓硫酸 C.
溶液 B.浓硫酸 C. 溶液
溶液D.稀硫酸 E.酸性
 溶液 F.品红溶液 G.铜丝
溶液 F.品红溶液 G.铜丝实验序号 | 预期转化 | 选择试剂 | 证明实现转化的现象 |
i |
| ||
ii |
|
|
(2)该小组同学利用所选试剂,设计了如图所示装置研究实验ⅱ。

①试管甲中发生反应的化学方程式是
②试管乙中的现象是
③下列关于
 的说法,不正确的是
的说法,不正确的是a.正常雨水的
 等于7,酸雨因为溶解了
等于7,酸雨因为溶解了 ,其
,其 小于7
小于7b.金属冶炼时产生的含
 废气经回收后可用于制备硫酸
废气经回收后可用于制备硫酸c.
 在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
您最近一年使用:0次
3 . 请用你学到的化学知识填空。
Ⅰ.实验室可用下图装置对铜与浓硫酸的反应进行探究。

(1)加热条件下铜与浓硫酸反应的化学方程式_______ 。反应中氧化剂与还原剂的物质的量之比_______ 。
(2)将产生的气体通入品红溶液中的现象_______ ,通入紫色石蕊溶液中的现象_______ 。
(3)某工厂使用的煤中硫的质量分数为0.64%,该工厂每天燃烧这种煤100 t,如果把产生的SO2全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量为_______ t。
Ⅱ.实验室制氯气可用下图装置,并进行氯气性质实验。
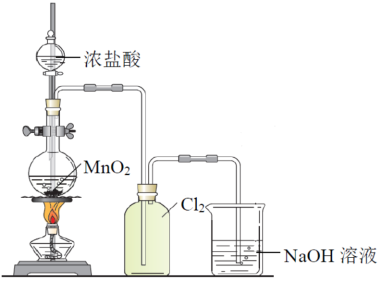
(4)写出实验室制备氯气的化学方程式:_______ 。
(5)将氯气通入冷的石灰乳中可制备用于环境消毒的漂白粉,写出此反应的化学方程式_______ 。
(6)将氯气通入KBr溶液中可发生置换反应,写出反应的离子方程式_______ ;通过单质之间的置换证明氧化性Cl2_______ Br2(填“>”,“<”或“=”)。
Ⅰ.实验室可用下图装置对铜与浓硫酸的反应进行探究。

(1)加热条件下铜与浓硫酸反应的化学方程式
(2)将产生的气体通入品红溶液中的现象
(3)某工厂使用的煤中硫的质量分数为0.64%,该工厂每天燃烧这种煤100 t,如果把产生的SO2全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量为
Ⅱ.实验室制氯气可用下图装置,并进行氯气性质实验。

(4)写出实验室制备氯气的化学方程式:
(5)将氯气通入冷的石灰乳中可制备用于环境消毒的漂白粉,写出此反应的化学方程式
(6)将氯气通入KBr溶液中可发生置换反应,写出反应的离子方程式
您最近一年使用:0次
解题方法
4 . 下列不能 达到“实验目的”的“实验操作及现象”是
| 选项 | 实验目的 | 实验操作及现象 |
| A | 证明浓硫酸有吸水性 | 向蔗糖中滴加浓硫酸,蔗糖变黑 |
| B | 证明SO2具有漂白性 | 向品红溶液中通入SO2,溶液褪色 |
| C | 证明氧化性:Br2>I2 | 向KI和淀粉的混合溶液中滴加溴水,溶液变蓝 |
| D | 检验NH4Cl溶液中的NH | 向NH4Cl溶液中加入浓NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 下列装置不能实现相应实验目的的是( )
A.制取SO2 | B.验证SO2漂白性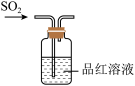 |
C.收集SO2 | D.处理含SO2的尾气 |
您最近一年使用:0次
2019-06-17更新
|
917次组卷
|
10卷引用:山东省2018年夏季普通高中学业水平合格考试化学试题
山东省2018年夏季普通高中学业水平合格考试化学试题【全国百强校】山东省济南市外国语学校三箭分校2018-2019学年高一下学期期中考试化学试题(已下线)2019年12月1日《每日一题》人教版(必修1)—— 每周一测山东省青岛平度市2019-2020学年高一下学期线上阶段测试化学试题江苏省盐城市上冈高级中学2020-2021学年高一上学期第二次学情检测化学试题(已下线)4.3.1 硫及其氧化物(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)人教版2019必修第二册 第五章 第一节 第1课时 硫和二氧化硫河北省张家口宣化一中2020-2021学年高一下学期3月月考化学试题山东省淄博市淄川区般阳中学2020-2021学年高一下学期合格考阶段性推进考试(1)化学试题江苏省邳州市宿羊山高级中学2021-2022学年高一上学期第二次学情检测化学试题
6 . 根据所学相关知识完成下列问题。
Ⅰ.小组Ⅰ用下图装置制取Cl2并探究性质,回答下列问题:

(1)装置①用于制取Cl2,反应的化学方程式是_____
(2)装置②的作用是_____
(3)装置③中的现象是_____
(4)装置④中发生反应的离子方程式是_____
Ⅱ.小组Ⅱ利用如图所示装置探究二氧化硫气体的性质,回答下列问题:
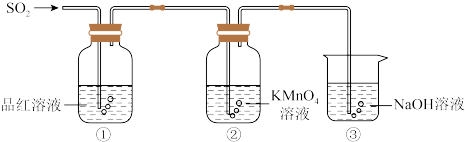
(5)实验室用铜和浓硫酸共热制取二氧化硫,反应的化学方程式是_____
(6)当观察到②中溶液颜色变浅时,①中的现象是_____
(7)装置③的作用是_____
(8)②中的现象说明二氧化硫具有的性质是_____
Ⅲ.小组Ⅲ用图1所示装置制取氨,并探究其性质,回答下列问题:
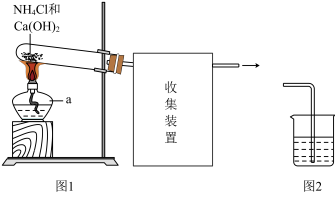
(9)仪器a的名称是_____
(10)图1试管内发生反应的化学方程式是_____
(11)图1方框中的收集装置应为_____ (填图3中字母标号)。
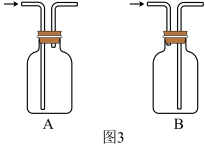
(12)将蘸有浓盐酸的棉球放入收集满NH3的集气瓶中,迅速盖上玻璃片,可观察到的实验现象是_____
(13)甲同学设计了图2所示的装置进行尾气处理,乙同学认为该设计不合理,其理由是_____
Ⅰ.小组Ⅰ用下图装置制取Cl2并探究性质,回答下列问题:

(1)装置①用于制取Cl2,反应的化学方程式是
(2)装置②的作用是
(3)装置③中的现象是
(4)装置④中发生反应的离子方程式是
Ⅱ.小组Ⅱ利用如图所示装置探究二氧化硫气体的性质,回答下列问题:

(5)实验室用铜和浓硫酸共热制取二氧化硫,反应的化学方程式是
(6)当观察到②中溶液颜色变浅时,①中的现象是
(7)装置③的作用是
(8)②中的现象说明二氧化硫具有的性质是
Ⅲ.小组Ⅲ用图1所示装置制取氨,并探究其性质,回答下列问题:

(9)仪器a的名称是
(10)图1试管内发生反应的化学方程式是
(11)图1方框中的收集装置应为

(12)将蘸有浓盐酸的棉球放入收集满NH3的集气瓶中,迅速盖上玻璃片,可观察到的实验现象是
(13)甲同学设计了图2所示的装置进行尾气处理,乙同学认为该设计不合理,其理由是
您最近一年使用:0次
解题方法
7 . 某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。
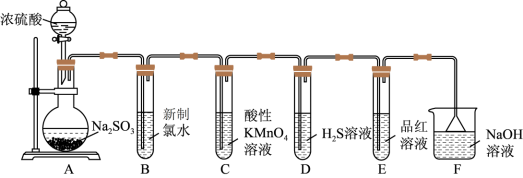
已知: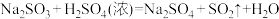 ;请回答下列问题:
;请回答下列问题:
(1)装置A中盛放亚硫酸钠溶液的仪器名称是_______ 。
(2)装置B中发生的离子方程式为_______ 。
(3)以上装置中表现了SO2氧化性的是_______ (填装置字母);
(4)装置F中倒扣漏斗的作用是_______ 。
(5)装置E的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:_______ 。

已知:
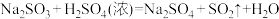 ;请回答下列问题:
;请回答下列问题:(1)装置A中盛放亚硫酸钠溶液的仪器名称是
(2)装置B中发生的离子方程式为
(3)以上装置中表现了SO2氧化性的是
(4)装置F中倒扣漏斗的作用是
(5)装置E的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:
您最近一年使用:0次
8 . 二氧化硫在食品加工中有着重要作用,但过量使用可能导致食品中残留量超标,会对人体健康造成不利影响。实验室可用下图装置制取并探究二氧化硫的性质。回答下列问题:

(1)①中试管内发生反应的化学方程式为_______ ,该反应中体现了浓H2SO4的酸性和_______ 性。在标准状况下生成224 mLSO2时,消耗的H2SO4的物质的量为_______ mol。
(2)实验过程中铜丝可以上下抽动,其作用为_______ 。
(3)②中试管内的溴水褪色,SO2表现出_______ 性,③中试管内的石蕊溶液出现的实验现象为_______ 。
(4)浸有NaOH溶液的棉团的作用为_______ 。

(1)①中试管内发生反应的化学方程式为
(2)实验过程中铜丝可以上下抽动,其作用为
(3)②中试管内的溴水褪色,SO2表现出
(4)浸有NaOH溶液的棉团的作用为
您最近一年使用:0次
9 . SO2可用作漂白剂、食品添加剂等。某兴趣小组用如下装置制取SO2,并验证其性质:

(1)盛放 的仪器名称为
的仪器名称为___________ 。
(2)D装置用于吸收尾气。在答题卡虚线框内画出D装置图,并注明所用试剂___________ 。
(3)进行实验,观察并记录现象,做出相应解释。

(1)盛放
 的仪器名称为
的仪器名称为(2)D装置用于吸收尾气。在答题卡虚线框内画出D装置图,并注明所用试剂
(3)进行实验,观察并记录现象,做出相应解释。
| 实验操作 | 实验现象 | 分析与解释 |
| 打开装置A中的漏斗活塞 | A装置中有气泡产生 | 化学方程式为 |
| B装置中浸润过品红溶液的滤纸a的颜色 |  具有 具有 | |
B装置中浸润过酸性 溶液的滤纸b褪色 溶液的滤纸b褪色 |  具有 具有 | |
| C装置中的现象是 |  具有氧化性 具有氧化性 |
您最近一年使用:0次
解题方法
10 . 某校化学兴趣小组用下图所示装置探究 的性质。请回答:
的性质。请回答:
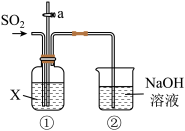
(1)装置②中发生反应的化学方程式是_______ 。
(2)若X为品红溶液,可观察到装置①中溶液_______ ,说明 具有
具有_______ 性。
(3)若X为紫色石蕊溶液,可观察到装置①中溶液_______ ,说明 的水溶液显
的水溶液显_______ (填“酸性”或“碱性”)。
(4)若X为 溶液,可观察到装置①中
溶液,可观察到装置①中_______ (填“有”或“无”)明显现象。打开活塞a,通入氧气,有白色沉淀生成,说明 最终被氧化为
最终被氧化为 ,由此可知
,由此可知 具有
具有_______ (填“氧化性”或“还原性”)。
(5)若X为 溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明
溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明 具有
具有_______ (填“氧化性”或“还原性”)。写出相应的化学方程式:_______ 。
 的性质。请回答:
的性质。请回答:
(1)装置②中发生反应的化学方程式是
(2)若X为品红溶液,可观察到装置①中溶液
 具有
具有(3)若X为紫色石蕊溶液,可观察到装置①中溶液
 的水溶液显
的水溶液显(4)若X为
 溶液,可观察到装置①中
溶液,可观察到装置①中 最终被氧化为
最终被氧化为 ,由此可知
,由此可知 具有
具有(5)若X为
 溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明
溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明 具有
具有
您最近一年使用:0次