1 . 利用如图所示装置进行 的制备和性质探究实验(夹持装置省略)。下列说法不正确的是
的制备和性质探究实验(夹持装置省略)。下列说法不正确的是
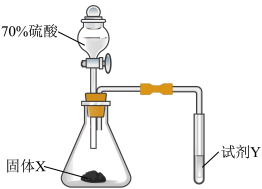
 的制备和性质探究实验(夹持装置省略)。下列说法不正确的是
的制备和性质探究实验(夹持装置省略)。下列说法不正确的是
| A.固体X可为Cu |
| B.若试剂Y为氢硫酸,则试管中可产生淡黄色沉淀 |
C.为证明 具有还原性,试剂Y可为酸性 具有还原性,试剂Y可为酸性 溶液 溶液 |
D.该装置中试管口应塞一团浸有 溶液的棉团 溶液的棉团 |
您最近一年使用:0次
名校
2 . 为探究 的性质,进行了如下实验。
的性质,进行了如下实验。
Ⅰ.在实验室制备 并探究其相关性质,装置如下图所示。
并探究其相关性质,装置如下图所示。 的仪器名称是
的仪器名称是___________ 。
(2)此仪器中发生的化学反应方程式为___________ 。
(3)下列 尾气处理装置不正确的是
尾气处理装置不正确的是___________ 。 具有还原性的是___________(填标号)。
具有还原性的是___________(填标号)。
Ⅱ.有同学提出: 与
与 溶液反应时,溶液中的溶解氧也有可能起到氧化作用。设计如图所示实验装置探究溶液中
溶液反应时,溶液中的溶解氧也有可能起到氧化作用。设计如图所示实验装置探究溶液中 与
与 氧化
氧化 的主导作用:
的主导作用:
0.1 mol/L 溶液、0.1 mol/L
溶液、0.1 mol/L  溶液、0.1 mol/L
溶液、0.1 mol/L  溶液、0.2mol/L
溶液、0.2mol/L  溶液
溶液
③ⅲ、ⅳ两组实验pH变化不同的原因可能是___________ 。
④由上表4个实验可知溶液中 与
与 氧化
氧化 占主导作用的是
占主导作用的是___________ (填“ ”或“
”或“ ”)。
”)。
(6)写出在有氧气的条件下, 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
 的性质,进行了如下实验。
的性质,进行了如下实验。Ⅰ.在实验室制备
 并探究其相关性质,装置如下图所示。
并探究其相关性质,装置如下图所示。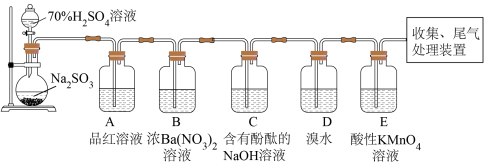
 的仪器名称是
的仪器名称是(2)此仪器中发生的化学反应方程式为
(3)下列
 尾气处理装置不正确的是
尾气处理装置不正确的是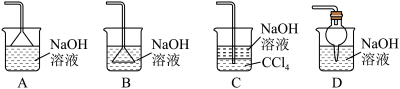
 具有还原性的是___________(填标号)。
具有还原性的是___________(填标号)。| A.品红溶液 | B.含有酚酞的NaOH溶液 |
| C.溴水 | D.酸性 溶液 溶液 |
Ⅱ.有同学提出:
 与
与 溶液反应时,溶液中的溶解氧也有可能起到氧化作用。设计如图所示实验装置探究溶液中
溶液反应时,溶液中的溶解氧也有可能起到氧化作用。设计如图所示实验装置探究溶液中 与
与 氧化
氧化 的主导作用:
的主导作用: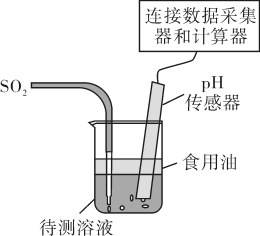
0.1 mol/L
 溶液、0.1 mol/L
溶液、0.1 mol/L  溶液、0.1 mol/L
溶液、0.1 mol/L  溶液、0.2mol/L
溶液、0.2mol/L  溶液
溶液| 步骤操作 | pH变化 | |
| ⅰ | 取25 mL煮沸过的0.1 mol·L  溶液,通入V mL 溶液,通入V mL  | pH轻微减小 |
| ⅱ | 取25 mL未煮沸的① | pH减小2.5 |
| ⅲ | 取25 mL煮沸过的0.1 mol·L  溶液,通入V mL 溶液,通入V mL  | pH几乎不变 |
| ⅳ | 取25 mL未煮沸的② | pH减小2 |
④由上表4个实验可知溶液中
 与
与 氧化
氧化 占主导作用的是
占主导作用的是 ”或“
”或“ ”)。
”)。(6)写出在有氧气的条件下,
 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:
您最近一年使用:0次
2024-05-30更新
|
193次组卷
|
3卷引用:2024届天津市河东区高三下学期二模化学试题
解题方法
3 . 利用下列装置进行实验,不能达到实验目的的是
|
|
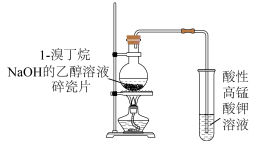
A.验证 氧化性 氧化性 | B.验证1-溴丁烷的消去反应 |
|
|
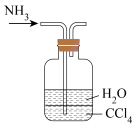
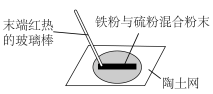
| C.制氨水 | D.证明Fe与S反应放热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 下列实验方案与实验目的不匹配的是
| 选项 | 实验目的 | 实验方案 |
| A | 探究 既有氧化性又有还原性 既有氧化性又有还原性 | 将 分别通入溴水和 分别通入溴水和 溶液 溶液 |
| B | 证明甲苯中甲基能活化苯环 | 将酸性 溶液分别加入苯和甲苯中并振荡 溶液分别加入苯和甲苯中并振荡 |
| C | 比较 水解程度和电离程度大小 水解程度和电离程度大小 | 常温下,用pH试纸测一定浓度 溶液的pH 溶液的pH |
| D | 除去乙酸乙酯中的乙酸和乙醇 | 用饱和 溶液洗涤后分液 溶液洗涤后分液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 下列实验方案设计中,操作现象都正确且能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
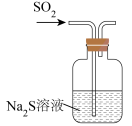
| A | 证明:H2SO3的酸性大于H2S | 向Na2S溶液中缓缓通入过量SO2,观察到大量臭鸡蛋气味气体逸出 |
| B | 证明:Fe比Cu活泼 | Cu片插入稀硫酸无气泡,Fe片和Cu片用导线连接后插入稀硫酸中,铜片表面产生气泡 |
| C | 证明:K2Cr2O7溶液中存在下列平衡Cr2O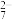 +H2O +H2O 2CrO 2CrO +2H+ +2H+ | 将K2Cr2O7固体溶于水后,加入浓盐酸,观察到溶液 橙色加深 |
| D | 证明:硫酸能否将Fe2+氧化为Fe3+ | 将Fe(NO3)2样品溶于稀硫酸,滴加KSCN溶液,观 察到溶液变红 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-23更新
|
674次组卷
|
3卷引用:四川省泸州市2021-2022学年高三第一次教学质量诊断性考试理科综合化学试题
四川省泸州市2021-2022学年高三第一次教学质量诊断性考试理科综合化学试题甘肃省张掖市高台县第一中学2022-2023学年高三上学期开学第一次检测化学试题(已下线)第29讲 化学综合实验(讲)-2023年高考化学一轮复习讲练测(全国通用)
6 . 某兴趣小组设计实验探究SO2与新制Cu(OH)2悬浊液反应的产物。

按图连接好装置(夹持装置省略),打开磁搅拌器,先往CuCl2溶液中加入NaOH溶液至恰好完全反应,再通入过量的SO2,三颈烧瓶中生成大量白色沉淀X。
(1)制取SO2最适宜的试剂是___________ 。
A.Na2SO3固体与20%的硝酸B.Na2SO3固体与20%的硫酸
C.Na2SO3固体与70%的硫酸D.Na2SO3固体与18.4mol·L-1的硫酸
(2)根据选定的试剂,虚框中应选用___________ (填“A”或“B”)装置;通入SO2过程中不断用磁搅拌器搅拌的目的是___________ 。
(3)甲同学推测X可能为CuSO3.他取出少量洗涤后的X加入足量稀硫酸进行实验验证,观察到___________ ,则甲同学推测错误。
(4)乙同学查阅资料:CuCl为白色固体,难溶于水,能溶于浓盐酸形成CuCl ;与氨水反应生成Cu(NH3)
;与氨水反应生成Cu(NH3)  ,在空气中会立即被氧化成深蓝色Cu(NH3)
,在空气中会立即被氧化成深蓝色Cu(NH3) 溶液。据此推测X可能为CuCl。他取出少量洗涤后的白色沉淀X,加入浓盐酸,沉淀溶解,加水稀释,又出现白色沉淀,据此得出乙同学推测正确。
溶液。据此推测X可能为CuCl。他取出少量洗涤后的白色沉淀X,加入浓盐酸,沉淀溶解,加水稀释,又出现白色沉淀,据此得出乙同学推测正确。
①从平衡角度解释加水稀释重新产生白色沉淀的原因___________ 。
②请再设计一种证明该白色沉淀为CuCl的方案:___________ 。
③三颈烧瓶中生成CuCl的离子方程式为:___________ 。

按图连接好装置(夹持装置省略),打开磁搅拌器,先往CuCl2溶液中加入NaOH溶液至恰好完全反应,再通入过量的SO2,三颈烧瓶中生成大量白色沉淀X。
(1)制取SO2最适宜的试剂是
A.Na2SO3固体与20%的硝酸B.Na2SO3固体与20%的硫酸
C.Na2SO3固体与70%的硫酸D.Na2SO3固体与18.4mol·L-1的硫酸
(2)根据选定的试剂,虚框中应选用
(3)甲同学推测X可能为CuSO3.他取出少量洗涤后的X加入足量稀硫酸进行实验验证,观察到
(4)乙同学查阅资料:CuCl为白色固体,难溶于水,能溶于浓盐酸形成CuCl
 ;与氨水反应生成Cu(NH3)
;与氨水反应生成Cu(NH3)  ,在空气中会立即被氧化成深蓝色Cu(NH3)
,在空气中会立即被氧化成深蓝色Cu(NH3) 溶液。据此推测X可能为CuCl。他取出少量洗涤后的白色沉淀X,加入浓盐酸,沉淀溶解,加水稀释,又出现白色沉淀,据此得出乙同学推测正确。
溶液。据此推测X可能为CuCl。他取出少量洗涤后的白色沉淀X,加入浓盐酸,沉淀溶解,加水稀释,又出现白色沉淀,据此得出乙同学推测正确。①从平衡角度解释加水稀释重新产生白色沉淀的原因
②请再设计一种证明该白色沉淀为CuCl的方案:
③三颈烧瓶中生成CuCl的离子方程式为:
您最近一年使用:0次
解题方法
7 . 下列实验操作规范且能达到目的的是
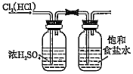 | 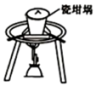 |  | 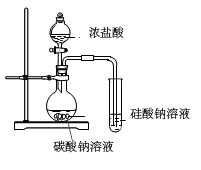 |
| 收集干燥纯净的氯气 | 熔融 固体 固体 | 验证 的氧化性 的氧化性 | 证明盐酸 碳酸 碳酸 硅酸的酸性 硅酸的酸性 |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下列有关实验操作或事实与相应现象或结论均正确的是( )
| 选项 | 操作或事实 | 现象或结论 |
| A | SO2和SO3混合气体通入足量的Ba(NO3)2溶液 | 产生白色沉淀,白色沉淀为BaSO3和BaSO4的混合物 |
| B | 将醋酸加入到含有水垢的水壶中 | 产生气泡,水垢脱落,可用醋酸清洗掉水垢 |
| C | 向水玻璃中通入SO2气体 | 溶液出现浑浊,证明非金属性:Si<S |
| D | 向待测液中加入适量的稀NaOH溶液,将湿润的蓝色石蕊试纸放在试管口 | 湿润的蓝色石蕊试纸未变红,则待测液中不存在NH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 对于下图所示实验,不能 达到实验目的的是

| A.实验甲:验证SO2的氧化性 |
| B.实验乙:曲MgCl2·6H2O制备无水MgCl2 |
| C.实验丙:比较KMnO4、Cl2、S的氧化性强弱 |
| D.实验丁:证明浓硫酸的吸水性、脱水性和强氧化性 |
您最近一年使用:0次
2021-01-23更新
|
86次组卷
|
2卷引用:安徽省县中联盟2023-2024学年高三下学期(三模)联考化学试题
2010·上海·零模
解题方法
10 . 在2008年初我国南方曾遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且lmolXY2含有54mol电子。
(1)用元素符号将X、Y两元素填写在下面元素周期表中所对应的位置。_________________
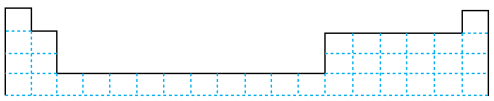
(2)X元素原子核外共有______ 种不同能量的电子。Y与氢元素形成的化合物的电子式是______________ 。
(3)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,写出D离子的核外电子排布式_____________________ ;D与E能形成一种化学式为ED2的分子,该分子是______________ 分子(填“极性”“非极性”),结构式为___________ ;D所在族元素的氢化物中,沸点最低的是______________ (写元素氢化物的化学式)。写出该氢化物与该元素的某种氧化物反应的化学方程式__________________ 。
(4)D、Y两元素哪种非金属性较强?________ 写出证明这一结论的一个实验事实:____
(1)用元素符号将X、Y两元素填写在下面元素周期表中所对应的位置。

(2)X元素原子核外共有
(3)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,写出D离子的核外电子排布式
(4)D、Y两元素哪种非金属性较强?
您最近一年使用:0次