11-12高一上·浙江温州·期末
1 . 含硫化合物的种类很多,现有H2SO4、H2SO3、SO2、Na2SO3、BaSO4、CuSO4、Na2SO4这7种常见的含硫化合物。回答下列问题:
(1)H2SO3转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式,并标明电子转移方向和数目:_________________________________ 。
(2)Ba2+有剧毒。某市曾发生一起“毒烧饼”事件,起因是烧饼摊主在制作烧饼的过程中误将碳酸钡当作干粉使用,导致多人食用烧饼后中毒。试写出碳酸钡与胃酸(以盐酸表示)反应的离子反应方程式______________________________ 。
(3)常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面____________ ,则发生了钝化;若铁棒表面________________ ,则未发生反应。
(4)用Na2SO3吸收法作为治理SO2污染的一种方法,其原理为(用化学方程式表示):______________________________ 。
(5)减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2。该反应的化学方程式:____________________________ 。
(6)制取硫酸铜有两种方法:方法一:2Cu+O2 2CuO,CuO+ H2SO4= CuSO4+H2O,
2CuO,CuO+ H2SO4= CuSO4+H2O,
方法二:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:
CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:_____________________________________________ (答任一点)。
(1)H2SO3转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式,并标明电子转移方向和数目:
(2)Ba2+有剧毒。某市曾发生一起“毒烧饼”事件,起因是烧饼摊主在制作烧饼的过程中误将碳酸钡当作干粉使用,导致多人食用烧饼后中毒。试写出碳酸钡与胃酸(以盐酸表示)反应的离子反应方程式
(3)常温下,将铁棒置于浓硫酸中,无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面
(4)用Na2SO3吸收法作为治理SO2污染的一种方法,其原理为(用化学方程式表示):
(5)减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2。该反应的化学方程式:
(6)制取硫酸铜有两种方法:方法一:2Cu+O2
 2CuO,CuO+ H2SO4= CuSO4+H2O,
2CuO,CuO+ H2SO4= CuSO4+H2O,方法二:Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:
CuSO4+SO2↑+2H2O,方法一与方法二相比,其优点是:
您最近半年使用:0次
2 . 向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀总物质的量和加入溶液B的体积关系如图所示:
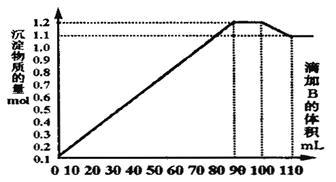
(1)当加入B溶液110 mL时,溶液中的沉淀是_______ (填化学式)
(2)将A.B溶液中各溶质的物质的量浓度填入表中:
(3)写出滴加B溶液90-100mL时的离子方程式:_______ 。

(1)当加入B溶液110 mL时,溶液中的沉淀是
(2)将A.B溶液中各溶质的物质的量浓度填入表中:
| 溶 质 | Na2SO4 | BaCl2 | AlCl3 | FeCl3 |
| /mol·L-1 |
(3)写出滴加B溶液90-100mL时的离子方程式:
您最近半年使用:0次
3 . 现有下列四种物质:① SO2、② NO、③ Na2SO4溶液、④ AlCl3溶液。其中,遇空气变为红棕色的是_______ (填序号,下同),能使品红溶液褪色的是_______ ,加入氯化钡溶液产生白色沉淀的是_______ ,逐滴加入氢氧化钠溶液,先产生白色沉淀,后沉淀溶解的是_______ 。
您最近半年使用:0次
4 . 向100mL 0.1mol/L H2SO4溶液中,逐滴加入0.1mol/L Ba(OH)2溶液至过量,下列图象正确的是
A.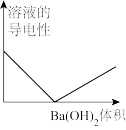 | B. |
C.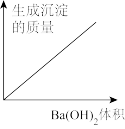 | D.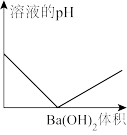 |
您最近半年使用:0次
5 . 重晶石矿的主要成分为硫酸钡,纯净的硫酸钡才能供医用作“钡餐”,在对某些内脏器官进行X 射线透视时服用。硫化钡是可溶于水的盐。讨论用重晶石矿制硫酸钡,设计流程如下:
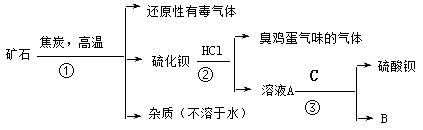
(1)写出步骤①的化学反应方程式___________ ,该反应产生的气体具有____ 、_____ 等用途。
(2)为进行②反应先要分离出硫化钡溶液,采用的方法是__________ 。在此之前要在溶液中滴入少量Ba(OH)2溶液,其作用是___________ 。
(3)若B物质在该生产过程中可循环使用,则③反应的化学方程式是:___________ 。
(4)有人提出②反应产生了有臭有毒的气体,可采用改变反应物的方法使无该气体产生,则②反应的化学方程式是:__________________________ 。
此时若要B物质还能循环使用,则C为__________ (写化学式)。
(5)BaSO4是因为具有_________ 、_________ 等性质而可用作“钡餐”的。

(1)写出步骤①的化学反应方程式
(2)为进行②反应先要分离出硫化钡溶液,采用的方法是
(3)若B物质在该生产过程中可循环使用,则③反应的化学方程式是:
(4)有人提出②反应产生了有臭有毒的气体,可采用改变反应物的方法使无该气体产生,则②反应的化学方程式是:
此时若要B物质还能循环使用,则C为
(5)BaSO4是因为具有
您最近半年使用:0次



