名校
解题方法
1 . 向含有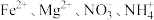 的溶液中先加入过量金属钠,有气体和沉淀生成,然后再加入过量的稀硝酸使沉淀溶解,最终离子数一定不变的是
的溶液中先加入过量金属钠,有气体和沉淀生成,然后再加入过量的稀硝酸使沉淀溶解,最终离子数一定不变的是
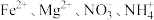 的溶液中先加入过量金属钠,有气体和沉淀生成,然后再加入过量的稀硝酸使沉淀溶解,最终离子数一定不变的是
的溶液中先加入过量金属钠,有气体和沉淀生成,然后再加入过量的稀硝酸使沉淀溶解,最终离子数一定不变的是A. | B. | C. | D. |
您最近一年使用:0次
名校
2 . 化学与生产、生活息息相关,下列说法错误的是
| A.氯气泄露时,人群要向地势高的地方疏散 |
| B.服用维生素C以保证亚铁补血剂的吸收效果 |
| C.高铁酸钠(Na2FeO4)用于自来水的杀菌、消毒 |
| D.钠着火时,应及时用水扑灭,防止造成其他损失 |
您最近一年使用:0次
名校
解题方法
3 . 下列表示对应化学反应的离子方程式正确的是
| A.Cl2通入氢氧化钠溶液:Cl2 + 2OH- = Cl- + ClO- + H2O |
| B.Na与水的反应离子方程式:2Na + 2H+=2Na+ + H2↑ |
| C.Na2O2与水反应: Na2O2 + 2H2O=2Na+ + 2OH-+ O2↑ |
| D.向CaCl2溶液中通入CO2:Ca2+ + H2O + CO2 = CaCO3 + 2H+ |
您最近一年使用:0次
解题方法
4 . 某小组想通过实验探究 Na、Mg、Al 三种金属元素性质的递变规律。
I.探究 Na、Mg、Al 分别与水反应的情况。
实验①:切一小块绿豆大小的金属 Na,用滤纸吸干其表面的煤油,将其投入盛有 100ml 水(含酚酞)的烧杯中。观察到 Na 与冷水发生剧烈反应,烧杯内溶液变红。
(1)与水反应生成氢氧化钠和氢气,写出该反应的化学方程式___________ 。
(2)上述反应中,作还原剂的是___________ 。
A.Na B.H2O C.NaOH
(3)上述反应中若有23克金属Na被充分反应,则产生气体在标况下的体积约为___________ L。
(4)溶液中,使酚酞试液变红的微粒是___________ 。
A.Na+ B.H+ C.OH-
实验②:分别取一小段镁条和铝条,放入两支试管中,向试管中各加入 2ml 水,再滴入2 滴酚酞试液,观察到试管中均无明显现象。
有同学提出实验②的设计存在问题,故对实验②作如下调整:
实验③:另取镁条和铝条,分别用砂纸打磨去除它们表面的氧化膜后,再进行以上实验 操作并加热。观察到:未加热时,反应现象均不明显;加热后镁条表面有气泡生成,溶液变红;加热后 Al 与水反应现象仍不明显。
(5)实验②的设计中未考虑到的因素是___________ 。
(6)通过上述实验,得出 Na、Mg、Al 的金属性由强到弱的顺序是___________ 。
Ⅱ.比较 NaOH、Mg(OH)2、Al(OH)3碱性的强弱。
实验④:在试管中加入2ml 0.5mol·L-1 Al2(SO4)3溶液,然后逐滴滴加 2mol·L-1 NaOH溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
实验⑤:在试管中加入2ml 1mol·L-1 MgSO4溶液,然后逐滴滴加2mol·L-1 NaOH 溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
(7)写出由实验④、⑤的实验现象可推导得出的结论。
(8)综上实验可知,NaOH、Mg(OH)2、Al(OH)3的碱性由强到弱的顺序是___________ 。
I.探究 Na、Mg、Al 分别与水反应的情况。
实验①:切一小块绿豆大小的金属 Na,用滤纸吸干其表面的煤油,将其投入盛有 100ml 水(含酚酞)的烧杯中。观察到 Na 与冷水发生剧烈反应,烧杯内溶液变红。
(1)与水反应生成氢氧化钠和氢气,写出该反应的化学方程式
(2)上述反应中,作还原剂的是
A.Na B.H2O C.NaOH
(3)上述反应中若有23克金属Na被充分反应,则产生气体在标况下的体积约为
(4)溶液中,使酚酞试液变红的微粒是
A.Na+ B.H+ C.OH-
实验②:分别取一小段镁条和铝条,放入两支试管中,向试管中各加入 2ml 水,再滴入2 滴酚酞试液,观察到试管中均无明显现象。
有同学提出实验②的设计存在问题,故对实验②作如下调整:
实验③:另取镁条和铝条,分别用砂纸打磨去除它们表面的氧化膜后,再进行以上实验 操作并加热。观察到:未加热时,反应现象均不明显;加热后镁条表面有气泡生成,溶液变红;加热后 Al 与水反应现象仍不明显。
(5)实验②的设计中未考虑到的因素是
(6)通过上述实验,得出 Na、Mg、Al 的金属性由强到弱的顺序是
Ⅱ.比较 NaOH、Mg(OH)2、Al(OH)3碱性的强弱。
实验④:在试管中加入2ml 0.5mol·L-1 Al2(SO4)3溶液,然后逐滴滴加 2mol·L-1 NaOH溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
实验⑤:在试管中加入2ml 1mol·L-1 MgSO4溶液,然后逐滴滴加2mol·L-1 NaOH 溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
(7)写出由实验④、⑤的实验现象可推导得出的结论。
| 现象 | 结论 | |
| ④ | 出现白色沉淀 | Al(OH)3的碱性比NaOH弱 |
| 沉淀全部溶解 | ||
| ⑤ | 出现白色沉淀 | |
| 沉淀不溶解 | Mg(OH)2无酸性 |
您最近一年使用:0次
名校
5 . 下列关于钠及其化合物的说法正确的是
| A.钠钾合金在室温下呈液态,可用作核反应堆的传热介质 |
B.将金属钠放入 溶液中,可观察到大量红色的铜析出 溶液中,可观察到大量红色的铜析出 |
| C.配制一定物质的量浓度的氢氧化钠溶液时,将氢氧化钠固体溶解后立即转移至容量瓶中定容 |
D. 与 与 都能和水反应生成碱,故两者均为碱性氧化物 都能和水反应生成碱,故两者均为碱性氧化物 |
您最近一年使用:0次
名校
解题方法
6 . 如图中, 为一种常见的单质,
为一种常见的单质, 是含有
是含有 元素的常见化合物。它们的焰色试验均为黄色。下列叙述不正确的是
元素的常见化合物。它们的焰色试验均为黄色。下列叙述不正确的是

 为一种常见的单质,
为一种常见的单质, 是含有
是含有 元素的常见化合物。它们的焰色试验均为黄色。下列叙述不正确的是
元素的常见化合物。它们的焰色试验均为黄色。下列叙述不正确的是
| A.以上反应中属于氧化还原反应的有①②③④ |
| B.B、C、D分别属于碱性氧化物、碱、盐 |
C. 与 与 反应的离子方程式为 反应的离子方程式为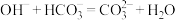 |
| D.等量的钠分别与足量氧气在常温和加热条件下反应,两个反应转移的电子数一样多 |
您最近一年使用:0次
名校
7 . 下列反应的离子方程式正确的是
A.金属钠与 反应: 反应: |
B. 溶液与 溶液与 反应: 反应: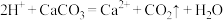 |
C.向 溶液中加入少量 溶液中加入少量 溶液: 溶液: |
D.铜与稀硫酸反应: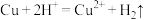 |
您最近一年使用:0次
名校
8 . 下列关于 说法不正确的是
说法不正确的是
 说法不正确的是
说法不正确的是A. 钠与 钠与 盐酸反应,转移的电子数为 盐酸反应,转移的电子数为 |
B. 的 的 参与反应转移的电子数一定为 参与反应转移的电子数一定为 |
C.常温常压下, 和 和 的混合气体 的混合气体 含有的原子数为 含有的原子数为 |
D.将 通入水中, 通入水中,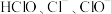 粒子数之和小于 粒子数之和小于 |
您最近一年使用:0次
名校
解题方法
9 . 现有 七种物质,它们之间能发生如下反应(图中部分反应物、产物及反应条件未标出)。请根据以上信息回答下列问题:
七种物质,它们之间能发生如下反应(图中部分反应物、产物及反应条件未标出)。请根据以上信息回答下列问题:
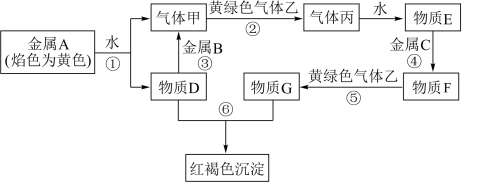
(1)A物质在空气中燃烧的产物是__________ 色的粉末,写出该物质与 反应的化学方程式
反应的化学方程式__________ 。
(2)写出反应③和反应⑤的离子反应方式:__________ 、__________ 。
(3)向物质F的水溶液中加入 溶液,现象为
溶液,现象为__________ ,写出上述过程发生的氧化还原反应反应的化学方程式__________ 。
 七种物质,它们之间能发生如下反应(图中部分反应物、产物及反应条件未标出)。请根据以上信息回答下列问题:
七种物质,它们之间能发生如下反应(图中部分反应物、产物及反应条件未标出)。请根据以上信息回答下列问题:
(1)A物质在空气中燃烧的产物是
 反应的化学方程式
反应的化学方程式(2)写出反应③和反应⑤的离子反应方式:
(3)向物质F的水溶液中加入
 溶液,现象为
溶液,现象为
您最近一年使用:0次
名校
10 . 已知Fe(OH)3为红褐色、难溶于水的物质。下列关于钠的反应现象的叙述不正确 的是
| 选项 | 操作 | 反应现象 |
| A | 切开钠,持续观察颜色变化 | 钠切面颜色先变暗,最后呈淡黄色 |
| B | 把小块钠投入硫酸铁溶液中 | 钠浮在水面上四处游动,产生红褐色沉淀 |
| C | 把小块钠投入饱和氢氧化钠溶液中 | 钠浮在水面上四处游动,产生白色浑浊 |
| D | 把钠放入坩埚中加热 | 钠先熔化后燃烧,产生黄色火焰 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



