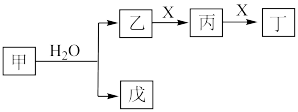
1 . I.某些常见无机物质存在如图的化学转化关系(部分生成物和反应条件略去),回答下列问题:________ 。
(2)若甲是一种淡黄色固体,丙是一种温室气体,则X的化学式为________ ,当 甲和水生成乙和戊时,反应转移电子的物质的量为
甲和水生成乙和戊时,反应转移电子的物质的量为________ 。
(3)若甲是由两种常见的元素组成的化合物,乙是气体且水溶液呈碱性,X为大气中的一种主要成分,写出丁与水反应的化学方程式________ 。戊是氢氧化物,既能和强酸反应又能和强碱反应,则甲的化学式为________ 。
Ⅱ.固体化合物X由3种元素组成,其转化关系如图,混合气体经过无水 时,固体变蓝,碱性溶液焰色反应为黄色。回答下列问题:
时,固体变蓝,碱性溶液焰色反应为黄色。回答下列问题:____________ 。
(5)X的化学式为________ ,X能和浓盐酸反应生成黄绿色气体,X在反应中作________ (填“氧化剂”或“还原剂”),若反应了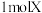 ,该反应转移电子的个数为
,该反应转移电子的个数为________ 。
(2)若甲是一种淡黄色固体,丙是一种温室气体,则X的化学式为
 甲和水生成乙和戊时,反应转移电子的物质的量为
甲和水生成乙和戊时,反应转移电子的物质的量为(3)若甲是由两种常见的元素组成的化合物,乙是气体且水溶液呈碱性,X为大气中的一种主要成分,写出丁与水反应的化学方程式
Ⅱ.固体化合物X由3种元素组成,其转化关系如图,混合气体经过无水
 时,固体变蓝,碱性溶液焰色反应为黄色。回答下列问题:
时,固体变蓝,碱性溶液焰色反应为黄色。回答下列问题: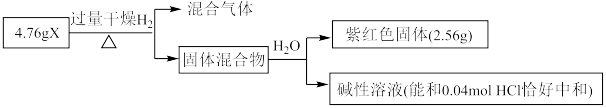
(5)X的化学式为
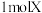 ,该反应转移电子的个数为
,该反应转移电子的个数为
您最近一年使用:0次
2 . A是一种常见的金属单质,B、C、D、E是含有A元素的常见化合物。转化关系如图所示:

回答下列问题:
(1)上述①~⑦反应中,A元素化合价发生变化的有________ (填标号)。
(2)E的化学式为________ ,写出该物质的一种用途________ 。
(3)反应②的化学反应方程式为________ ;
(4)反应③的离子方程式为________ ;
(5)反应⑥的化学方程式为________ 。

回答下列问题:
(1)上述①~⑦反应中,A元素化合价发生变化的有
(2)E的化学式为
(3)反应②的化学反应方程式为
(4)反应③的离子方程式为
(5)反应⑥的化学方程式为
您最近一年使用:0次
解题方法
3 . 下列反应的离子方程式正确的是
A.钠放入水中: |
B.过氧化钠放入水中: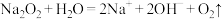 |
C.腐蚀印刷铜电路板: |
D. 通入水中: 通入水中: |
您最近一年使用:0次
解题方法
4 . 下列操作规范但不能达到实验目的的是
|
|
|
|
A.用过氧化氢在MnO2催化作用下制取O2 | B.除去 | C.验证溶液X中存在 | D.验证有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 下列关于钠及其化合物的说法错误的是
| A.钠、过氧化钠及氢氧化钠长时间露置于空气中最终都会变成Na2CO3 |
| B.钠在空气中燃烧,发出黄色火焰,生成白色固体 |
| C.可用水来检验某Na2O样品中是否含有Na2O2 |
| D.向碳酸钠溶液中滴加少量酚酞试液,溶液变为红色 |
您最近一年使用:0次
6 . 下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 陈述Ⅲ |
| A | 小苏打可用于治疗胃酸过多 | Na2CO3可与盐酸反应 | Ⅰ对,Ⅱ对,有 |
| B | 将过氧化钠加入石蕊溶液中,溶液先变蓝后褪色 | 过氧化钠与水反应生成氢氧化钠和漂白性物质 | Ⅰ对,Ⅱ对,有 |
| C | 明矾可用于净水 | 明矾溶于水后,生成具有很大表面积的氢氧化铝胶体微粒 | Ⅰ对,Ⅱ对,有 |
| D | 金属钠保存在煤油中以隔绝空气 | 常温下,金属钠在空气中生成过氧化钠 | Ⅰ对,Ⅱ对,有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 化学物质丰富多彩,化学反应千变万化,而常见物质之间的反应往往“隐藏着某些反应机理”。学校化学兴趣小组探究Na2O2与H2O的反应,实验如下:
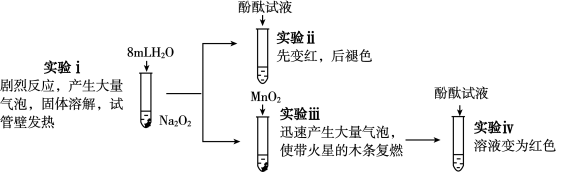
下列有关说法不正确的是

下列有关说法不正确的是
| A.实验i中发生反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑ |
| B.实验iii中MnO2做H2O2分解反应的催化剂 |
| C.本实验可以说明Na2O2与H2O反应有H2O2生成 |
| D.本实验可以说明使酚酞试液褪色的是O2 |
您最近一年使用:0次
8 . 根据如图所示的转化关系推断各物质,已知A为淡黄色A体,B和C为气体,E医疗上治疗胃酸过多的一种药剂,H为单质,请问答下列问题:
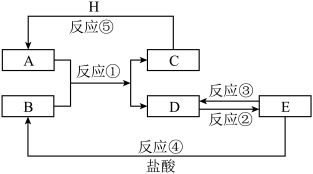
(1)请写出物质的化学式:A___________ ,A中阴阳离子个数比为___________ 。
(2)反应①的化学方程式为_______________ ,反应④的离子方程式为___________________________ 。
(3)D溶液中含有少量的E,可采用的除杂方法为_____________________ (用离子化学方程式表示)。
(4)请设计实验鉴别D溶液和E溶液:______________________ 。
(5)取一定质量的D和E混合物为烧至恒重,冷却至室温,共收集到4.4g气体。加热后剩余的固体物质与足量盐酸反应,共收集到8.8g气体,则原固体混合物中D的质量为___________ 。

(1)请写出物质的化学式:A
(2)反应①的化学方程式为
(3)D溶液中含有少量的E,可采用的除杂方法为
(4)请设计实验鉴别D溶液和E溶液:
(5)取一定质量的D和E混合物为烧至恒重,冷却至室温,共收集到4.4g气体。加热后剩余的固体物质与足量盐酸反应,共收集到8.8g气体,则原固体混合物中D的质量为
您最近一年使用:0次
名校
9 . 化学物质丰富多彩,化学反应千变万化,而常见物质之间的反应往往“隐藏着某些反应机理”。学校化学兴趣小组对含钠元素物质的某些反应进行了初步探究。
I.该小组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”。

步骤1:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,观察实验现象。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,观察实验现象。
步骤2:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,观察实验现象。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,观察实验现象。
请回答下列问题:
(1)装置②中盛放的试剂及作用是_________ 。
(2)本实验预期现象是_________ 。
(3)有同学提出质疑,认为上述实验即使观察到木条复燃,也不能证明有水存在时,是过氧化钠与二氧化碳发生了化学反应,其理由是_________ 。
II.本小组还进一步探究了 与
与 的反应,实验如下:
的反应,实验如下:

(4)由该实验现象,可推知过氧化钠加入水的过程中发生的化学反应有_________ 。
III.向300 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的(忽略溶液体积的变化),
溶液中缓慢通入一定量的(忽略溶液体积的变化),
充分反应后,向上述所得溶液中,逐滴滴加1 的盐酸。本小组将所得气体的体积与所加盐酸的体积关系绘制图像如下图所示,回答下列问题:
的盐酸。本小组将所得气体的体积与所加盐酸的体积关系绘制图像如下图所示,回答下列问题:

(5)①向氢氧化钠溶液中通入 后的溶质及物质的量之比为
后的溶质及物质的量之比为_________ 。
②B点时,反应所得溶液中溶质的物质的量浓度是_________ 。
I.该小组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”。

步骤1:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,观察实验现象。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,观察实验现象。步骤2:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,观察实验现象。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,观察实验现象。请回答下列问题:
(1)装置②中盛放的试剂及作用是
(2)本实验预期现象是
(3)有同学提出质疑,认为上述实验即使观察到木条复燃,也不能证明有水存在时,是过氧化钠与二氧化碳发生了化学反应,其理由是
II.本小组还进一步探究了
 与
与 的反应,实验如下:
的反应,实验如下:
(4)由该实验现象,可推知过氧化钠加入水的过程中发生的化学反应有
III.向300
 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的(忽略溶液体积的变化),
溶液中缓慢通入一定量的(忽略溶液体积的变化),充分反应后,向上述所得溶液中,逐滴滴加1
 的盐酸。本小组将所得气体的体积与所加盐酸的体积关系绘制图像如下图所示,回答下列问题:
的盐酸。本小组将所得气体的体积与所加盐酸的体积关系绘制图像如下图所示,回答下列问题:
(5)①向氢氧化钠溶液中通入
 后的溶质及物质的量之比为
后的溶质及物质的量之比为②B点时,反应所得溶液中溶质的物质的量浓度是
您最近一年使用:0次
名校
10 . 学习小组探究 与水反应。取
与水反应。取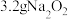 粉末加入到
粉末加入到 水中,充分反应得溶液A(溶液体积几乎无变化),进行以下实验。
水中,充分反应得溶液A(溶液体积几乎无变化),进行以下实验。
 与水反应。取
与水反应。取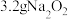 粉末加入到
粉末加入到 水中,充分反应得溶液A(溶液体积几乎无变化),进行以下实验。
水中,充分反应得溶液A(溶液体积几乎无变化),进行以下实验。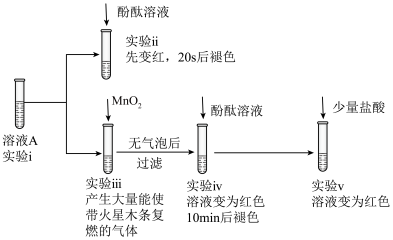
A.由实验ⅰ、ⅲ中现象可推知, 中加 中加 发生反应: 发生反应: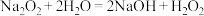 |
B.由实验ⅱ、ⅲ、iv可知,实验ⅱ中溶液褪色与 有关 有关 |
C.由实验ⅵ、ⅴ可知,实验ⅵ中溶液褪色的原因是 较大 较大 |
| D.向褪色后的实验ⅱ溶液中,滴加少量的盐酸,溶液最终变成红色 |
您最近一年使用:0次
2024-01-05更新
|
136次组卷
|
3卷引用:山东省滨州市邹平市第一中学2023-2024学年高一上学期11月期中考试化学试题







 生成
生成

