名校
解题方法
1 . 由我国自主研发的“奋斗者号潜水艇在大平洋马里亚纳海沟成功坐底,创造了中国载人深潜的新纪录。

(1)过氧化钠可用作潜水艇的供氧剂,写出Na2O2和CO2反应的化学方程式:______________ ,该反应中生成1 mol O2转移的电子数为____________ 。
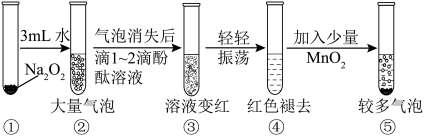
(2)某实验小组通过如图所示实验,探究Na2O2与水的反应,下列说法正确的是_______。 (双选)

(1)过氧化钠可用作潜水艇的供氧剂,写出Na2O2和CO2反应的化学方程式:
(2)某实验小组通过如图所示实验,探究Na2O2与水的反应,下列说法正确的是_______。 (双选)

| A.②中的大量气泡主要成分是氢气 |
| B.③中溶液变红,说明有酸性物质生成 |
| C.④中现象可能是由于溶液中含有强氧化性物质造成的 |
| D.⑤中MnO2的主要作用是验证溶液中存在过氧化氢 |
您最近一年使用:0次
名校
解题方法
2 . 把等物质的量的碳酸氢钠和过氧化钠放在密闭容器中加热,完全反应后排出气体。剩余固体的成分包括________ ,其物质的量之比为________ 。若排出的气体的质量为1.6克,则原混合固体的质量为_______ 克。
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,观察到的现象是_______。
(2)钠在空气中燃烧可制得过氧化钠,过氧化钠的用途之一便是在呼吸面具中做供氧剂,用化学语言(反应方程式)来说明其原理:(提示:人呼出的气体中含有CO2和水蒸气)_______ 。
(3)某实验小组通过以下实验来比较Na2CO3和NaHCO3两种物质的性质。称取两种固体各2g,分别放入两个小烧杯中,再各滴加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴加2滴酚酞试液。
①a烧杯中固体完全溶解,而b烧杯固体有剩余,b烧杯内的物质是_______ 。
②同学们在两烧杯中还观察到了其它现象,其中a烧杯中出现的现象:Ⅰ溶液温度_______ (填“升高”或“降低”),Ⅱ滴加酚酞试液显_______ (填“红色”或“浅红)”。
(4)为比较两者热稳定性设计了“套管实验”,实验装置如图所示,整个实验过程中,能观察到澄清石灰水变浑浊的是烧杯_______ (填“A”成“B”)。

(5)以下能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是_______ 。
A.用pH试纸测定同浓度的Na2CO3和NaHCO3溶液pH值并做比较
B.分别在这两种物质的溶液中,加入少量CaCl2溶液
C.分别在这两种物质的溶液中,加入少量Ca(OH)2溶液
(6)常温下,用如图1所示装置,分别向 溶液和
溶液和 溶液中逐滴滴加
溶液中逐滴滴加 的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。
的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。

①表示向NaHCO3溶液中滴加盐酸的是曲线_______ (填X或Y)。
②写出ac段反应实质(离子方程式):_______ 。
(7)向 的NaOH溶液中通入标况下4.48L的CO2,请计算此时溶液中溶质的组成及物质的量
的NaOH溶液中通入标况下4.48L的CO2,请计算此时溶液中溶质的组成及物质的量_______ 。
(1)盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,观察到的现象是_______。
| A.钠在水层中反应并四处游动 | B.钠停留在煤油层中不发生反应 |
| C.钠在煤油的液面上反应并四处游动 | D.钠在煤油与水的界面处反应并上下跳动 |
(3)某实验小组通过以下实验来比较Na2CO3和NaHCO3两种物质的性质。称取两种固体各2g,分别放入两个小烧杯中,再各滴加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴加2滴酚酞试液。
①a烧杯中固体完全溶解,而b烧杯固体有剩余,b烧杯内的物质是
②同学们在两烧杯中还观察到了其它现象,其中a烧杯中出现的现象:Ⅰ溶液温度
(4)为比较两者热稳定性设计了“套管实验”,实验装置如图所示,整个实验过程中,能观察到澄清石灰水变浑浊的是烧杯

(5)以下能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是
A.用pH试纸测定同浓度的Na2CO3和NaHCO3溶液pH值并做比较
B.分别在这两种物质的溶液中,加入少量CaCl2溶液
C.分别在这两种物质的溶液中,加入少量Ca(OH)2溶液
(6)常温下,用如图1所示装置,分别向
 溶液和
溶液和 溶液中逐滴滴加
溶液中逐滴滴加 的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。
的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。
①表示向NaHCO3溶液中滴加盐酸的是曲线
②写出ac段反应实质(离子方程式):
(7)向
 的NaOH溶液中通入标况下4.48L的CO2,请计算此时溶液中溶质的组成及物质的量
的NaOH溶液中通入标况下4.48L的CO2,请计算此时溶液中溶质的组成及物质的量
您最近一年使用:0次
名校
4 . 回答下列问题:
(1)①胆矾的化学式是_______ ;②乙醛的结构简式是_______ 。
(2)过氧化钠与水反应的化学方程式是_______ 。
(3)向新制的 悬浊液中加入葡萄糖溶液,加热,观察到的现象是
悬浊液中加入葡萄糖溶液,加热,观察到的现象是_______ 。
(1)①胆矾的化学式是
(2)过氧化钠与水反应的化学方程式是
(3)向新制的
 悬浊液中加入葡萄糖溶液,加热,观察到的现象是
悬浊液中加入葡萄糖溶液,加热,观察到的现象是
您最近一年使用:0次
2022-06-24更新
|
269次组卷
|
2卷引用:浙江省嘉兴市2021-2022学年高一下学期期末检测化学试题
解题方法
5 . 化学与我们的生活、生产、环境等息息相关。回答下列问题:
(1)明矾的化学式为KAl(SO4)·12H2O,它常用于净水。明矾放入水中起净水作用的物质是___________ 。明矾与过量NaOH溶液反应的离子方程式是___________ 。
(2)维生素C能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有___________ 性,该转化反应中Fe3+作___________ 剂。
(3)某无土栽培用的营养液中,c(NH ):c(SO
):c(SO ):c(K+):c(Cl-)=8:4:9:9.若用NH4Cl、KCl、K2SO4来配制该营养液,则这三种盐的物质的量之比为
):c(K+):c(Cl-)=8:4:9:9.若用NH4Cl、KCl、K2SO4来配制该营养液,则这三种盐的物质的量之比为___________ 。
(4)汽车燃料中一般不含氮元素,尾气中所含NO是如何产生的?___________ 。能减少或有效控制汽车尾气污染有效且可行的措施是___________ 。
(5)在鲜活鱼的长途运输中,需在水中加入供氧剂。Na2O2(易溶于水)、CaO2(微溶于水)都可与水发生反应生成碱和氧气。写出Na2O2与水反应的化学方程式:___________ 。这两种物质中选___________ 作为供氧剂更好,理由是___________ 。
(1)明矾的化学式为KAl(SO4)·12H2O,它常用于净水。明矾放入水中起净水作用的物质是
(2)维生素C能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(3)某无土栽培用的营养液中,c(NH
 ):c(SO
):c(SO ):c(K+):c(Cl-)=8:4:9:9.若用NH4Cl、KCl、K2SO4来配制该营养液,则这三种盐的物质的量之比为
):c(K+):c(Cl-)=8:4:9:9.若用NH4Cl、KCl、K2SO4来配制该营养液,则这三种盐的物质的量之比为(4)汽车燃料中一般不含氮元素,尾气中所含NO是如何产生的?
(5)在鲜活鱼的长途运输中,需在水中加入供氧剂。Na2O2(易溶于水)、CaO2(微溶于水)都可与水发生反应生成碱和氧气。写出Na2O2与水反应的化学方程式:
您最近一年使用:0次
2022-01-20更新
|
165次组卷
|
2卷引用:四川省绵阳市2021-2022学年高一上学期期末考试化学试题
名校
解题方法
6 . 结合所学内容,完成下列问题:
(1)刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2,请写出反应的离子反应方程式_______ 。
(2)呼吸面具中,Na2O2起反应的化学方程式_______ 。
(3)在标准状况下,112mL某气体的质量为0.32g,试计算这种气体的相对分子质量_______ 。
(4)红热的木炭与浓硝酸反应的化学方程式为:C+4HNO3(浓) CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为
CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为__ ;如果产生标准状况下22.4LCO2,则转移的电子的物质的量为__ mol。
(1)刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2,请写出反应的离子反应方程式
(2)呼吸面具中,Na2O2起反应的化学方程式
(3)在标准状况下,112mL某气体的质量为0.32g,试计算这种气体的相对分子质量
(4)红热的木炭与浓硝酸反应的化学方程式为:C+4HNO3(浓)
 CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为
CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
9-10高一下·四川成都·期末
解题方法
7 . 下图中A~G是化合物,A是一种正盐,H是一种无色气态单质,C在高温下是气体,而常温下是一种无色液体, E为含钠的化合物。它们之间有如下转化关系:
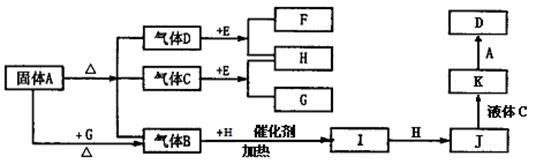
(1)实验室检验A的阳离子的一种方法为____________________________________________________________________________________________________________________________ 。
(2)K的浓溶液与碳单质反应的化学方程式______________________________ ,B与H催化氧化的化学方程式_______________________________________ 。上述转化中,属于氧化还原反应,且氧化剂和还原剂是同种物质的反应有________ 个。
(3)K的稀溶液中通入SO2气体,发生的化学反应的离子方程式为_________________________________________________________________________________________ 。
(4)H气体与H2S气体以4:5的体积比混合,电火花点燃后充分反应,发生反应的总的化学反应方程式为_________________________________________________________________ 。
(5)标准状况,将J与H按7:1的体积比充满烧瓶,将其倒置于盛有足量水的水槽中(假设进入烧瓶中的液体不扩散),实验结束后,烧瓶中溶液的物质的量浓度是___________ mol/L(计算结果保留3位小数)。

(1)实验室检验A的阳离子的一种方法为
(2)K的浓溶液与碳单质反应的化学方程式
(3)K的稀溶液中通入SO2气体,发生的化学反应的离子方程式为
(4)H气体与H2S气体以4:5的体积比混合,电火花点燃后充分反应,发生反应的总的化学反应方程式为
(5)标准状况,将J与H按7:1的体积比充满烧瓶,将其倒置于盛有足量水的水槽中(假设进入烧瓶中的液体不扩散),实验结束后,烧瓶中溶液的物质的量浓度是
您最近一年使用:0次
9-10高一下·甘肃兰州·期末
8 . 下图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,X受热分解所得气体在标况下的体积比为1:1,H为淡黄色粉末,B和G常温下是液体,其余均为气体。根据图中关系推断:

(1)化学式X________ ;
(2)A的电子式为__________ ;空间构型___________ ;
C的结构式为___________ ;H所包含的化学键类型__________ 。
(3)工业上制取A的化学反应方程式____ ;A→D的化学反应方程式____ ;
C+H→E的化学反应方程式_______ ;G→D的离子反应方程式_____ 。

(1)化学式X
(2)A的电子式为
C的结构式为
(3)工业上制取A的化学反应方程式
C+H→E的化学反应方程式
您最近一年使用:0次



