名校
解题方法
1 . 下列有关钠及其化合物的叙述错误的是
| A.Na2O2吸收CO2产生O2,可用作呼吸面具供氧剂 |
| B.高压钠灯发出的黄光透雾能力强,可用于道路和广场照明 |
| C.碳酸钠可用于制玻璃、造纸 |
| D.钠长期暴露在空气中的最终产物是NaHCO3 |
您最近一年使用:0次
2023-09-04更新
|
286次组卷
|
4卷引用:辽宁省大连市第八中学2021-2022学年高一上学期期中考试化学试题
名校
解题方法
2 . 以不同类别物质间的转化为线索,构建钠及其化合物关系如下:

下列分析不正确 的是

下列分析
| A.反应③表明CO2具有酸性氧化物的性质 |
| B.利用反应④,可除去NaHCO3固体中混有的少量Na2CO3 |
| C.反应⑤、⑥可应用于潜水艇中氧气的供给 |
| D.上述转化中发生的反应有分解反应、化合反应、置换反应 |
您最近一年使用:0次
解题方法
3 . 常见金属和非金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)实验室制取氢氧化铝时,常用铝盐溶液和_______ (填“氨水”或“氢氧化钠溶液”)作为原料。
(2)铝制餐具不宜长时间存放酸性、碱性食物,但铝制容器可以盛装浓硝酸的原因是_______ 。
(3)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是_______ (用离子方程式表示)。
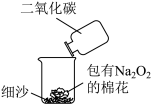
(4)如图实验可用来验证Na2O2与CO2的反应,实验过程中可观察到包有Na2O2的棉花燃烧。写出该反应的化学方程式_______ ,棉花燃烧说明该反应具有的特点是_______ 。
(5)铁红是一种红色颜料,其成分是_______ (填化学式)。将一定量的铁红溶于160 mL5 mol/L的盐酸中,再加入一定量铁粉恰好完全溶解,收集到气体2.24 L (标准状况下),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为_______ g。
(1)实验室制取氢氧化铝时,常用铝盐溶液和
(2)铝制餐具不宜长时间存放酸性、碱性食物,但铝制容器可以盛装浓硝酸的原因是
(3)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是
(4)如图实验可用来验证Na2O2与CO2的反应,实验过程中可观察到包有Na2O2的棉花燃烧。写出该反应的化学方程式

(5)铁红是一种红色颜料,其成分是
您最近一年使用:0次
名校
4 . 下列事实及其解释不正确的是
| A.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3 |
| B.钠保存在煤油中,是因为煤油不与钠发生反应,且钠比煤油密度大,煤油可以使钠隔绝空气 |
| C.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应 |
| D.钠长期露置在空气中的产物是Na2CO3,原因是钠与氧气反应生成的Na2O与水和二氧化碳反应后,经风化后得到Na2CO3粉末 |
您最近一年使用:0次
解题方法
5 . 完成下列问题
(1)下面是某同学对有关物质进行分类的列表:
每组分类均有错误,其错误的物质分别是_______ 、_______ 、_______ (填化学式)。
(2)写出Na2O2与CO2反应的方程式_______ (并用双线桥法标出电子转移情况)
(3)KHSO4在水溶液中的电离方程式可以表示为_______ ;
(4)向KHSO4溶液中加入碳酸氢钠,可以观察到的现象是_______ ,反应的离子方程式为_______ 。
(5)向KHSO4溶液中加入锌片,反应的离子方程式为_______ 。
(1)下面是某同学对有关物质进行分类的列表:
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| 第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
| 第二组 | NaOH | HCl | NaCl | Na2O2 | SO3 |
| 第三组 | KOH | CH3COOH | CaF2 | Al2O3 | SO2 |
(2)写出Na2O2与CO2反应的方程式
(3)KHSO4在水溶液中的电离方程式可以表示为
(4)向KHSO4溶液中加入碳酸氢钠,可以观察到的现象是
(5)向KHSO4溶液中加入锌片,反应的离子方程式为
您最近一年使用:0次
名校
解题方法
6 . 下列有关物质的性质与用途,不具有对应关系的是
A. 溶液呈酸性,可用于刻蚀铜板 溶液呈酸性,可用于刻蚀铜板 |
B. 的熔点高,常用作耐火、耐高温材料 的熔点高,常用作耐火、耐高温材料 |
C. 与 与 反应,可用于潜艇中的供氧剂 反应,可用于潜艇中的供氧剂 |
D. 具有强氧化性,常作为杀菌、消毒剂 具有强氧化性,常作为杀菌、消毒剂 |
您最近一年使用:0次
2022-12-22更新
|
177次组卷
|
2卷引用:天津市第四十七中学2021-2022学年高一上学期第二次月考化学试题
7 . 原子序数依次增大的五种短周期元素A、B、C、D、E,已知A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y;A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物,回答下列问题:
(1)B在周期表中的位置是_______ 。
(2)D和E形成的一种化合物与BD2发生氧化还原反应,该反应的化学方程式_______ 。
(3)B元素的单质与浓硫酸反应的化学方程式_______ 。
(4)C元素的最高价氧化物的水化物与其氢化物反应的离子方程式_______ 。
(1)B在周期表中的位置是
(2)D和E形成的一种化合物与BD2发生氧化还原反应,该反应的化学方程式
(3)B元素的单质与浓硫酸反应的化学方程式
(4)C元素的最高价氧化物的水化物与其氢化物反应的离子方程式
您最近一年使用:0次
8 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式:_______ 。
(2)氯水、漂白液和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,其化学方程式为_______ 。
②漂白液与洁厕灵不能混合使用,原因是_______ (用离子方程式表示)
(3)①用化学方程式表示侯德榜制碱法的反应原理:________ 。
②将CO2通入饱和Na2CO3溶液有晶体析出,写出反应的离子方程式_______ 。
(4)工业上,常用H2O2除去FeCl3溶液中的FeCl2,反应的离子方程式为_______ 。
(1)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式:
(2)氯水、漂白液和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
①工业上利用氯气和氢氧化钙反应可制得漂白粉,其化学方程式为
②漂白液与洁厕灵不能混合使用,原因是
(3)①用化学方程式表示侯德榜制碱法的反应原理:
②将CO2通入饱和Na2CO3溶液有晶体析出,写出反应的离子方程式
(4)工业上,常用H2O2除去FeCl3溶液中的FeCl2,反应的离子方程式为
您最近一年使用:0次
解题方法
9 . 某混合物由Na2O2、Na2O、Na2CO3、NaHCO3、NaCl中的几种组成,向其中加入足量的盐酸有气体放出,将气体通过足量的NaOH溶液,气体体积减小;将上述混合物在空气中加热,有气体放出,但残留固体质量有所增加,则下列判断正确的是
| A.混合物中一定含Na2CO3、NaCl |
| B.混合物中一定含有Na2O2、Na2O、NaHCO3 |
| C.无法确定混合物中是否含有Na2CO3 |
| D.混合物中一定不含Na2CO3、NaCl |
您最近一年使用:0次
名校
10 . 设NA为阿伏加德罗常数,下列有关NA的说法正确的是
| A.标准状态下,2.24 L CO2通过足量的Na2O2,转移的电子数目为0.1NA |
| B.6 mol/LFeCl310 mL能制得Fe(OH)3胶粒0.06NA |
| C.0.1 mol/LCH3COOH溶液100 mL,含H+的数目为0.01NA |
| D.7.8 g Na2O2中含阴、阳离子的总数为0.4NA |
您最近一年使用:0次
2022-12-21更新
|
197次组卷
|
2卷引用:湖北省十堰市第二中学2021-2022学年高一上学期12月考试化学试题



