名校
解题方法
1 . 室温下,下列实验的探究方案能够达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 室温下,向一定量的饱和 溶液中通入足量的 溶液中通入足量的 气体,观察是否有晶体析出 气体,观察是否有晶体析出 | 探究室温下 固体和 固体和 固体在水中的溶解度大小 固体在水中的溶解度大小 |
| B | 向两支试管中各加入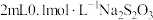 溶液,分别放入盛有冷水和热水的两个烧杯中,再同时分别向两支试管中加入 溶液,分别放入盛有冷水和热水的两个烧杯中,再同时分别向两支试管中加入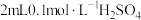 溶液,振荡,观察现象 溶液,振荡,观察现象 | 探究温度对化学反应速率的影响 |
| C | 向 的蔗糖溶液中加入少量稀 的蔗糖溶液中加入少量稀 ,加热,再加入新制氢氧化铜溶液,观察现象 ,加热,再加入新制氢氧化铜溶液,观察现象 | 探究蔗糖的水解条件 |
| D | 以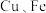 为电极,以酸化的 为电极,以酸化的 的 的 溶液作电解质溶液,连接成原电池装置,过一段时间,从 溶液作电解质溶液,连接成原电池装置,过一段时间,从 电极区取少量溶液于试管中,再向试管中滴入2滴 电极区取少量溶液于试管中,再向试管中滴入2滴 溶液,观察现象 溶液,观察现象 | 探究牺牲阳极的阴极保护法 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-12-15更新
|
440次组卷
|
2卷引用:四川省成都市石室中学2024届高三上学期一诊模拟考试理科综合化学试题
名校
2 . 某实验小组欲探究 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为___________ 。
(2)称取两种固体各2g,分别加入两个小烧杯中,再各加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①发现 固体完全溶解,而
固体完全溶解,而 固体有剩余,由此得出结论:
固体有剩余,由此得出结论:___________ 。
②同学们在两烧杯中还观察到以下现象。其中,盛放 的烧杯中出现的现象是
的烧杯中出现的现象是___________ (填字母序号)
a.溶液温度升高 b.溶液温度下降
c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置I和II中分别放入药品,将气球内的固体同时倒入试管中。
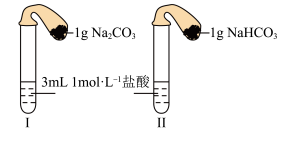
①两试管中均产生气体,___________ 的反应程度更为剧烈。(填“I”或“II”)
②反应结束后,恢复至室温,下列说法正确的是___________ 。
a.装置I的气球体积较大 b.装置II的气球体积较大
c.生成气体的体积根据盐酸计算 d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成 的溶液,设计如下方案并对反应现象做出预测:
的溶液,设计如下方案并对反应现象做出预测:
实施实验后,发现操作1的现象与预测有差异:产生白色沉淀和二氧化碳气体。则该条件下, 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为
(2)称取两种固体各2g,分别加入两个小烧杯中,再各加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①发现
 固体完全溶解,而
固体完全溶解,而 固体有剩余,由此得出结论:
固体有剩余,由此得出结论:②同学们在两烧杯中还观察到以下现象。其中,盛放
 的烧杯中出现的现象是
的烧杯中出现的现象是a.溶液温度升高 b.溶液温度下降
c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置I和II中分别放入药品,将气球内的固体同时倒入试管中。

①两试管中均产生气体,
②反应结束后,恢复至室温,下列说法正确的是
a.装置I的气球体积较大 b.装置II的气球体积较大
c.生成气体的体积根据盐酸计算 d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成
 的溶液,设计如下方案并对反应现象做出预测:
的溶液,设计如下方案并对反应现象做出预测:| 实验方案 | 预测现象 | 预测依据 |
操作1:向 溶液中滴加 溶液中滴加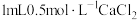 溶液 溶液 | 无白色沉淀 |  溶液中的 溶液中的 浓度很小,不能与 浓度很小,不能与 反应 反应 |
操作2:向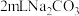 溶液中滴加 溶液中滴加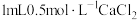 溶液 溶液 | 有白色沉淀 |  溶液中的 溶液中的 浓度较大,能与 浓度较大,能与 发生反应 发生反应 |
 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近半年使用:0次
名校
解题方法
3 . 某校化学课外小组为了鉴别 和
和 两种白色固体,用不同的方法做了以下实验,如图所示。
两种白色固体,用不同的方法做了以下实验,如图所示。
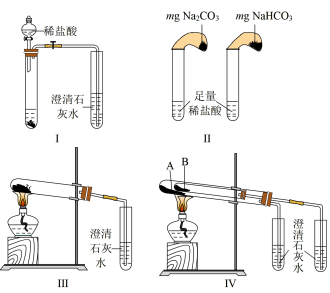
(1)方法Ⅰ是向两种白色粉末中,分别逐滴加入稀盐酸。
方法Ⅰ________ (填“能”或“不能”)鉴别 和
和 。
。
(2)方法Ⅱ能鉴别 和
和 的现象是
的现象是________ .
(3)方法Ⅲ、Ⅳ均能鉴别这两种物质:与方法Ⅲ相比,方法Ⅳ的优点是________(填字母)。
(4)若用方法Ⅳ验证 和
和 的稳定性,则试管B中装入的固体是
的稳定性,则试管B中装入的固体是________ (填化学式)。
(5)除了以上方法,请再写出1种鉴别二者的方法________ 。
 和
和 两种白色固体,用不同的方法做了以下实验,如图所示。
两种白色固体,用不同的方法做了以下实验,如图所示。
(1)方法Ⅰ是向两种白色粉末中,分别逐滴加入稀盐酸。
方法Ⅰ
 和
和 。
。(2)方法Ⅱ能鉴别
 和
和 的现象是
的现象是(3)方法Ⅲ、Ⅳ均能鉴别这两种物质:与方法Ⅲ相比,方法Ⅳ的优点是________(填字母)。
| A.方法Ⅳ比方法Ⅲ复杂 |
| B.方法Ⅳ比方法Ⅲ安全 |
| C.方法Ⅳ比方法Ⅲ操作简便 |
| D.方法Ⅳ可以用一套装置同时进行两个实验,而方法Ⅲ不行 |
(4)若用方法Ⅳ验证
 和
和 的稳定性,则试管B中装入的固体是
的稳定性,则试管B中装入的固体是(5)除了以上方法,请再写出1种鉴别二者的方法
您最近半年使用:0次
解题方法
4 . 以NaCl为原料,可制取Na、Na2O2、NaOH和Na2CO3等。Na2CO3可用侯氏制碱法制取,主要涉及如下反应:
(1)N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ•mol-1
2NH3(g) ΔH=-92.4kJ•mol-1
(2)NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
(3)2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
下列有关比较正确的是
(1)N2(g)+3H2(g)
 2NH3(g) ΔH=-92.4kJ•mol-1
2NH3(g) ΔH=-92.4kJ•mol-1(2)NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
(3)2NaHCO3
 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O下列有关比较正确的是
| A.键能(E):6E(N−H)>E(N≡N)+3E(H−H) | B.热稳定性:NaHCO3>Na2CO3 |
| C.同浓度溶液的pH:NaHCO3>Na2CO3 | D.沸点:NH3>H2O |
您最近半年使用:0次
解题方法
5 . 下列实验装置或实验操作能完成相应实验目的的是
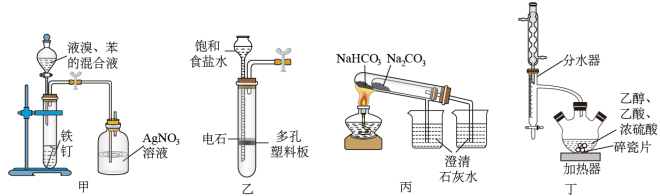

| A.装置甲:验证苯和液溴发生取代反应 | B.装置乙:实验室制乙炔 |
| C.装置丙:验证碳酸钠和碳酸氢钠的稳定性 | D.装置丁:提高乙酸乙酯的产率 |
您最近半年使用:0次
6 . 实验是学习化学、探究化学过程的重要途径。下列装置不能达到相应实验目的的是
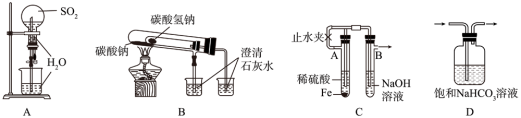

| A.进行喷泉实验 | B.比较 与 与 的热稳定性 的热稳定性 |
C.制备 沉淀 沉淀 | D.除去 中混有的 中混有的 气体 气体 |
您最近半年使用:0次
解题方法
7 . 下列除杂方案正确的是
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 |
| A |  溶液 溶液 |  | 通入适量的 |
| B |  溶液 溶液 |  |  粉 粉 |
| C |  溶液 溶液 |  | 滴加澄清石灰水 |
| D |  溶液 溶液 |  | 加入适量的氯化钡溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-01-27更新
|
201次组卷
|
2卷引用:广东省清远市2021-2022学年高一上学期期末教学质量检测化学试题
解题方法
8 . Na2CO3和NaHCO3是重要的无机化工产品,广泛应用于食品、化工、医药等领域。如图是利用天然碱(主要成分为Na2CO3、NaHCO3和少量NaCl)制备Na2CO3和NaHCO3的工艺流程。
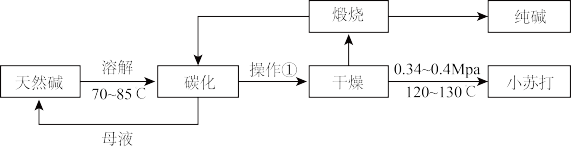
完成下列填空:
(1)操作①为___ 。
(2)碳化装置中反应的离子方程式___ 。
(3)解释选择0.34~0.4MPa干燥的原因___ 。
(4)对比索尔维制碱法,说明利用天然碱制碱的优势___ 。
(5)为了测定产品中小苏打中NaHCO3的含量进行以下实验。
实验步骤:
步骤一:称2.000g小苏打样品,配制小苏打溶液250mL。
步骤二:取20.00mL小苏打溶液置于锥形瓶中,用0.1000mol·L-1盐酸滴定,溶液pH随盐酸体积变化如图所示。

完成下列填空:
①取20.00mL小苏打溶液需要使用的定量仪器名称____ 。
②根据滴定曲线分析,若采用传统滴定法,应选择的指示剂是___ ,此时滴定终点的现象为___ 。
③计算该样品中NaHCO3的质量分数为____ 。

完成下列填空:
(1)操作①为
(2)碳化装置中反应的离子方程式
(3)解释选择0.34~0.4MPa干燥的原因
(4)对比索尔维制碱法,说明利用天然碱制碱的优势
(5)为了测定产品中小苏打中NaHCO3的含量进行以下实验。
实验步骤:
步骤一:称2.000g小苏打样品,配制小苏打溶液250mL。
步骤二:取20.00mL小苏打溶液置于锥形瓶中,用0.1000mol·L-1盐酸滴定,溶液pH随盐酸体积变化如图所示。

完成下列填空:
①取20.00mL小苏打溶液需要使用的定量仪器名称
②根据滴定曲线分析,若采用传统滴定法,应选择的指示剂是
③计算该样品中NaHCO3的质量分数为
您最近半年使用:0次
9 . 下列说法正确的是
| A.钢铁在潮湿空气中生锈主要是发生了化学腐蚀 |
| B.NaHCO3的热稳定性比Na2CO3强 |
| C.水玻璃是建筑行业常用的一种黏合剂 |
| D.溴化银是一种重要的感光材料,常用于人工降雨 |
您最近半年使用:0次



