名校
解题方法
1 . 化学与生活密切相关,下列有关物质及其用途叙述正确的是
| A.过氧化钠是碱性氧化物,且可以作潜艇中的供氧剂 |
| B.碳酸钠在医疗上是治疗胃酸过多的一种药剂 |
| C.向碳酸氢钠中加少量水,插入温度计,显示温度上升 |
| D.碳酸钠可用于造纸、制皂、玻璃等工业方面 |
您最近一年使用:0次
名校
解题方法
2 . 下列有关物质的性质与用途说法不正确的是
| A.碳酸钠的水溶液显碱性,可用作食用碱 |
| B.碳酸氢钠受热易分解,可以用作焙制糕点的膨松剂 |
| C.过氧化钠具有强还原性,可用于潜水艇的供氧剂 |
| D.ClO2具有强氧化性,可用于自来水杀菌消毒 |
您最近一年使用:0次
名校
解题方法
3 . 元素的价一类二维图是我们学习元素及其化合物相关知识的重要模型和工具,图为钠的价一类二维图。请回答以下问题:

(1)NaH中H元素的化合价是___________ 。
(2)钠单质通常保存在___________ 中。
(3)请写出①中某种淡黄色固体的用途:___________ 。
(4)把钠放到装有水的烧杯中,钠会浮在水面上,原因是___________ ;金属钠与水反应的离子方程式是___________ 。
(5)利用如图实验比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为___________ ,写出实验过程中试管内发生反应的化学方程式:___________ 。


(1)NaH中H元素的化合价是
(2)钠单质通常保存在
(3)请写出①中某种淡黄色固体的用途:
(4)把钠放到装有水的烧杯中,钠会浮在水面上,原因是
(5)利用如图实验比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为

您最近一年使用:0次
名校
4 . 下列有关钠的化合物的性质及用途的叙述,不正确的是
| A.碳酸钠可用于治疗胃溃疡病人的胃酸过多症 |
| B.碳酸钠、碳酸氢钠的水溶液均呈碱性,可用作食用碱或工业用碱 |
| C.Na2O2呈淡黄色,可用作呼吸面具供氧剂 |
| D.碳酸钠溶于水会放热,碳酸氢钠溶于水吸热 |
您最近一年使用:0次
名校
5 . 钠元素在自然界分布很广,储量极为丰富,都以化合态存在。钠及其化合物(如 等)在生产生活中被广泛应用。
等)在生产生活中被广泛应用。
(1)金属钠用途广泛。
①可用于制备 。采用空气和
。采用空气和 为原料可直接制备
为原料可直接制备 。空气与熔融金属
。空气与熔融金属 反应前需依次通过
反应前需依次通过_______ 、_______ (填序号)。
a.浓硫酸 b.饱和食盐水 c. 溶液 d.酸性
溶液 d.酸性 溶液
溶液
②金属钠还可以用于钛、锆、铌、钽等金属的冶炼。如高温条件下, 与
与 反应制备
反应制备 ,反应的化学方程式为
,反应的化学方程式为_______ 。
(2)碳酸钠和碳酸氢钠均可作食用碱。传统蒸馒头常采用酵头发面,再用 调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生
调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
①等质量的碳酸钠和碳酸氢钠与足量醋酸充分反应,消耗醋酸更多的是_______ 。(写名称)
②若面团发得不好,面团内的气孔少,略有酸味。可不用 而用
而用 ,继续揉面,上锅蒸后也能蒸出松软可口的馒头。解释
,继续揉面,上锅蒸后也能蒸出松软可口的馒头。解释 的作用
的作用_______ 。
(3)某实验兴趣小组想探究某食用碱( 或
或 )的成分,依次进行如下实验:
)的成分,依次进行如下实验:
实验1:取适量(约 )食用碱固体于试管中,滴加少量水,振荡,观察到固体溶解,并伴随放热现象。据此推测,该食用碱主要成分为
)食用碱固体于试管中,滴加少量水,振荡,观察到固体溶解,并伴随放热现象。据此推测,该食用碱主要成分为_______ 。(写化学式)
实验2: 长期放置在空气中会变质(部分转变为
长期放置在空气中会变质(部分转变为 ),现欲测定该食用碱中
),现欲测定该食用碱中 的质量分数,设计如下实验装置。
的质量分数,设计如下实验装置。

称取食用碱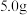 置于A试管中,C中加入一定质量并足量的
置于A试管中,C中加入一定质量并足量的 固体,充分加热,观察到D处的现象为
固体,充分加热,观察到D处的现象为_______ 。实验结束后,测得 固体增重
固体增重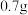 ,则该食用碱中
,则该食用碱中 的质量分数为
的质量分数为_______ 。
 等)在生产生活中被广泛应用。
等)在生产生活中被广泛应用。(1)金属钠用途广泛。
①可用于制备
 。采用空气和
。采用空气和 为原料可直接制备
为原料可直接制备 。空气与熔融金属
。空气与熔融金属 反应前需依次通过
反应前需依次通过a.浓硫酸 b.饱和食盐水 c.
 溶液 d.酸性
溶液 d.酸性 溶液
溶液②金属钠还可以用于钛、锆、铌、钽等金属的冶炼。如高温条件下,
 与
与 反应制备
反应制备 ,反应的化学方程式为
,反应的化学方程式为(2)碳酸钠和碳酸氢钠均可作食用碱。传统蒸馒头常采用酵头发面,再用
 调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生
调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。①等质量的碳酸钠和碳酸氢钠与足量醋酸充分反应,消耗醋酸更多的是
②若面团发得不好,面团内的气孔少,略有酸味。可不用
 而用
而用 ,继续揉面,上锅蒸后也能蒸出松软可口的馒头。解释
,继续揉面,上锅蒸后也能蒸出松软可口的馒头。解释 的作用
的作用(3)某实验兴趣小组想探究某食用碱(
 或
或 )的成分,依次进行如下实验:
)的成分,依次进行如下实验:实验1:取适量(约
 )食用碱固体于试管中,滴加少量水,振荡,观察到固体溶解,并伴随放热现象。据此推测,该食用碱主要成分为
)食用碱固体于试管中,滴加少量水,振荡,观察到固体溶解,并伴随放热现象。据此推测,该食用碱主要成分为实验2:
 长期放置在空气中会变质(部分转变为
长期放置在空气中会变质(部分转变为 ),现欲测定该食用碱中
),现欲测定该食用碱中 的质量分数,设计如下实验装置。
的质量分数,设计如下实验装置。
称取食用碱
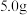 置于A试管中,C中加入一定质量并足量的
置于A试管中,C中加入一定质量并足量的 固体,充分加热,观察到D处的现象为
固体,充分加热,观察到D处的现象为 固体增重
固体增重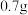 ,则该食用碱中
,则该食用碱中 的质量分数为
的质量分数为
您最近一年使用:0次
2023-11-24更新
|
123次组卷
|
2卷引用:河北省石家庄市第二中学2023-2024学年高一上学期期中考试化学试题
6 . 钠及其化合物在认识物质转化规律以及生产生活中均有重要应用。
Ⅰ.钠与水的反应
(1)将钠投入足量含有酚酞的水中,作了如下记录,将实验现象与匹配的实验结论连线:_______ 。
(2)写出钠与水反应的化学方程式_______ 。
(3)若反应中生成H2的体积为1.12L(标准状况下),则参与反应的金属Na的质量是_______ 。
(4)同物质类别的金属Mg也能与水发生反应,试着调用反应规律分析Na和Mg分别与水反应的剧烈程度:Na_______ Mg(填“>”“<”或“=”)。
Ⅱ.钠与氧气的反应
(5)钠与氧气反应的产物有多种可能,造成产物多样的原因是_______ 。
(6)其中产物_______ (填化学式)可用作潜水艇和呼吸面具中的供氧剂,写出其与CO2反应的化学方程式_______ 。
Ⅲ.碳酸钠、碳酸氢钠在食品加工方面有着广泛的用途
(7)下列关于Na2CO3的认识正确的是_______ 。
a.受热易分解 b.俗称纯碱、苏打 c.属于碱 d.可与酸反应
(8)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面”将酸去除。等质量的Na2CO3和NaHCO3,因_______ (填“Na2CO3”或“NaHCO3”)消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。
(9)若面团发得不好,面团内的气孔少,不够膨松。需添加_______ (填“Na2CO3”或“NaHCO3”),继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式表示其产气原理_______ 。
Ⅰ.钠与水的反应
(1)将钠投入足量含有酚酞的水中,作了如下记录,将实验现象与匹配的实验结论连线:
实验现象 实验结论 A.钠浮在水面上 a.有碱生成B.钠四处游动 b.有气体产生 C.溶液变红 c.反应放热,钠熔点低 D.钠熔成光亮的小球 d.钠的密度比水小 |
(3)若反应中生成H2的体积为1.12L(标准状况下),则参与反应的金属Na的质量是
(4)同物质类别的金属Mg也能与水发生反应,试着调用反应规律分析Na和Mg分别与水反应的剧烈程度:Na
Ⅱ.钠与氧气的反应
(5)钠与氧气反应的产物有多种可能,造成产物多样的原因是
(6)其中产物
Ⅲ.碳酸钠、碳酸氢钠在食品加工方面有着广泛的用途
(7)下列关于Na2CO3的认识正确的是
a.受热易分解 b.俗称纯碱、苏打 c.属于碱 d.可与酸反应
(8)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面”将酸去除。等质量的Na2CO3和NaHCO3,因
(9)若面团发得不好,面团内的气孔少,不够膨松。需添加
您最近一年使用:0次
名校
7 . 钠和钠的化合物有许多重要的用途,碳酸钠可用于从海水提取溴,涉及的反应如下:3Br2+6Na2CO3+3H2O=5NaBr+NaBrO3+6NaHCO3。
(1)用双线桥法标出电子转移的方向和数目_______ 。
(2)该反应的离子方程式为_______ 。
(3)该反应中氧化剂与还原剂的物质的量之比是_______ 。
(4)钠着火时应采取的灭火措施是_______ ,不能用水灭火,原因是_______ (涉及反应的离子方程式)。
(5)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈_______ 色。
(6)等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,在相同条件下产生CO2的体积V(Na2CO3)_______ V(NaHCO3)(填“大于”,“小于”或“等于”)。
(7)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为_______ 。
(1)用双线桥法标出电子转移的方向和数目
(2)该反应的离子方程式为
(3)该反应中氧化剂与还原剂的物质的量之比是
(4)钠着火时应采取的灭火措施是
(5)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈
(6)等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,在相同条件下产生CO2的体积V(Na2CO3)
(7)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为
您最近一年使用:0次
解题方法
8 . 关于NaHCO3的性质和用途。下列说法正确的是
| A. NaHCO3可用于烘焙糕点 |
| B.相同温度下NaHCO3的溶解度比Na2CO3要大 |
| C. NaHCO3只能和酸反应,不能和碱反应 |
| D.可以用Ca(OH)2来鉴别Na2CO3和NaHCO3 |
您最近一年使用:0次
名校
9 . 回答下列问题:
(1)盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,观察到的现象是_______。
(2)钠在空气中燃烧可制得过氧化钠,过氧化钠的用途之一便是在呼吸面具中做供氧剂,用化学语言(反应方程式)来说明其原理:(提示:人呼出的气体中含有CO2和水蒸气)_______ 。
(3)某实验小组通过以下实验来比较Na2CO3和NaHCO3两种物质的性质。称取两种固体各2g,分别放入两个小烧杯中,再各滴加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴加2滴酚酞试液。
①a烧杯中固体完全溶解,而b烧杯固体有剩余,b烧杯内的物质是_______ 。
②同学们在两烧杯中还观察到了其它现象,其中a烧杯中出现的现象:Ⅰ溶液温度_______ (填“升高”或“降低”),Ⅱ滴加酚酞试液显_______ (填“红色”或“浅红)”。
(4)为比较两者热稳定性设计了“套管实验”,实验装置如图所示,整个实验过程中,能观察到澄清石灰水变浑浊的是烧杯_______ (填“A”成“B”)。

(5)以下能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是_______ 。
A.用pH试纸测定同浓度的Na2CO3和NaHCO3溶液pH值并做比较
B.分别在这两种物质的溶液中,加入少量CaCl2溶液
C.分别在这两种物质的溶液中,加入少量Ca(OH)2溶液
(6)常温下,用如图1所示装置,分别向 溶液和
溶液和 溶液中逐滴滴加
溶液中逐滴滴加 的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。
的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。

①表示向NaHCO3溶液中滴加盐酸的是曲线_______ (填X或Y)。
②写出ac段反应实质(离子方程式):_______ 。
(7)向 的NaOH溶液中通入标况下4.48L的CO2,请计算此时溶液中溶质的组成及物质的量
的NaOH溶液中通入标况下4.48L的CO2,请计算此时溶液中溶质的组成及物质的量_______ 。
(1)盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,观察到的现象是_______。
| A.钠在水层中反应并四处游动 | B.钠停留在煤油层中不发生反应 |
| C.钠在煤油的液面上反应并四处游动 | D.钠在煤油与水的界面处反应并上下跳动 |
(3)某实验小组通过以下实验来比较Na2CO3和NaHCO3两种物质的性质。称取两种固体各2g,分别放入两个小烧杯中,再各滴加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴加2滴酚酞试液。
①a烧杯中固体完全溶解,而b烧杯固体有剩余,b烧杯内的物质是
②同学们在两烧杯中还观察到了其它现象,其中a烧杯中出现的现象:Ⅰ溶液温度
(4)为比较两者热稳定性设计了“套管实验”,实验装置如图所示,整个实验过程中,能观察到澄清石灰水变浑浊的是烧杯

(5)以下能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是
A.用pH试纸测定同浓度的Na2CO3和NaHCO3溶液pH值并做比较
B.分别在这两种物质的溶液中,加入少量CaCl2溶液
C.分别在这两种物质的溶液中,加入少量Ca(OH)2溶液
(6)常温下,用如图1所示装置,分别向
 溶液和
溶液和 溶液中逐滴滴加
溶液中逐滴滴加 的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。
的稀盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。
①表示向NaHCO3溶液中滴加盐酸的是曲线
②写出ac段反应实质(离子方程式):
(7)向
 的NaOH溶液中通入标况下4.48L的CO2,请计算此时溶液中溶质的组成及物质的量
的NaOH溶液中通入标况下4.48L的CO2,请计算此时溶液中溶质的组成及物质的量
您最近一年使用:0次
解题方法
10 .  和
和 是中学化学中常见的物质,在生产生活中有重要的用途。
是中学化学中常见的物质,在生产生活中有重要的用途。
i.某小组同学依据性质差异,采用比较的方法设计实验鉴别 和
和 。
。
(1)实验Ⅰ中,分别向两支试管中滴加几滴水,A中温度计示数略有降低,B中温度计示数升高。说明固体b与水作用的过程中_______ (填“放出”或“吸收”)热量,可判断固体b为 。
。
(2)实验Ⅱ中,向试管C和D中分别加入5mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。判断固体d为_______ (填化学式)。
(3)25℃时,在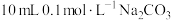 溶液中逐滴加入
溶液中逐滴加入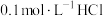 溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数(某微粒x的物质的量分数
溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数(某微粒x的物质的量分数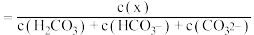
 )变化如图所示。请写出OAB段的离子方程式
)变化如图所示。请写出OAB段的离子方程式_______ 。

ii.实验室用 固体配制500 mL 0.10 mol/L的
固体配制500 mL 0.10 mol/L的 溶液,回答下列问题:
溶液,回答下列问题:
(4)称量的 固体质量应为
固体质量应为_______ g。
(5)实验操作的正确顺序是_______ 。(填序号)
①将称量好的 中加适量蒸馏水溶解在小烧杯中。
中加适量蒸馏水溶解在小烧杯中。
②将①所得溶液冷却到室温后,小心转入_______ (填仪器名称)中。
③将容量瓶瓶塞塞紧,充分摇匀。
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次。
⑤继续加蒸馏水至液面距刻度线1~2cm处,改用_______ (填仪器名称),小心滴加蒸馏水至溶液凹液面最低点与刻度线相切。
(6)取出100mL配制好的溶液,加蒸馏水稀释至 。则稀释后溶液的体积为
。则稀释后溶液的体积为_______ 。
(7)下列操作会使所配溶液的物质的量浓度偏低的是_______。(填字母序号)
 和
和 是中学化学中常见的物质,在生产生活中有重要的用途。
是中学化学中常见的物质,在生产生活中有重要的用途。i.某小组同学依据性质差异,采用比较的方法设计实验鉴别
 和
和 。
。| 实验Ⅰ | 实验Ⅱ |
 |  |
 。
。(2)实验Ⅱ中,向试管C和D中分别加入5mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。判断固体d为
(3)25℃时,在
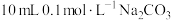 溶液中逐滴加入
溶液中逐滴加入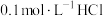 溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数(某微粒x的物质的量分数
溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数(某微粒x的物质的量分数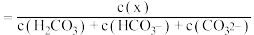
 )变化如图所示。请写出OAB段的离子方程式
)变化如图所示。请写出OAB段的离子方程式
ii.实验室用
 固体配制500 mL 0.10 mol/L的
固体配制500 mL 0.10 mol/L的 溶液,回答下列问题:
溶液,回答下列问题:(4)称量的
 固体质量应为
固体质量应为(5)实验操作的正确顺序是
①将称量好的
 中加适量蒸馏水溶解在小烧杯中。
中加适量蒸馏水溶解在小烧杯中。②将①所得溶液冷却到室温后,小心转入
③将容量瓶瓶塞塞紧,充分摇匀。
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次。
⑤继续加蒸馏水至液面距刻度线1~2cm处,改用
(6)取出100mL配制好的溶液,加蒸馏水稀释至
 。则稀释后溶液的体积为
。则稀释后溶液的体积为(7)下列操作会使所配溶液的物质的量浓度偏低的是_______。(填字母序号)
| A.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外 |
| B.定容时,俯视容量瓶上的刻度线 |
| C.加水定容时,水量超过了刻度线 |
| D.洗涤步骤中,洗涤液没有转入容量瓶 |
您最近一年使用:0次



