名校
1 . 钠及其化合物的生产、应用,是化工生产与研究的重要组成部分。
(1)金属钠可用于除去有机溶剂(如苯、醚等)中的少许水分,有关反应的化学方程式是___________ 。
(2)“神舟号”载人航天器的返回舱内,为防止CO2浓度过大引起宇航员困乏,用过氧化钠降低CO2的浓度,有关反应的化学方程式是___________ 。
(3)工业碳酸钠(纯度约为98%)中常含有少量Ca2+、Mg2+、Fe3+、Cl-和SO 等杂质离子,经提纯可获得试剂级碳酸钠(纯度约为99.95%),采用的工艺流程如图:
等杂质离子,经提纯可获得试剂级碳酸钠(纯度约为99.95%),采用的工艺流程如图:

①加入NaOH的主要目的是为了除去___________ (填离子符号)。
②为了检验试剂级碳酸钠中是否含有Cl-,可进行的操作是:取少量待测固体溶于蒸馏水配成溶液后,再取少量溶液于试管中,___________ 。
(4) 可用于治疗胃酸过多,反应的离子方程式为
可用于治疗胃酸过多,反应的离子方程式为___________ 。等质量的 与
与 相比,消耗胃酸的量:
相比,消耗胃酸的量:
________  (填“>”、“<”或“=”)。不宜用
(填“>”、“<”或“=”)。不宜用 治疗胃酸过多的原因是
治疗胃酸过多的原因是___________ (答出一点即可)。
(1)金属钠可用于除去有机溶剂(如苯、醚等)中的少许水分,有关反应的化学方程式是
(2)“神舟号”载人航天器的返回舱内,为防止CO2浓度过大引起宇航员困乏,用过氧化钠降低CO2的浓度,有关反应的化学方程式是
(3)工业碳酸钠(纯度约为98%)中常含有少量Ca2+、Mg2+、Fe3+、Cl-和SO
 等杂质离子,经提纯可获得试剂级碳酸钠(纯度约为99.95%),采用的工艺流程如图:
等杂质离子,经提纯可获得试剂级碳酸钠(纯度约为99.95%),采用的工艺流程如图:
①加入NaOH的主要目的是为了除去
②为了检验试剂级碳酸钠中是否含有Cl-,可进行的操作是:取少量待测固体溶于蒸馏水配成溶液后,再取少量溶液于试管中,
(4)
 可用于治疗胃酸过多,反应的离子方程式为
可用于治疗胃酸过多,反应的离子方程式为 与
与 相比,消耗胃酸的量:
相比,消耗胃酸的量:
 (填“>”、“<”或“=”)。不宜用
(填“>”、“<”或“=”)。不宜用 治疗胃酸过多的原因是
治疗胃酸过多的原因是
您最近一年使用:0次
名校
2 . 下列说法中不正确 的是
| A.Na2CO3比NaHCO3易溶于水 |
| B.Na2CO3比NaHCO3稳定 |
| C.Na2CO3和NaHCO3都能跟石灰水反应得到白色沉淀 |
| D.物质的质量相等的Na2CO3和NaHCO3分别与足量盐酸反应得到的CO2物质的质量之比为2∶1 |
您最近一年使用:0次
2021-11-05更新
|
43次组卷
|
9卷引用:2015-2016学年宁夏六盘山高级中学高一上学期期末化学试卷
2015-2016学年宁夏六盘山高级中学高一上学期期末化学试卷内蒙古乌兰察布市集宁一中2017-2018学年高一12月月考化学试题安徽省濉溪县临涣中学2017-2018学年高一上学期第二次月考化学试题云南省峨山彝族自治县第一中学2017-2018学年高一上学期期末考试化学试题江西省抚州市南城县第二中学2019-2020学年高一上学期第二次月考化学试题安徽省阜阳市颍上二中2019-2020学年高一上学期第二次段考化学试题安徽省亳州市黉学高级中学2019-2020学年高一上学期期中考试化学试题(英才班)湖南省怀化市第五中学2021-2022学年高一上学期期中考试化学试题宁夏石嘴山市第三中学2021-2022学年高一上学期期末考试化学试题
名校
解题方法
3 . 某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如图的探究方案,请你参与并完成该探究方案。
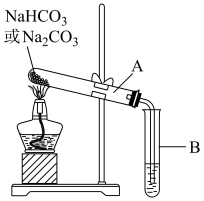
(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成。
(1)设计实验:①利用如图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是___ (填“澄清的石灰水”或“NaOH溶液”)。
(2)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有___ 沉淀生成(填沉淀的颜色)。
(3)说明Na2CO3和NaHCO3的热稳定性是:Na2CO3___ NaHCO3(填“>”或“<”)。

(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成。
(1)设计实验:①利用如图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是
(2)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有
(3)说明Na2CO3和NaHCO3的热稳定性是:Na2CO3
您最近一年使用:0次
2021-11-02更新
|
119次组卷
|
3卷引用:湖南省怀化市第五中学2019-2020学年高一下学期期中考试化学试题
名校
4 . 为除去括号内的杂质,所选用的试剂或方法正确的是
| A.Na2CO3溶液(NaHCO3),加入过量的NaOH溶液 |
| B.CO2(HCl),通过饱和碳酸钠溶液 |
| C.Cl2(HCl),通过饱和食盐水 |
| D.Na2CO3溶液(Na2SO4),加入过量Ba(OH)2溶液,过滤 |
您最近一年使用:0次
2021-10-23更新
|
583次组卷
|
3卷引用:山东省青岛二中2020-2021学年高一上学期期中化学试题
名校
解题方法
5 . 有关NaHCO3和Na2CO3的性质,以下叙述错误的是
| A.等质量的NaHCO3和Na2CO3与足量盐酸反应,在相同条件下Na2CO3产生的CO2体积大 |
| B.等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积Na2CO3多 |
| C.将石灰水加入NaHCO3溶液中不产生沉淀,加入Na2CO3溶液中产生白色沉淀 |
| D.等物质的量浓度的两种溶液,Na2CO3溶液的碱性弱于NaHCO3溶液 |
您最近一年使用:0次
解题方法
6 . 下列有关说法中正确的是
A.可用 与 与 反应制取 反应制取 气体 气体 |
| B.钠在氯气中燃烧时产生大量的白雾 |
C.相同温度下, 的溶解度小于 的溶解度小于 的溶解度 的溶解度 |
| D.氧化铁是铁锈的主要成分,因此氧化铁俗称为铁锈 |
您最近一年使用:0次
7 . 我国化学家侯德榜发明了联合制碱法,为世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已略去)。

(1)①~③所涉及的操作方法中,包含过滤的是___________ (填序号)。
(2)根据上图,将化学方程式补充完整: NH3 + CO2 +___________ +___________ = NaHCO3↓+ NH4Cl
(3)煅烧NaHCO3固体的化学方程式是___________ 。
(4)下列说法中,正确的是_____ (填字母)。
A. CO2可循环使用 B. NH4Cl副产物可用作肥料 C. 溶液B中一定含有Na+、NH 、Cl-
、Cl-
(5)同学们将Na2CO3和NaHCO3固体分别配制成0.5 mol·L-1的溶液,设计如下方案并对反应现象作出预测:

(1)①~③所涉及的操作方法中,包含过滤的是
(2)根据上图,将化学方程式补充完整: NH3 + CO2 +
(3)煅烧NaHCO3固体的化学方程式是
(4)下列说法中,正确的是
A. CO2可循环使用 B. NH4Cl副产物可用作肥料 C. 溶液B中一定含有Na+、NH
 、Cl-
、Cl-(5)同学们将Na2CO3和NaHCO3固体分别配制成0.5 mol·L-1的溶液,设计如下方案并对反应现象作出预测:
| 实验方案 | 预测现象 | 预测依据 |
| 操作1:向2 mLNa2CO3溶液中滴加1 mL 0.5 mol·L-1CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO 浓度较大,能与CaCl2发生反应 浓度较大,能与CaCl2发生反应 |
| 操作2:向2 mLNaHCO3溶液中滴加1 mL 0.5 mol·L-1CaCl2溶液 | 无白色沉淀 | NaHCO3溶液中的CO 浓度很小,不能与CaCl2反应 浓度很小,不能与CaCl2反应 |
您最近一年使用:0次
名校
解题方法
8 . 某小组同学进行 和
和 性质的探究,实验如下(夹持装置已略去,气密性已检验)。
性质的探究,实验如下(夹持装置已略去,气密性已检验)。
(1)实验I,能够证明 的热稳定性强于
的热稳定性强于 的证据是
的证据是___________ 。
(2)实验II,方框中为洗气装置,请将该装置补充完整__________ 。
(3)实验II,烧瓶中反应的化学方程式___________ 。
(4)实验II,试剂a为饱和 溶液,其作用是
溶液,其作用是___________ 。
(5)实验II,持续一段时间后,观察到饱和 溶液中有细小晶体析出,(该晶体成分与烧瓶中固体成分相同)用化学方程式表示产生细小晶体的原因:
溶液中有细小晶体析出,(该晶体成分与烧瓶中固体成分相同)用化学方程式表示产生细小晶体的原因:___________ 。
 和
和 性质的探究,实验如下(夹持装置已略去,气密性已检验)。
性质的探究,实验如下(夹持装置已略去,气密性已检验)。| 实验I | 实验II |
 |  |
 的热稳定性强于
的热稳定性强于 的证据是
的证据是(2)实验II,方框中为洗气装置,请将该装置补充完整
(3)实验II,烧瓶中反应的化学方程式
(4)实验II,试剂a为饱和
 溶液,其作用是
溶液,其作用是(5)实验II,持续一段时间后,观察到饱和
 溶液中有细小晶体析出,(该晶体成分与烧瓶中固体成分相同)用化学方程式表示产生细小晶体的原因:
溶液中有细小晶体析出,(该晶体成分与烧瓶中固体成分相同)用化学方程式表示产生细小晶体的原因:
您最近一年使用:0次
名校
解题方法
9 . 下列叙述正确的是
A. 的热稳定性比 的热稳定性比 强 强 | B.钢铁在潮湿空气中生锈主要是发生了化学腐蚀 |
C. 中加入过量的 中加入过量的 溶液可以得到 溶液可以得到 | D.高压钠灯可用于道路照明 |
您最近一年使用:0次
名校
10 . 将过量的CO2分别通入到①CaCl2溶液、②Na2SiO3溶液、③Ca(OH)2溶液、④饱和Na2CO3溶液中,最终有固体析出的是
| A.②④ | B.①②③ |
| C.①③④ | D.①②③④ |
您最近一年使用:0次



