名校
解题方法
1 . 下列各组反应,最终一定能得到白色沉淀的是( )
| A.向CaCl2溶液中通入少量CO2 |
| B.向CuSO4溶液中加入足量NaOH溶液 |
| C.向FeCl2溶液中加入足量NaOH溶液 |
| D.向MgSO4溶液中加入足量NaOH溶液 |
您最近一年使用:0次
2020-04-03更新
|
759次组卷
|
8卷引用:山西省应县第一中学2018-2019学年高一上学期第四次月考化学试题
19-20高一·浙江·阶段练习
解题方法
2 . 老师在做镁条在空气中燃烧。细心的同学发现,燃烧后的生成物除了白色粉末状固体以外,还有少量淡黄色固体。同学们查资料知道氧化镁与水只是微量反应,于是他们对淡黄白色固体进行了如下的探究:
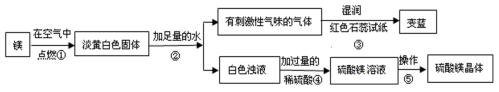
请回答下列的问题:
(1)镁在空气中燃烧的现象有:__________________________ 、_____________ 、有白色的烟、有淡黄白色固体生成;
(2)经查阅资料了解到,淡黄色固体为镁条和氮气反应生成的氮化镁(氮元素为-3价),根据上述反应现象写出氮化镁与水反应的化学方程式为:_____________ 。
(3)操作⑤包含的具体操作名称是:蒸发浓缩、______________ 。

请回答下列的问题:
(1)镁在空气中燃烧的现象有:
(2)经查阅资料了解到,淡黄色固体为镁条和氮气反应生成的氮化镁(氮元素为-3价),根据上述反应现象写出氮化镁与水反应的化学方程式为:
(3)操作⑤包含的具体操作名称是:蒸发浓缩、
您最近一年使用:0次
3 . 现有200 mL MgCl2和AlCl3混合溶液,其中Mg2+浓度0.2mol/L、Cl-浓度为1.3 mol/L。要使Mg2+转化成Mg(OH)2并使Mg2+、Al3+分离开来,至少需要4 mol/L NaOH溶液( )
| A.80mL | B.100mL | C.120mL | D.140mL |
您最近一年使用:0次
2019-03-17更新
|
424次组卷
|
8卷引用:【全国百强校】宁夏回族自治区银川一中2018-2019学年高一上学期12月阶段性测试化学试题
4 . 某课外活动小组探究镁与CO2、NO2的反应。
(1)实验发现点燃的镁条能在CO2气体中继续燃烧,产生黑、白两种固体,请用化学反应解释该现象_____________ 。
(2)该小组采用类比Mg与CO2反应的思路对Mg与NO2的反应进行预测:写出Mg与NO2反应的化学方程式_____________ 。
(3)设计实验验证猜测(用于连接玻璃管的乳胶管均内衬锡纸)
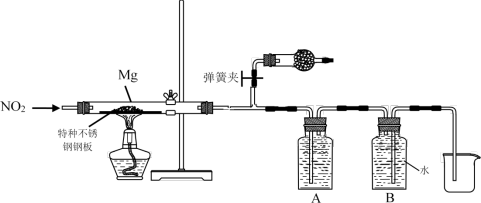
资料信息:2NO2 + 2NaOH = NaNO3 + NaNO2 + H2O
①装置A中的试剂是_____________ 。
②干燥管和装置B的作用分别是_____________ 、_____________ 。
③实验开始时正确的操作步骤是_____________ 。
a.通入NO2 b.打开弹簧夹
c.点燃酒精灯 d.当硬质玻璃管充满红综色气体后,关闭弹簧夹
(4)实验结束时,同学们观察到与预测相符合的现象,但当用水洗涤硬质玻璃管时,固体遇水产生有刺激性气味的气体,该气体能使湿润的石蕊试纸变蓝。
①同学们认为硬质玻璃管中还发生了另一个反应,该反应为_____________ ,
②请用化学方程式解释加水产生该气体的原因_____________ 。
(1)实验发现点燃的镁条能在CO2气体中继续燃烧,产生黑、白两种固体,请用化学反应解释该现象
(2)该小组采用类比Mg与CO2反应的思路对Mg与NO2的反应进行预测:写出Mg与NO2反应的化学方程式
(3)设计实验验证猜测(用于连接玻璃管的乳胶管均内衬锡纸)

资料信息:2NO2 + 2NaOH = NaNO3 + NaNO2 + H2O
①装置A中的试剂是
②干燥管和装置B的作用分别是
③实验开始时正确的操作步骤是
a.通入NO2 b.打开弹簧夹
c.点燃酒精灯 d.当硬质玻璃管充满红综色气体后,关闭弹簧夹
(4)实验结束时,同学们观察到与预测相符合的现象,但当用水洗涤硬质玻璃管时,固体遇水产生有刺激性气味的气体,该气体能使湿润的石蕊试纸变蓝。
①同学们认为硬质玻璃管中还发生了另一个反应,该反应为
②请用化学方程式解释加水产生该气体的原因
您最近一年使用:0次
2019-01-04更新
|
498次组卷
|
3卷引用:湖北省黄冈市罗田县第一中学2019届高三上学期12月月考理科综合化学试题
湖北省黄冈市罗田县第一中学2019届高三上学期12月月考理科综合化学试题鲁科版(2019)高一必修第一册第三章C 高考挑战区 过模拟 2年模拟精编精练(已下线)专题07 铝、镁及其化合物(限时精练)-2022年高三毕业班化学常考点归纳与变式演练
名校
解题方法
5 . 请回答:
(1)化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分解:2Mg5Al3(OH)19(H2O)4=27H2O↑+10MgO+3A12O3
①写出该化合物作阻燃剂的依据_______
②用离子方程式表示除去固体产物中Al2O3的原理_______ 。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由_______ 。
(3)铝的亲氧性,可表现在铝能夺取化合物中的氧,例如2Al+Fe2O3=Al2O3+2Fe.且反应放出大量的热,在冶金学上称为铝热反应。取少量铝热反应所得的固体混合物,将其溶于足量稀硫酸,滴加KSCN溶液无明显现象,_______ (填“能”或“不能”)说明固体混合物中无Fe2O3,理由是_______ 、_______ (用离子方程式说明)。
(1)化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分解:2Mg5Al3(OH)19(H2O)4=27H2O↑+10MgO+3A12O3
①写出该化合物作阻燃剂的依据
②用离子方程式表示除去固体产物中Al2O3的原理
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由
(3)铝的亲氧性,可表现在铝能夺取化合物中的氧,例如2Al+Fe2O3=Al2O3+2Fe.且反应放出大量的热,在冶金学上称为铝热反应。取少量铝热反应所得的固体混合物,将其溶于足量稀硫酸,滴加KSCN溶液无明显现象,
您最近一年使用:0次
2018-12-26更新
|
224次组卷
|
2卷引用:【全国百强校】山西省太原市第五中学2018-2019学年高一上学期12月月考化学试题
6 . 硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
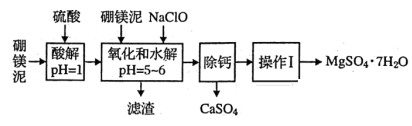
(1)实验中需用1mol/L的硫酸480mL,若用18.4mol/L的浓硫酸来配置,量取浓硫酸时需使用的量筒规格为( ) 。
A 10mL B 20mL C 50mL D 100mL
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl-还有一种离子也会被NaClO氧化,该反应的离子方程式为___________________________ ;滤渣中除含有氢氧化铁、氢氧化铝外还有_________ 。
(3)在“除钙”前需检验滤液中Fe3+是否被除尽,简述检验方法_____________________ 。
(4)已知硫酸镁、硫酸钙的溶解度如下表
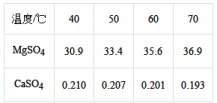
“除钙”是将;硫酸镁和硫酸钙混合溶液中的硫酸钙除去根据上表数据,采取的操作是_______________ 、趁热过滤、_________ 、____________ ,便得到比较纯净的硫酸镁。
(5)实验中提供的硼镁泥共100g,得到的MgSO4·7H2O为172.2g,则MgSO4·7H2O的产率为__________________ 。

(1)实验中需用1mol/L的硫酸480mL,若用18.4mol/L的浓硫酸来配置,量取浓硫酸时需使用的量筒规格为
A 10mL B 20mL C 50mL D 100mL
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl-还有一种离子也会被NaClO氧化,该反应的离子方程式为
(3)在“除钙”前需检验滤液中Fe3+是否被除尽,简述检验方法
(4)已知硫酸镁、硫酸钙的溶解度如下表

“除钙”是将;硫酸镁和硫酸钙混合溶液中的硫酸钙除去根据上表数据,采取的操作是
(5)实验中提供的硼镁泥共100g,得到的MgSO4·7H2O为172.2g,则MgSO4·7H2O的产率为
您最近一年使用:0次
2018-12-17更新
|
782次组卷
|
2卷引用:【校级联考】天津市静海区2019届高三上学期三校联考化学试题
10-11高一下·山东济宁·期末
名校
7 . 某溶液中可能含有大量的Mg2+、Al3+、H+、Cl-和少量OH-,向该溶液中逐滴加入0.5 mol·L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示,则可判断原溶液中( )
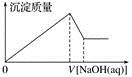

| A.有Mg2+,没有Al3+ |
| B.有Al3+,没有Mg2+ |
| C.有Mg2+和Al3+ |
| D.有大量的H+、Mg2+和Al3+ |
您最近一年使用:0次
2017-12-27更新
|
669次组卷
|
13卷引用:内蒙古巴彦淖尔市第一中学2017-2018学年高一12月月考化学试题(A卷)
内蒙古巴彦淖尔市第一中学2017-2018学年高一12月月考化学试题(A卷)内蒙古巴彦淖尔市第一中学2017-2018学年高一12月月考化学试题(B卷)吉林省实验中学2018届高三上学期第四次模拟考试化学试题安徽省肥东县高级中学2019届高三上学期9月调研考试化学试题贵州省息烽县一中2018-2019学年高一上学期期中考试化学试题陕西省咸阳市武功县普集高级中学2019-2020学年高一上学期第三次月考化学试题安徽省芜湖市无为市华星学校2020-2021学年高一上学期第二次月考化学试题(已下线)2010—2011学年山东省泗水一中高一下学期期末考试化学试卷【校级联考】江西省南昌市八一中学、洪都中学2018-2019学年高一上学期期末考试化学试题安徽省定远重点中学2018-2019学年高一下学期开学考试化学试题人教版高中化学必修1第三章《金属及其化合物》测试卷1广西龙州县高级中学2019-2020学年高一上学期期末考试化学试题云南省元江县一中2020-2021学年高一上学期期中考试化学试题
12-13高一上·广东中山·期末
名校
解题方法
8 . 某溶液中有Mg2+、 、
、 和
和 四种阳离子,若向其中加入过量的
四种阳离子,若向其中加入过量的 溶液,微热并搅拌,过滤,在滤渣中再加入过量的盐酸,所得溶液中大量增加的阳离子是
溶液,微热并搅拌,过滤,在滤渣中再加入过量的盐酸,所得溶液中大量增加的阳离子是
 、
、 和
和 四种阳离子,若向其中加入过量的
四种阳离子,若向其中加入过量的 溶液,微热并搅拌,过滤,在滤渣中再加入过量的盐酸,所得溶液中大量增加的阳离子是
溶液,微热并搅拌,过滤,在滤渣中再加入过量的盐酸,所得溶液中大量增加的阳离子是A. | B. | C. | D.Mg2+ |
您最近一年使用:0次
2017-03-21更新
|
324次组卷
|
13卷引用:2012-2013学年浙江乐清第二中学高一第二次(12月)月考化学试卷
(已下线)2012-2013学年浙江乐清第二中学高一第二次(12月)月考化学试卷2017届山东省桓台第二中学高三上学期第一次月考化学试卷2016-2017学年河北冀州中学高一12月月考文化学卷【全国百强校】河北省辛集中学2017-2018学年高二6月月考化学试题江西省赣州市赣县第三中学2018-2019学年高一上学期12月月考化学试题吉林省汪清县第六中学2021届高三第三次月考模拟化学试题河北省保定市唐县第一中学2021-2022学年高一下学期6月考试化学试题天津市第二十中学2022-2023学年高一上学期第二次统练化学试题(已下线)2011-2012学年广东省中山市高一上学期期末统一考试化学试卷2016-2017学年福建省安溪一中、养正中学、惠安一中、泉州实验中学高一上学期期末联考化学试卷2017-2018学年高一人教版必修一:17 铁的重要化合物课时训练化学试题安徽省滁州市定远县西片三校2017-2018学年高二上学期期末考试化学试题新疆乌鲁木齐市高级中学2023-2024学年高一上学期1月期末化学试题
9 . 在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.SiO2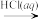 SiCl4 SiCl4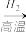 Si Si |
B.FeS2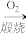 SO2 SO2 H2SO4 H2SO4 |
C.N2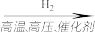 NH3 NH3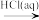 NH4Cl(aq) NH4Cl(aq) |
D.MgCO3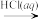 MgCl2(aq) MgCl2(aq)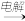 Mg Mg |
您最近一年使用:0次
2016-12-09更新
|
1482次组卷
|
32卷引用:2017届广西钦州港经济开发区中学高三上9月月考化学试卷
2017届广西钦州港经济开发区中学高三上9月月考化学试卷新疆生产建设兵团第二中学2016-2017学年高二下学期第四次月考化学试题广东省蓝精灵中学2018-2019学年高二上学期联考化学试题【全国百强校】福建省莆田市仙游县第一中学2018-2019学年高一下学期第一次月考(3月)化学试题湖南省长沙市雅礼中学2020届高三上学期第3次月考化学试题陕西省西安市第一中学2021届高三上学期第五次模拟考试化学试题16 2024年苏州第十中学高二3月月考2015-2016学年江苏省天一中学高二下学期期末化学试卷2016年全国普通高等学校招生统一考试化学(江苏卷精编版)2017届安徽省师大附中高三上学期期中化学试卷2016-2017学年湖北省蕲春县高二上学期期中化学试卷2017届江西师大附中高三上学期期中化学试卷安徽省师范大学附属中学2016-2017学年高一下学期期末考试化学试题2018版化学(苏教版)高考总复习专题一对接高考精练--物质的组成、性质及分类湖南省长沙市第一中学2018届高三上学期无机化合物综合练习(一)化学试题吉林省抚松五中 、 长白县实验中学、长白山二中、长白山实验中学2018届高三四盟校期中联考化学试题福建省福建师范大学第二附属中学2018届高三上学期期中考试化学试题(已下线)《考前20天终极攻略》-5月26日 元素及其化合物(已下线)解密06 非金属及其化合物(教师版)——备战2018年高考化学之高频考点解密(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第1讲 碳、硅及其无机非金属材料【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【教学案】(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第3讲 硫及其化合物 (教学案)(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第1讲 碳、硅及无机非金属材料 (教学案)(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第4讲 氮及其化合物 (教学案)(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(教学案)2016年全国普通高等学校招生统一考试化学(江苏卷参考版)(已下线)考点01 传统文化化学与生活化学基本概念——《备战2020年高考精选考点专项突破题集》(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)北京市第四中学2023-22024学年高一下学期期中考试 化学试题
10 . 向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如图,则原混合溶液中MgCl2与FeCl3的物质的量之比为
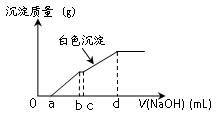

A.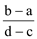 | B.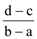 | C.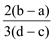 | D.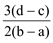 |
您最近一年使用:0次
2016-12-09更新
|
615次组卷
|
8卷引用:2011届上海市十校高三下学期第二次联考化学试卷
(已下线)2011届上海市十校高三下学期第二次联考化学试卷2014-2015内蒙古北方重工业集团三中高一下学期第一次月考化学试卷(已下线)2010年河北省正定中学高二第二学期期中考试化学试题(已下线)2010年上海市浦东新区高考预测化学卷(已下线)2013届上海市普陀区高三第一学期期末考试化学试卷苏教版2017届高三单元精练检测三化学试题苏教版2017届高三单元精练检测三化学试题人教版2017届高三单元精练检测三化学试题



