解题方法
1 . 某小组想通过实验探究 三种金属元素性质的递变规律。
三种金属元素性质的递变规律。
1.下表是元素周期表的一部分,将 三种元素填入相应位置
三种元素填入相应位置_______ 。
I.探究 分别与水反应的情况。
分别与水反应的情况。
实验①切一小块绿豆大小的金属 ,用滤纸吸干其表面的煤油,将其投入盛有
,用滤纸吸干其表面的煤油,将其投入盛有 水(含酚酞)的烧杯中。观察到
水(含酚酞)的烧杯中。观察到 与冷水发生剧烈反应,烧杯内溶液变红。
与冷水发生剧烈反应,烧杯内溶液变红。
2. 与
与 反应生成
反应生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式_______ 。该反应中作还原剂的是_______ 。
A. B.
B. C.
C.
3. 溶液中使酚酞试液变红的微粒是
溶液中使酚酞试液变红的微粒是_______ 。
A. B.
B. C.
C.
实验②分别取一小段镁条和铝条,放入两支试管中,向试管中各加入 水,再滴入2滴酚酞试液,观察到试管中均无明显现象。
水,再滴入2滴酚酞试液,观察到试管中均无明显现象。
有同学提出实验②的设计存在问题,故对实验②作如下调整:
实验③另取镁条和铝条,分别用砂纸打磨去除它们表面的氧化膜后,再进行以上实验操作并加热。观察到:未加热时,反应现象均不明显;加热后镁条表面有气泡生成,溶液变红;加热后 与水反应现象仍不明显。
与水反应现象仍不明显。
4.实验②的设计中未考虑到的因素是_______ 。
5.通过上述实验,得出 的金属性由强到弱顺序
的金属性由强到弱顺序_______ 。
A. B.
B.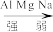
6.除反应物自身性质外,上述实验还验证了化学反应速率与_______ 有关。
Ⅱ.比较 碱性的强弱。
碱性的强弱。
实验④在试管中加入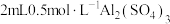 溶液,然后逐滴滴加
溶液,然后逐滴滴加 溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
实验⑤在试管中加入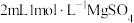 溶液,然后逐滴滴加
溶液,然后逐滴滴加 溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
7.写出由实验④、⑤的实验现象可推导得出的结论。
8.综上实验可知, 的碱性由强到弱顺序:
的碱性由强到弱顺序:_______ 。
A.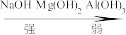 B.
B.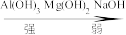
 三种金属元素性质的递变规律。
三种金属元素性质的递变规律。1.下表是元素周期表的一部分,将
 三种元素填入相应位置
三种元素填入相应位置H | |||
C | |||
I.探究
 分别与水反应的情况。
分别与水反应的情况。实验①切一小块绿豆大小的金属
 ,用滤纸吸干其表面的煤油,将其投入盛有
,用滤纸吸干其表面的煤油,将其投入盛有 水(含酚酞)的烧杯中。观察到
水(含酚酞)的烧杯中。观察到 与冷水发生剧烈反应,烧杯内溶液变红。
与冷水发生剧烈反应,烧杯内溶液变红。2.
 与
与 反应生成
反应生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式A.
 B.
B. C.
C.
3.
 溶液中使酚酞试液变红的微粒是
溶液中使酚酞试液变红的微粒是A.
 B.
B. C.
C.
实验②分别取一小段镁条和铝条,放入两支试管中,向试管中各加入
 水,再滴入2滴酚酞试液,观察到试管中均无明显现象。
水,再滴入2滴酚酞试液,观察到试管中均无明显现象。有同学提出实验②的设计存在问题,故对实验②作如下调整:
实验③另取镁条和铝条,分别用砂纸打磨去除它们表面的氧化膜后,再进行以上实验操作并加热。观察到:未加热时,反应现象均不明显;加热后镁条表面有气泡生成,溶液变红;加热后
 与水反应现象仍不明显。
与水反应现象仍不明显。4.实验②的设计中未考虑到的因素是
5.通过上述实验,得出
 的金属性由强到弱顺序
的金属性由强到弱顺序A.
 B.
B.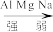
6.除反应物自身性质外,上述实验还验证了化学反应速率与
Ⅱ.比较
 碱性的强弱。
碱性的强弱。实验④在试管中加入
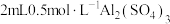 溶液,然后逐滴滴加
溶液,然后逐滴滴加 溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。
溶液至过量,边加边振荡。观察到试管中先出现白色沉淀后全部溶解。实验⑤在试管中加入
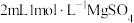 溶液,然后逐滴滴加
溶液,然后逐滴滴加 溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。
溶液至过量,边加边振荡。观察到试管中出现白色沉淀且不溶解。7.写出由实验④、⑤的实验现象可推导得出的结论。
实验序号 | 现象 | 结论 |
④ | 出现白色沉淀 |
|
沉淀全部溶解 | ||
⑤ | 出现白色沉淀 | |
沉淀不溶解 |
|
 的碱性由强到弱顺序:
的碱性由强到弱顺序:A.
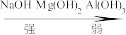 B.
B.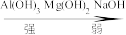
您最近一年使用:0次
名校
解题方法
2 . 将在空气中久置的铝片投入足量稀硫酸中,该铝片与稀硫酸反应产生氢气的速率与反应时间可用下图来表示(已知该反应为放热反应),请回答下列问题。
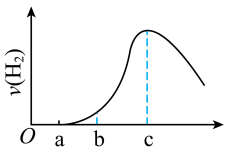
(1)曲线由 段,用离子方程式表示不产生氢气的原因
段,用离子方程式表示不产生氢气的原因___________ 。
(2)曲线由 段,产生氢气的速率较慢的原因
段,产生氢气的速率较慢的原因___________ 。
(3)曲线由 段,产生氢气的速率增加较快的主要原因
段,产生氢气的速率增加较快的主要原因___________ 。
(4)曲线由 以后,产生氢气的速率逐渐下降的主要原因
以后,产生氢气的速率逐渐下降的主要原因___________ 。
(5)下列措施能加快上述反应的化学反应速率的是___________

(1)曲线由
 段,用离子方程式表示不产生氢气的原因
段,用离子方程式表示不产生氢气的原因(2)曲线由
 段,产生氢气的速率较慢的原因
段,产生氢气的速率较慢的原因(3)曲线由
 段,产生氢气的速率增加较快的主要原因
段,产生氢气的速率增加较快的主要原因(4)曲线由
 以后,产生氢气的速率逐渐下降的主要原因
以后,产生氢气的速率逐渐下降的主要原因(5)下列措施能加快上述反应的化学反应速率的是___________
| A.把稀硫酸换成浓硫酸 | B.铝片改为铝粉 |
| C.加入少量硫酸铜溶液 | D.加入少量饱和硫酸钠溶液 |
您最近一年使用:0次
名校
解题方法
3 . 以下是有关铝的实验探究,请回答相关问题:
(1)用铝粉和 Fe2O3做铝热反应实验,需要的试剂还有___________。
(2)镁能发生和铝类似的“镁热反应”,写出镁在高温下和 Fe2O3反应的化学方程式___________ 。
(3)向集满CO2的铝制易拉罐中加入过量 NaOH 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪; 再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:___________ 。
(4)向铝粉中添加少量 NH4Cl固体并充分混合,将其加热到1000℃时可与 N₂反应制备 AlN,下列说法正确的是___________
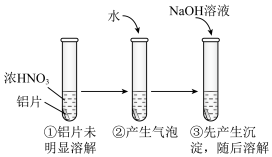
(5)用打磨过的铝片进行如下实验, 下列分析不合理的是___________
(6)为探究铝片(未打磨)与Na2CO3溶液的反应,实验如下:
下列说法不正确的是___________
(7)某铝土矿的主要成分为Al2O3·xH2O,还含有Fe2O3和 SiO2杂质。称取 17.50g铝土矿样品,加入 200mL1.65mol/L 的稀硫酸,恰好完全反应,过滤得沉淀0.30g,然后在滤液中加入足量的 NaOH 溶液,得到沉淀 2.14g。
①该试样中Fe2O3的物质的量为___________ mol。
② 样品中Al2O3·xH2O的x=__________ 。
(1)用铝粉和 Fe2O3做铝热反应实验,需要的试剂还有___________。
| A.KCl | B.KClO3 | C.MnO2 | D.Mg |
(2)镁能发生和铝类似的“镁热反应”,写出镁在高温下和 Fe2O3反应的化学方程式
(3)向集满CO2的铝制易拉罐中加入过量 NaOH 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪; 再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
(4)向铝粉中添加少量 NH4Cl固体并充分混合,将其加热到1000℃时可与 N₂反应制备 AlN,下列说法正确的是___________
| A.AlN是一种金属材料 |
| B.AlN与足量氢氧化钠溶液共热时生成氢氧化铝和氨气 |
| C.少量 NH4Cl能够破坏 Al表面的 Al2O3薄膜 |
| D.AlN与足量盐酸反应的离子方程式为AlN+3H+=Al3++NH3↑ |
(5)用打磨过的铝片进行如下实验, 下列分析不合理的是___________

| A.①中铝片发生了钝化 |
| B.②中产生的气泡是氮氧化合物,不是氢气 |
| C.③中沉淀溶解的离子方程式是Al(OH)3+OH-=[Al(OH)4]- |
| D.②中加水稀释过程中,仅发生了氧化还原反应 |
(6)为探究铝片(未打磨)与Na2CO3溶液的反应,实验如下:
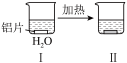 |  | |
| 无明显现象 | 铝片表面产生细小气泡 | 出现白色沉淀,产生大量气泡(经检验为H2和CO2) |
A.Na2CO3溶液中存在水解平衡:  |
| B.对比Ⅰ 、Ⅲ,推测 Na2CO3溶液能破坏铝表面的氧化膜 |
| C.Ⅳ溶液中可能存在大量 Al3+ |
D.推测出现白色浑浊的可能原因:[Al(OH)4]-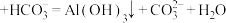 |
(7)某铝土矿的主要成分为Al2O3·xH2O,还含有Fe2O3和 SiO2杂质。称取 17.50g铝土矿样品,加入 200mL1.65mol/L 的稀硫酸,恰好完全反应,过滤得沉淀0.30g,然后在滤液中加入足量的 NaOH 溶液,得到沉淀 2.14g。
①该试样中Fe2O3的物质的量为
② 样品中Al2O3·xH2O的x=
您最近一年使用:0次
名校
4 . 为测定某种铝镁合金中铝的质量分数,探究小组进行了实验:称取质量为20g的合金,加入300g的稀盐酸,合金恰好被溶解,并产生了质量为2g的氢气。以下问题均需要写出计算过程:
(1)铝镁合金中铝的质量分数是多少_______ ?
(2)所用稀盐酸的溶质质量分数是多少_______ ?
(3)若要将反应后的溶液中的溶质全部转变为MgCl2,至少需要加入多少质量的镁_______ ?
(1)铝镁合金中铝的质量分数是多少
(2)所用稀盐酸的溶质质量分数是多少
(3)若要将反应后的溶液中的溶质全部转变为MgCl2,至少需要加入多少质量的镁
您最近一年使用:0次
名校
解题方法
5 . 按图所示方法来收集产生的气体,需将钠包好,再放入水中。取相同质量的钠按下列两种情况:
①用铝箔包住钠、②用铜箔包住钠。则收集产生的气体在相同条件下体积的关系是

①用铝箔包住钠、②用铜箔包住钠。则收集产生的气体在相同条件下体积的关系是

| A.二者收集气体一样多 | B.①收集气体体积较大 |
| C.②收集气体体积较大 | D.无法确定 |
您最近一年使用:0次
名校
6 . 铝与氧化铁混合后可称为铝热剂,以下混合物也能作为铝热剂的是
| A.氧化铝与铁 | B.氧化铝与四氧化三铁 |
| C.铝与氧化镁 | D.铝与五氧化二钒 |
您最近一年使用:0次
名校
解题方法
7 . 将铝与氧化铁混合制备单质铁的反应称为铝热反应,反应装置如图所示:

(1)空白处还需加入的试剂为___________ 。
(2)写出一种铝热反应的实际应用___________ 。

(1)空白处还需加入的试剂为
(2)写出一种铝热反应的实际应用
您最近一年使用:0次
8 . 用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断下列说法错误的是
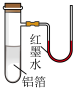

| A.实验中发生的反应都是氧化还原反应 | B.铝是一种较活泼的金属 |
| C.铝与氧气反应放出热量 | D.铝片上生成的白毛是氧化汞 |
您最近一年使用:0次
9 . 某古玩爱好者收藏的“商代铝碗”在“鉴宝”时被专家当场否定,其理由是
| A.铝的导热性较强,不易做碗 |
| B.铝的性质活泼,会与食物发生反应,不能做碗 |
| C.铝的质地较软,易变形,不易做碗 |
| D.铝的性质较活泼,难提炼,商代不可能有铝制品 |
您最近一年使用:0次
22-23高一下·上海浦东新·期末
名校
解题方法
10 . 铝单质加入氢氧化钠溶液中发生反应的离子方程式为_______ 。
您最近一年使用:0次

 的碱性比
的碱性比 无酸性
无酸性

