1 . 铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。
(1)铝粉和铁的氧化物(FeO-Fe2O3)可配成铝热剂用于焊接钢轨,反应的化学方程式是_______ 。
(2)以铝土矿(主要成分为Al2O3。含SiO2和Fe2O3等杂质)为原料生产铝和铵明矾晶体[NH4Al(SO4)2·12H2O]的一种工艺流程如下【已知:SiO2在“碱溶”时转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀】。

①实验前,要将铝土矿粉碎的目的是_______ 。
②用氧化物的形式表示铝硅酸钠的化学式_______ 。
③步骤②涉及到的离子方程式是:_______ 。
④写出利用Al2O3制备金属Al的化学方程式:_______ 。
⑤若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1:1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为_______ 。
(1)铝粉和铁的氧化物(FeO-Fe2O3)可配成铝热剂用于焊接钢轨,反应的化学方程式是
(2)以铝土矿(主要成分为Al2O3。含SiO2和Fe2O3等杂质)为原料生产铝和铵明矾晶体[NH4Al(SO4)2·12H2O]的一种工艺流程如下【已知:SiO2在“碱溶”时转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀】。

①实验前,要将铝土矿粉碎的目的是
②用氧化物的形式表示铝硅酸钠的化学式
③步骤②涉及到的离子方程式是:
④写出利用Al2O3制备金属Al的化学方程式:
⑤若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1:1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为
您最近一年使用:0次
2018-07-16更新
|
1314次组卷
|
2卷引用:【全国百强校】山西省临汾第一中学2017-2018学年高一下学期期末考试化学试题
名校
解题方法
2 . MnCO3是信息产业和机电工业的重要基础功能材料,某地有含锰矿石(主要成分是MnO2还含CaO、Al2O3、FeS等杂质),由此矿石生产MnCO3的工艺流程如下:
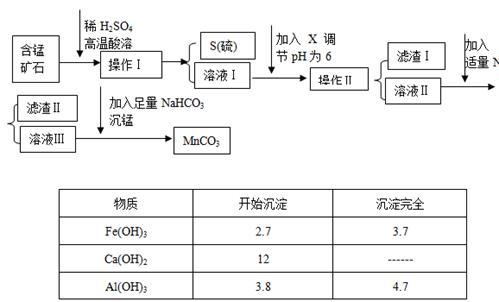
回答下列问题:
(1)操作Ⅰ为:___________ 。
(2)取溶液Ⅰ加入KSCN溶液,溶液呈血红色,试写出酸溶过程中FeS发生反应的离子方程式:
(3)调节溶液pH所用物质X最好为( )
(4)滤渣Ⅰ为___________ ,滤渣Ⅱ为___________ 。
(5)沉锰的化学方程式为:______________________ 。
(6)MnCO3也是制造锂离子电池的重要原料,在此电池的正极,充放电过程中发生LiMn2O4与Li1-xMn2O4之间的转化,写出该电池充电时正极发生的反应式:________ 。

回答下列问题:
(1)操作Ⅰ为:
(2)取溶液Ⅰ加入KSCN溶液,溶液呈血红色,试写出酸溶过程中FeS发生反应的离子方程式:
(3)调节溶液pH所用物质X最好为
| A.NaOH溶液 | B.氨水 | C.MnCO3固体 | D.盐酸 |
(4)滤渣Ⅰ为
(5)沉锰的化学方程式为:
(6)MnCO3也是制造锂离子电池的重要原料,在此电池的正极,充放电过程中发生LiMn2O4与Li1-xMn2O4之间的转化,写出该电池充电时正极发生的反应式:
您最近一年使用:0次
2016-03-17更新
|
665次组卷
|
2卷引用:2016届山西省忻州一中等四校高三下第三次联考理综化学试卷



