1 .  含镁、铝、铜的粉末分为两等份,一份与过量氢氧化钠溶液反应得到
含镁、铝、铜的粉末分为两等份,一份与过量氢氧化钠溶液反应得到 (标准状况),另一份与过量盐酸反应得到
(标准状况),另一份与过量盐酸反应得到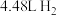 (标准状况),该粉末中镁、铝、铜的物质的量之比为
(标准状况),该粉末中镁、铝、铜的物质的量之比为
 含镁、铝、铜的粉末分为两等份,一份与过量氢氧化钠溶液反应得到
含镁、铝、铜的粉末分为两等份,一份与过量氢氧化钠溶液反应得到 (标准状况),另一份与过量盐酸反应得到
(标准状况),另一份与过量盐酸反应得到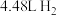 (标准状况),该粉末中镁、铝、铜的物质的量之比为
(标准状况),该粉末中镁、铝、铜的物质的量之比为A. | B. | C.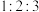 | D.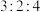 |
您最近一年使用:0次
2024-02-14更新
|
218次组卷
|
4卷引用:江苏省常州市第二中学2023-2024学年高一上学期第二次学情检测化学试题
名校
2 . 下列各组离子,在指定溶液中一定能大量共存的是
A.无色溶液中: 、K+、Cl-、Cu2+ 、K+、Cl-、Cu2+ |
B.某酸性溶液中:Cl-、 、Mg2+、 、Mg2+、 |
C.加入铝片能产生氢气的溶液中:Na+、K+、 、Cl- 、Cl- |
D.含有大量Ba2+的溶液中:Cl-、K+、OH-、 |
您最近一年使用:0次
2024-02-13更新
|
129次组卷
|
2卷引用:河北省郑口中学2023-2024学年高一上学期第四次质量检测化学试卷
解题方法
3 . 将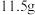 钠、
钠、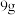 铝、
铝、 铁分别投入
铁分别投入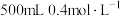 的盐酸中,结果正确的是
的盐酸中,结果正确的是
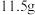 钠、
钠、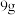 铝、
铝、 铁分别投入
铁分别投入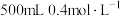 的盐酸中,结果正确的是
的盐酸中,结果正确的是| A.钠与盐酸反应最剧烈,反应后产生的气体最多 |
| B.铝与盐酸反应后,铝完全溶解,固体无剩余 |
C.铁与盐酸反应后, 的浓度为 的浓度为 |
| D.电子转移数:铁比铝多 |
您最近一年使用:0次
名校
4 . 下列各组离子在给定溶液中一定能大量共存的是
A.澄清透明的溶液:K+、 、Cl-、Cu2+ 、Cl-、Cu2+ |
B.使紫色石蕊变红的溶液:Na+、ClO-、 、K+ 、K+ |
C.使无色酚酞变红的溶液:Fe2+、 、Ca2+、Cl- 、Ca2+、Cl- |
D.加入铝粉能产生氢气的溶液:K+、 、Cl-、Na+ 、Cl-、Na+ |
您最近一年使用:0次
名校
5 . 研究合金的成分、性质与应用具有重要意义。由钠、镁、铝、锌四种金属单质中的两种金属组成的合金共4.8g,与足量的稀硫酸反应产生2.24L氢气(标准状况),则合金中一定含有的金属是
| A.Na | B.Zn | C.Al | D.Mg |
您最近一年使用:0次
6 . 把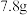 镁铝合金的粉末放入过量的盐酸中,得到
镁铝合金的粉末放入过量的盐酸中,得到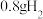 。下列说法错误的是
。下列说法错误的是
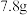 镁铝合金的粉末放入过量的盐酸中,得到
镁铝合金的粉末放入过量的盐酸中,得到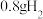 。下列说法错误的是
。下列说法错误的是A.合金中铝的质量分数约为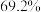 | B.合金中镁和铝的物质的量之比为 |
C.镁和铝还原出的 体积之比为 体积之比为 | D.在标准状况下,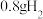 的体积为 的体积为 |
您最近一年使用:0次
名校
解题方法
7 . 某溶液与Al反应能放出H2,下列离子在该溶液中一定能大量共存的是
A.NH 、Fe2+、Cl−、SO 、Fe2+、Cl−、SO | B.Na+、K+、Cl−、SO |
C.Mg2+、Ag+、Cl−、NO | D.K+、Ca2+、HCO 、Cl− 、Cl− |
您最近一年使用:0次
名校
8 . 钢铁和铝合金已经成为大量使用的金属材料,下列说法不正确 的是
A.不铩钢中合金元素主要是 和 和 ,具有很强的抗腐蚀性能 ,具有很强的抗腐蚀性能 |
| B.铝表面容易生成一层致密的氧化铝保护膜 |
C.等物质的量的两份铝粉,分别放入足量的盐酸和氢氧化钠溶液中,放出的 在同温同压下体积之比为 在同温同压下体积之比为 |
D.赤铁矿主要成分是 ,磁铁矿的主要成分是 ,磁铁矿的主要成分是 , , 俗称铁红 俗称铁红 |
您最近一年使用:0次
9 . 合金已成为飞机制造、化工生产等行业的重要材料。某研究性学习小组的同学,为测定某含镁40%~60%的铝镁合金(不含其他元素) 中铝的质量分数,设计下列两种不同的实验方案进行探究。回答下列问题。
方案一:
(1)研究小组同学准备用 NaOH 固体配制240mL1.0 的NaOH溶液。
的NaOH溶液。
①本实验必须用到的玻璃仪器有:量筒、胶头滴管、烧杯、___________ 。
②要配制出此溶液,研究小组同学应用托盘天平称出___________ gNaOH。
③在配制过程中,小组同学的其他操作都是正确的,但下列操作中会引起所配制溶液浓度偏高的是___________ (填字母)。
A. NaOH固体在称量前已部分变质
B. 有少量NaOH溶液残留在烧杯里
C. 定容时,俯视容量瓶的刻度线
D. 定容摇匀后,发现溶液凹液面最低处低于刻度线,用胶头滴管补水至刻度线
(2)称取8.1g 铝镁合金粉末样品,溶于VmL1.0 的NaOH溶液中,充分反应,过滤、洗涤、干燥、称量固体,该步骤中若未洗涤固体,测得铝的质量分数将
的NaOH溶液中,充分反应,过滤、洗涤、干燥、称量固体,该步骤中若未洗涤固体,测得铝的质量分数将___________ (选填“偏高” “偏低”或“不受影响”)。
方案二:
将5.1g 铝镁合金与足量稀硫酸反应,测定生成气体的体积。
(3)同学们拟选用下图实验装置完成实验:
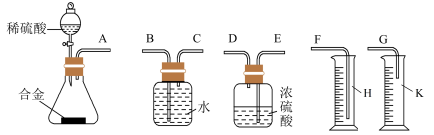
①你认为最简易的装置的连接顺序是:A接______,_______接______,______接______(填接口字母,可不填满)。___________
②实验结束时,在测量实验中生成氢气的体积时,你认为合理的是___________ (填字母)。
A.待实验装置冷却后再读数
B.上下移动量筒H,使其中液面与广口瓶中液面相平
C.视线与凹液面的最低点水平相切,读取量筒中水的体积
D.上下移动量筒K,使其中液面与广口瓶中液面相平
(4)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:
①稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;
②实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小,于是他们设计了如图所示的实验装置:
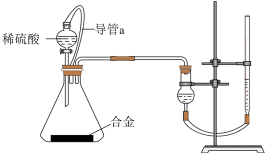
①装置中导管a的作用是___________
②实验后测得生成的氢气在标准状况下的体积为5.6 L,则铝的质量分数为___________ (请保留1位小数) 。
方案一:
(1)研究小组同学准备用 NaOH 固体配制240mL1.0
 的NaOH溶液。
的NaOH溶液。①本实验必须用到的玻璃仪器有:量筒、胶头滴管、烧杯、
②要配制出此溶液,研究小组同学应用托盘天平称出
③在配制过程中,小组同学的其他操作都是正确的,但下列操作中会引起所配制溶液浓度偏高的是
A. NaOH固体在称量前已部分变质
B. 有少量NaOH溶液残留在烧杯里
C. 定容时,俯视容量瓶的刻度线
D. 定容摇匀后,发现溶液凹液面最低处低于刻度线,用胶头滴管补水至刻度线
(2)称取8.1g 铝镁合金粉末样品,溶于VmL1.0
 的NaOH溶液中,充分反应,过滤、洗涤、干燥、称量固体,该步骤中若未洗涤固体,测得铝的质量分数将
的NaOH溶液中,充分反应,过滤、洗涤、干燥、称量固体,该步骤中若未洗涤固体,测得铝的质量分数将方案二:
将5.1g 铝镁合金与足量稀硫酸反应,测定生成气体的体积。
(3)同学们拟选用下图实验装置完成实验:

①你认为最简易的装置的连接顺序是:A接______,_______接______,______接______(填接口字母,可不填满)。
②实验结束时,在测量实验中生成氢气的体积时,你认为合理的是
A.待实验装置冷却后再读数
B.上下移动量筒H,使其中液面与广口瓶中液面相平
C.视线与凹液面的最低点水平相切,读取量筒中水的体积
D.上下移动量筒K,使其中液面与广口瓶中液面相平
(4)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:
①稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;
②实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小,于是他们设计了如图所示的实验装置:

①装置中导管a的作用是
②实验后测得生成的氢气在标准状况下的体积为5.6 L,则铝的质量分数为
您最近一年使用:0次
名校
10 . 镁铝合金(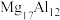 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为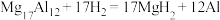 。得到的混合物Y(
。得到的混合物Y( )在一定条件下释放出氢气。在
)在一定条件下释放出氢气。在 溶液中,混合物Y能完全释放出
溶液中,混合物Y能完全释放出 。
。 完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出
完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出 的物质的量?
的物质的量?___________ (请写出简要的计算过程,必须列出关系式)
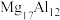 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为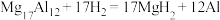 。得到的混合物Y(
。得到的混合物Y( )在一定条件下释放出氢气。在
)在一定条件下释放出氢气。在 溶液中,混合物Y能完全释放出
溶液中,混合物Y能完全释放出 。
。 完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出
完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出 的物质的量?
的物质的量?
您最近一年使用:0次



