解题方法
1 . 下列离子方程式书写正确的是
A.用食醋除去水垢中的碳酸钙: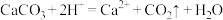 |
B.铜与浓硫酸加热条件下反应:4H++SO +Cu +Cu Cu2++SO2↑+2H2O Cu2++SO2↑+2H2O |
C.氯化铝溶液中加入过量氨水: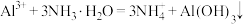 |
D.向酸性高锰酸钾溶液中滴加过氧化氢: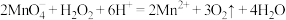 |
您最近一年使用:0次
名校
解题方法
2 . 下列指定反应的离子方程式正确的是
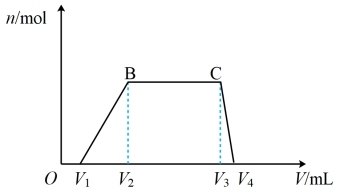
A.NH4HCO3溶液中加少量 NaOH 溶液: + + +2OH-= NH3 ↑+ +2OH-= NH3 ↑+  +2H2O +2H2O |
| B.AlCl3溶液中加入过量的氨水:Al3++3OH-=Al (OH)3↓ |
C.稀硫酸和氢氧化钡溶液反应:H++ +Ba2++OH- =BaSO4 ↓+ H2O +Ba2++OH- =BaSO4 ↓+ H2O |
D.过量氨水吸收工业尾气中的SO2: 2NH3·H2O+ SO2=2 + +  +2H2O +2H2O |
您最近一年使用:0次
2023-12-04更新
|
143次组卷
|
2卷引用:安徽省桐城中学2023-2024学年高一上学期第一次教学质量检测化学试题
名校
解题方法
3 . 下列反应中涉及的离子方程式书写正确的是
| A.铁发生吸氧腐蚀时的负极反应: Fe—3e-=Fe3+ |
B.将过量SO2通入NaClO溶液中: SO2 +H2O+ ClO-= HClO+  |
C.向AlCl3溶液中滴加过量氨水: Al3+ + 4NH3·H2O= 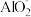 + 4 + 4 +2H2O +2H2O |
D.将少量NaHCO3溶液加入Ba(OH)2溶液中:  + OH-+ Ba2+ =H2O+ BaCO3↓ + OH-+ Ba2+ =H2O+ BaCO3↓ |
您最近一年使用:0次
名校
解题方法
4 . 探究氢氧化铝的两性,是适宜的试剂是
| A.Al、氨水、稀盐酸 |
B. 、氨水、稀盐酸 、氨水、稀盐酸 |
C. 溶液、NaOH溶液、稀盐酸 溶液、NaOH溶液、稀盐酸 |
D. 溶液、氨水、稀盐酸 溶液、氨水、稀盐酸 |
您最近一年使用:0次
解题方法
5 . 下列离子方程式书写正确的是
A.足量SO2通入 溶液中:SO2+2OH-= 溶液中:SO2+2OH-= +H2O +H2O |
B. 溶液中加入足量氨水: 溶液中加入足量氨水: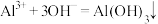 |
C.往 溶液中加入铜粉: 溶液中加入铜粉: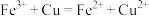 |
D. 溶液与 溶液与 反应: 反应: |
您最近一年使用:0次
名校
解题方法
6 . 能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合: |
B.将等物质的量浓度的 和 和 溶液以体积比1:2混合: 溶液以体积比1:2混合: |
C.硅酸钠溶液中通入二氧化碳: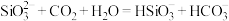 |
D.明矾溶液与过量氨水混合: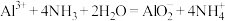 |
您最近一年使用:0次
2022-07-21更新
|
138次组卷
|
3卷引用:安徽省芜湖市第一中学2022-2023学年高一下学期3月份教学质量诊断测试化学试卷
名校
7 . 现有部分短周期元素的性质或原子结构如下表:
请用化学用语回答下列问题:
(1)Y元素符号是___________ ,W在周期表中的位置是___________ 。
(2)元素X与元素Z相比,非金属性较强的是___________ (填元素符号),写出一个能表示X、Z非金属性强弱关系的化学反应方程式:___________ 。
(3)写出实验室制取Y的最高价氧化物对应水化物的离子方程式:___________ 。
(4)ZX2和W2按照体积比1:1充分混合后,再通入品红溶液中,观察到的实验现象是___________ ,其原因是___________ (用离子方程式表示)。
| X | X原子的L层电子数是K层电子数的3倍 |
| Y | Y存在质量数为27,中子数为14的核素 |
| Z | Z原子的L层电子数是K层和M层电子数之和 |
| W | 常温下,W的单质为黄绿色气体 |
(1)Y元素符号是
(2)元素X与元素Z相比,非金属性较强的是
(3)写出实验室制取Y的最高价氧化物对应水化物的离子方程式:
(4)ZX2和W2按照体积比1:1充分混合后,再通入品红溶液中,观察到的实验现象是
您最近一年使用:0次
2021-09-19更新
|
82次组卷
|
2卷引用:安徽省合肥艺术中学2020-2021学年高一下学期第一次调研考试化学试题
名校
解题方法
8 . 下列离子方程式的书写正确的是
| A.铜和稀硫酸反应:Cu + 2H+=Cu2++H2↑ |
B.NaHCO3溶液与HCl溶液反应:H++ =CO2↑+H2O =CO2↑+H2O |
| C.钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ |
D.氯化铝溶液中加入过量的氨水:Al3++4NH3·H2O= +4 +4 +2H2O +2H2O |
您最近一年使用:0次
2021-01-08更新
|
159次组卷
|
2卷引用:安徽省池州市江南中学2020-2021学年高一上学期期末考试化学试题
名校
解题方法
9 . 铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。
(1)可以用电镀法在钢制品上电镀铝,为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应消耗2mol NaOH时,所得气体的物质的量为_______ mol。
(2)双羟基铝碳酸钠[NaAl(OH)2CO3]是一种常用的抗酸药,它与胃酸反应的化学方程式为_______ 。
(3)如图是从铝土矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并生产AlN的工艺流程:
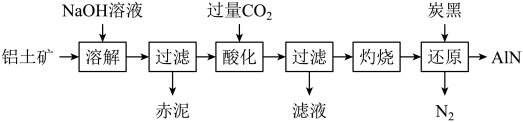
①“溶解”时,SiO2与NaOH溶液反应生成的硅酸钠与溶液中偏铝酸钠发生反应: ,“赤泥”的主要成分为
,“赤泥”的主要成分为_______ (写出化学式)。
②“酸化”时,通入过量CO2与NaAlO2反应,生成滤液的主要成分是_______ (写化学式)。
③“还原”时,炭黑在高温下被氧化为CO,反应的化学方程式为_______ 。
(4)1L某混合溶液,可能含有的离子如下表:
往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示。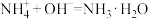
①该溶液中一定不含有的离子是_______ 。
②V1、V2、V3、V4之间的关系为_______ 。
(1)可以用电镀法在钢制品上电镀铝,为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应消耗2mol NaOH时,所得气体的物质的量为
(2)双羟基铝碳酸钠[NaAl(OH)2CO3]是一种常用的抗酸药,它与胃酸反应的化学方程式为
(3)如图是从铝土矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并生产AlN的工艺流程:

①“溶解”时,SiO2与NaOH溶液反应生成的硅酸钠与溶液中偏铝酸钠发生反应:
 ,“赤泥”的主要成分为
,“赤泥”的主要成分为②“酸化”时,通入过量CO2与NaAlO2反应,生成滤液的主要成分是
③“还原”时,炭黑在高温下被氧化为CO,反应的化学方程式为
(4)1L某混合溶液,可能含有的离子如下表:
| 可能大量含有的阳离子 | H+、Mg2+、Al3+、 |
| 可能大量含有的阴离子 | Cl-、 |
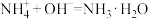

①该溶液中一定不含有的离子是
②V1、V2、V3、V4之间的关系为
您最近一年使用:0次
2020-11-19更新
|
1611次组卷
|
6卷引用:安徽省六安第一中学2023-2024学年高一上学期期末考试化学试题
名校
解题方法
10 . 下列表示对应化学反应的离子方程式正确的是
A.NaOH溶液与足量NaHCO3溶液反应:OH- + HCO = CO = CO + H2O + H2O |
B.Fe2(SO4)3溶液中加入足量Ba(OH)2溶液:Fe3+ + SO + Ba2+ + 3OH-=Fe(OH)3↓ + BaSO4↓ + Ba2+ + 3OH-=Fe(OH)3↓ + BaSO4↓ |
| C.碳酸钡中加入稀硫酸:BaCO3 + 2H+= Ba2+ + H2O + CO2↑ |
| D.氯化铝溶液与过量氨水反应 Al3+ + 3OH-=Al(OH)3↓ |
您最近一年使用:0次
2020-09-11更新
|
644次组卷
|
3卷引用:安徽省滁州市定远县育才学校2020-2021学年高一上学期期末考试化学试题



