20. 甘氨酸亚铁[(NH
2CH
2COO)
2Fe]是一种很好的补铁强化剂,易溶于水,人体吸收效果好。可用甘氨酸与FeCO
3反应制得:2NH
2CH
2COOH+FeCO
3→(NH
2CH
2COO)
2Fe+CO
2↑+H
2O。某学习小组在实验室中模拟了这一过程,请你根据学习小组的设计回答有关问题(已知有关物质性质如表):
| 甘氨酸 | 甘氨酸亚铁 |
| 易溶于水,微溶于乙醇,是两性化合物,氨基可被强氧化剂氧化 | 易溶于水,难溶于乙醇,易被氧化 |
I.制备FeCO
3装置如图所示(固定和夹持仪器省略)。
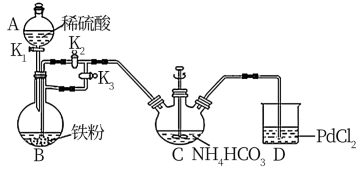
(1)仪器A的名称是
___。实验中先打开活塞K
1放入适量稀硫酸,关闭活塞K
2,打开活塞K
3,一段时间后再关闭活塞K
1,这样操作的目的是
___;然后关闭活塞K
3,打开活塞K
2,目的是
___。
(2)C中发生反应的离子方程式为
___。
II.制备甘氨酸亚铁。实验过程如下:
①将I中制得的FeCO
3充分洗净,取其0.2mol放回洗净的C瓶中(此时将搅拌器换成恒压漏斗)。装置如图所示(加热仪器、固定和夹持仪器省略)。

已知:H
2通入PdCl
2溶液中的反应:H
2+PdCl
2=Pd↓(黑色)+2HCl
②打开活塞K
1放入适量稀硫酸(铁粉足量),关闭活塞K
2,打开活塞K
3,一段时间后关闭活塞K
1。
③通过恒压漏斗向C中加入200mL1.0mol/L甘氨酸溶液,加热使反应物充分反应。
④反应结束后,过滤,在滤液中加入适量无水乙醇充分振汤再过滤、洗涤固体并干燥即得产品甘氨酸亚铁15.3g。
(3)过程④中加入无水乙醇的目的是
__。
(4)过程②中“一段时间后关闭活塞K
1”,是指观察到
___现象时关闭活塞K
1。
(5)本实验所得甘氨酸亚铁(甘氨酸亚铁摩尔质量:M=204g/mol)的产率是
___%。
(6为测定甘氨酸亚铁产品纯度,用酸性KMnO
4溶液滴定法测定样品中甘氨酸亚铁的Fe
2+的量,进而计算甘氨酸亚铁产品纯度,结果测出的产品纯度总是大于100%(假设杂质不与酸性KMnO
4溶液反应),导致误差的原因可能是
___。