名校
解题方法
1 . 下列离子方程式书写正确的是
| A.少量金属锌投入氯化铁溶液中:2Zn+3Fe3+=2Zn2++3Fe |
| B.向硫酸铝溶液中滴入少量氨水:Al3++3OH-=Al(OH)3↓ |
C.氢氧化镁与稀硫酸反应:Mg(OH)2+2H++ =MgSO4↓+2H2O =MgSO4↓+2H2O |
D.向NaHCO3溶液中加入少量Ba(OH)2溶液:Ba2++2OH-+2 =BaCO3↓+2H2O+ =BaCO3↓+2H2O+ |
您最近半年使用:0次
解题方法
2 . 明矾[KAl(SO4)2∙12H2O]在造纸、净水等方面应用广泛,实验室以铝灰为原料制备明矾的流程如下图所示,

已知:①铝灰含Al、Al2O3和少量FeO、Fe2O3、SiO2;
②SiO2不溶于强酸;
③不同温度KAl(SO4)2∙12H2O的溶解度:
回答下列问题:
(1)“酸浸”后溶液中主要的金属离子有Fe3+、___________ 。“滤渣Ⅰ”的主要成分为___________ (填化学式)。
(2)①“氧化”过程中H2O2的作用是___________ (用离子方程式表示)。
②Fe2+的“氧化效率”与温度的关系如图所示,试解释温度过高,“氧化效率”降低的可能原因是___________ 。

(3)溶液的pH对铝、铁沉淀率的影响如图所示。“调pH”时应控制溶液的pH范围为___________ 。
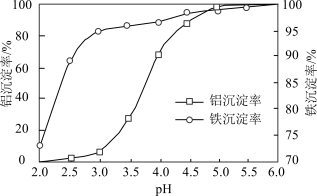
A.3.0~3.5 B.4.0~4.5 C.4.5~5.0
(4)“沉铝”中发生的离子方程式为___________ 。
(5)得到明矾晶体的“系列操作”包括___________ 、___________ 、过滤、洗涤、干燥。

已知:①铝灰含Al、Al2O3和少量FeO、Fe2O3、SiO2;
②SiO2不溶于强酸;
③不同温度KAl(SO4)2∙12H2O的溶解度:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
| KAl(SO4)2∙12H2O/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
(1)“酸浸”后溶液中主要的金属离子有Fe3+、
(2)①“氧化”过程中H2O2的作用是
②Fe2+的“氧化效率”与温度的关系如图所示,试解释温度过高,“氧化效率”降低的可能原因是

(3)溶液的pH对铝、铁沉淀率的影响如图所示。“调pH”时应控制溶液的pH范围为

A.3.0~3.5 B.4.0~4.5 C.4.5~5.0
(4)“沉铝”中发生的离子方程式为
(5)得到明矾晶体的“系列操作”包括
您最近半年使用:0次
名校
解题方法
3 . 根据如图所示的转化关系判断,下列说法正确的是(反应条件已略去)


A.生成等质量 时,①和②反应消耗 时,①和②反应消耗 |
B.反应③和④消耗等量的Al时,生成的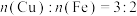 |
| C.反应③中氧化剂与还原剂的物质的量之比为2∶3 |
D.反应⑤的离子方程式为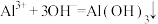 |
您最近半年使用:0次
2023-11-29更新
|
144次组卷
|
8卷引用:北京市石景山区2018届高三第一学期期末考试化学试题
名校
解题方法
4 . 下列有关反应的离子方程式书写错误的是
A.用小苏打治疗胃酸过多: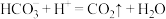 |
B.在碱性溶液中 与 与 反应生成 反应生成 : : |
C.向 溶液中滴加少量 溶液中滴加少量 溶液: 溶液: |
D.向 溶液中加入过量稀氨水: 溶液中加入过量稀氨水: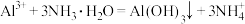 |
您最近半年使用:0次
2023-09-10更新
|
281次组卷
|
2卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高一上学期1月期末考试化学试题
名校
解题方法
5 . 以稀硫酸、NaOH和1mol Al为原料,用三种不同途径制取1mol Al(OH)3。
甲:Al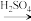 Al2(SO4)3
Al2(SO4)3 Al(OH)3
Al(OH)3
乙:Al NaAl(OH)4
NaAl(OH)4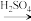 Al(OH)3
Al(OH)3
丙: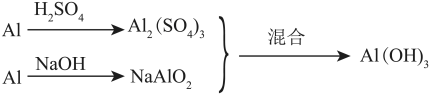
乙的第一步反应中的氧化剂是___________ 。消耗原料由多至少的方案顺序为___________ (用甲、乙、丙表示)。
甲:Al
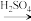 Al2(SO4)3
Al2(SO4)3 Al(OH)3
Al(OH)3乙:Al
 NaAl(OH)4
NaAl(OH)4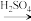 Al(OH)3
Al(OH)3丙:
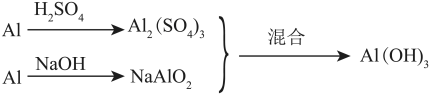
乙的第一步反应中的氧化剂是
您最近半年使用:0次
名校
解题方法
6 . 以下六种化合物中,不能通过化合反应直接生成的有
①Na2CO3 ②NaHCO3 ③Na2O2 ④Al(OH)3 ⑤FeCl3 ⑥Fe3O4
①Na2CO3 ②NaHCO3 ③Na2O2 ④Al(OH)3 ⑤FeCl3 ⑥Fe3O4
| A.1种 | B.2种 | C.3种 | D.4种 |
您最近半年使用:0次
2023-02-13更新
|
77次组卷
|
2卷引用:甘肃省金昌市永昌县第一高级中学2022-2023学年高一上学期期末考试化学试题
7 . 有下列物质:①硫酸 ② 溶液 ③
溶液 ③ ④小苏打 ⑤纯碱 ⑥
④小苏打 ⑤纯碱 ⑥ ⑦明矾。回答下列问题:
⑦明矾。回答下列问题:
(1)将上述物质按下图进行分类。
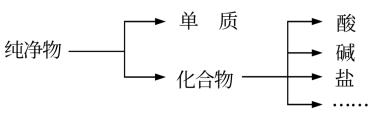
图中所示所属的分类方法为_______ 。
(2)纯碱是重要的化工原料之一,写出其在水中的电离方程式:_______ 。
(3)明矾 [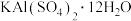 ]是常见的净水剂,属于
]是常见的净水剂,属于_______ (填“酸”“碱”或“盐”),实验室利用明矾制备 的离子方程式为
的离子方程式为_______ 。
(4)取 溶液做导电性实验,往烧杯中滴加
溶液做导电性实验,往烧杯中滴加 稀硫酸。装置如图1,测得溶液电导率如图2所示。
稀硫酸。装置如图1,测得溶液电导率如图2所示。

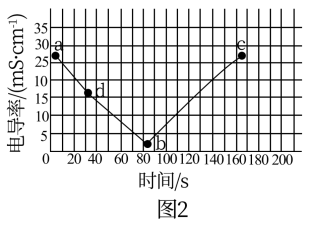
①由 过程中,可观察到的现象有
过程中,可观察到的现象有_______ ,发生反应的离子方程式为_______ 。
②b点时加入 溶液的体积为
溶液的体积为_______  。
。
 溶液 ③
溶液 ③ ④小苏打 ⑤纯碱 ⑥
④小苏打 ⑤纯碱 ⑥ ⑦明矾。回答下列问题:
⑦明矾。回答下列问题:(1)将上述物质按下图进行分类。

图中所示所属的分类方法为
(2)纯碱是重要的化工原料之一,写出其在水中的电离方程式:
(3)明矾 [
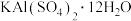 ]是常见的净水剂,属于
]是常见的净水剂,属于 的离子方程式为
的离子方程式为(4)取
 溶液做导电性实验,往烧杯中滴加
溶液做导电性实验,往烧杯中滴加 稀硫酸。装置如图1,测得溶液电导率如图2所示。
稀硫酸。装置如图1,测得溶液电导率如图2所示。

①由
 过程中,可观察到的现象有
过程中,可观察到的现象有②b点时加入
 溶液的体积为
溶液的体积为 。
。
您最近半年使用:0次
2022-01-24更新
|
91次组卷
|
2卷引用:广东省茂名高州市2021-2022学年高一上学期期末考试化学试题
解题方法
8 . 能正确表示下列化学反应的离子方程式的是
A.硝酸银溶液与铜反应: |
B.氢氧化钡溶液与稀硝酸反应: |
C.向氯化铝溶液中滴加氨水: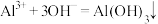 |
D.铁粉与稀盐酸反应制备氢气: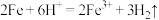 |
您最近半年使用:0次
9 . 用氧化铝为原料来制取氢氧化铝的最好的方法是
| A.将氧化铝粉末溶于水 | B.将氧化铝粉末溶于盐酸,再滴加氢氧化钠溶液 |
| C.将氧化铝粉末溶于盐酸中,再滴加氨水 | D.将氧化铝粉末溶于氢氧化铝溶液中,再滴加盐酸 |
您最近半年使用:0次
名校
解题方法
10 . 铝是地壳中含量最多的金属元素,铝及其化合物在生产和生活中有广泛的用途,请回答下列问题:
(1)我们知道,铝是一种活泼的金属,在常温下就能与空气中的氧气反应,但在日常生活中铝制品却司空见惯,原因是_______ ,铝制器皿无论盛放酸性或碱性溶液,均会被腐蚀,请写出铝与烧碱溶液发生反应的离子方程式:_______ 。
(2)高纯氧化铝常被用作荧光粉基体材料,制备高纯氧化铝要用化学方法,其中一种方法是将 溶液中的铝沉淀出来,再将生成的沉淀经脱水制得氧化铝。为完全沉淀
溶液中的铝沉淀出来,再将生成的沉淀经脱水制得氧化铝。为完全沉淀 溶液中的铝元素,可采用的方法是
溶液中的铝元素,可采用的方法是_______ 。
(3)胃舒平的有效成分是氢氧化铝,是治疗胃酸(盐酸)过多的常用药物,胃舒平治疗胃酸过多的原理是_______ (用离子方程式表示),小苏打片也可以治疗胃酸过多,小苏打片发挥功效的离子方程式为_______ 。

(1)我们知道,铝是一种活泼的金属,在常温下就能与空气中的氧气反应,但在日常生活中铝制品却司空见惯,原因是
(2)高纯氧化铝常被用作荧光粉基体材料,制备高纯氧化铝要用化学方法,其中一种方法是将
 溶液中的铝沉淀出来,再将生成的沉淀经脱水制得氧化铝。为完全沉淀
溶液中的铝沉淀出来,再将生成的沉淀经脱水制得氧化铝。为完全沉淀 溶液中的铝元素,可采用的方法是
溶液中的铝元素,可采用的方法是(3)胃舒平的有效成分是氢氧化铝,是治疗胃酸(盐酸)过多的常用药物,胃舒平治疗胃酸过多的原理是

您最近半年使用:0次
2021-01-28更新
|
235次组卷
|
3卷引用:山西省2020-2021学年高一上学期期末考试化学试题
山西省2020-2021学年高一上学期期末考试化学试题山西省长治市第一中学2020-2021学年高一上学期期末测试试题(已下线)3.2.1 铁合金 铝和铝合金 新型合金-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)



