解题方法
1 . 生活离不开化学,生活中有许多中学化学常见的物质,它们的主要成分如下表:
回答下列问题:
(1) 中所含化学键类型为
中所含化学键类型为___________ (填“离子键”或“共价键”)。
(2)明矾可用来制备氢氧化铝,请选择与之反应的最佳试剂:___________ (填“氨水”或“氢氧化钠溶液”)。
(3) 的电离方程式为
的电离方程式为___________ 。
(4) 溶液中混有少量
溶液中混有少量 ,可加适量的
,可加适量的 溶液除杂,离子方程式为
溶液除杂,离子方程式为___________ , 固体中若含有少量
固体中若含有少量 固体,可采取的除杂方法为
固体,可采取的除杂方法为___________ 。
(5)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:___________ 。
(6) 属于
属于___________ 电解质(填“强”、“弱”或“非”)。
| 商品 | 食盐 | 明矾 | 84消毒液 |
| 主要成分 | ① | ② | ③ |
| 商品 | 发酵粉 | 白醋 | 洁厕灵 |
| 主要成分 | ④ | ⑤ | ⑥ |
(1)
 中所含化学键类型为
中所含化学键类型为(2)明矾可用来制备氢氧化铝,请选择与之反应的最佳试剂:
(3)
 的电离方程式为
的电离方程式为(4)
 溶液中混有少量
溶液中混有少量 ,可加适量的
,可加适量的 溶液除杂,离子方程式为
溶液除杂,离子方程式为 固体中若含有少量
固体中若含有少量 固体,可采取的除杂方法为
固体,可采取的除杂方法为(5)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:
(6)
 属于
属于
您最近一年使用:0次
名校
2 . 下列有关反应的离子方程式书写错误的是
A.用小苏打治疗胃酸过多: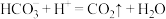 |
B.在碱性溶液中 与 与 反应生成 反应生成 : : |
C.向 溶液中滴 溶液中滴 溶液: 溶液: |
D.向 溶液中加入过量稀氨水: 溶液中加入过量稀氨水: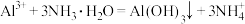 |
您最近一年使用:0次
名校
解题方法
3 . 下列有关电极方程式或离子方程式正确的是
A.以铜电极电解饱和食盐水的电解方程式:2Cl-+2H2O 2OH-+Cl2↑+H2↑ 2OH-+Cl2↑+H2↑ |
| B.铅蓄电池充电时的阳极反应:Pb2++2H2O-2e-=PbO2+4H+ |
C.少量SO2通入NaClO溶液:3ClO-+SO2+H2O= +2HClO+Cl- +2HClO+Cl- |
D.Al2(SO4)3溶液中加入过量氨水:Al3++4NH3·H2O=[Al(OH)4]-+4 |
您最近一年使用:0次
名校
4 . 下列离子方程式书写正确的是
A. 溶液腐蚀铜电路板: 溶液腐蚀铜电路板: |
B.氯气溶于水: |
C.硫酸亚铁溶液保存不当出现棕黄色沉淀: |
D.明矾溶液与过量氨水混合: |
您最近一年使用:0次
名校
解题方法
5 . 下列离子方程式书写正确的是
| A.少量金属锌投入氯化铁溶液中:2Zn+3Fe3+=2Zn2++3Fe |
| B.向硫酸铝溶液中滴入少量氨水:Al3++3OH-=Al(OH)3↓ |
C.氢氧化镁与稀硫酸反应:Mg(OH)2+2H++ =MgSO4↓+2H2O =MgSO4↓+2H2O |
D.向NaHCO3溶液中加入少量Ba(OH)2溶液:Ba2++2OH-+2 =BaCO3↓+2H2O+ =BaCO3↓+2H2O+ |
您最近一年使用:0次
6 . 实验室制备 沉淀,最适宜的方法是
沉淀,最适宜的方法是
 沉淀,最适宜的方法是
沉淀,最适宜的方法是A. 溶液中加入足量 溶液中加入足量 溶液 溶液 | B. 溶液中加入足量的氨水 溶液中加入足量的氨水 |
C. 与 与 溶液 溶液 | D. 溶于热水 溶于热水 |
您最近一年使用:0次
名校
解题方法
7 . 下列指定反应的离子方程式书写正确的是
A.氯气与水反应: |
B.将少量 通入 通入 溶液: 溶液: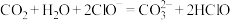 |
C.向 溶液中加入氨水至过量: 溶液中加入氨水至过量: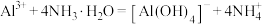 |
D.向 溶液中滴加 溶液中滴加 溶液至中性: 溶液至中性: |
您最近一年使用:0次
解题方法
8 . 明矾[KAl(SO4)2∙12H2O]在造纸、净水等方面应用广泛,实验室以铝灰为原料制备明矾的流程如下图所示,

已知:①铝灰含Al、Al2O3和少量FeO、Fe2O3、SiO2;
②SiO2不溶于强酸;
③不同温度KAl(SO4)2∙12H2O的溶解度:
回答下列问题:
(1)“酸浸”后溶液中主要的金属离子有Fe3+、___________ 。“滤渣Ⅰ”的主要成分为___________ (填化学式)。
(2)①“氧化”过程中H2O2的作用是___________ (用离子方程式表示)。
②Fe2+的“氧化效率”与温度的关系如图所示,试解释温度过高,“氧化效率”降低的可能原因是___________ 。

(3)溶液的pH对铝、铁沉淀率的影响如图所示。“调pH”时应控制溶液的pH范围为___________ 。
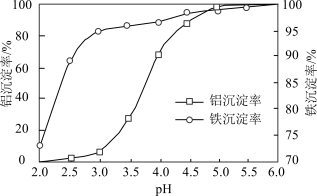
A.3.0~3.5 B.4.0~4.5 C.4.5~5.0
(4)“沉铝”中发生的离子方程式为___________ 。
(5)得到明矾晶体的“系列操作”包括___________ 、___________ 、过滤、洗涤、干燥。

已知:①铝灰含Al、Al2O3和少量FeO、Fe2O3、SiO2;
②SiO2不溶于强酸;
③不同温度KAl(SO4)2∙12H2O的溶解度:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
| KAl(SO4)2∙12H2O/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
(1)“酸浸”后溶液中主要的金属离子有Fe3+、
(2)①“氧化”过程中H2O2的作用是
②Fe2+的“氧化效率”与温度的关系如图所示,试解释温度过高,“氧化效率”降低的可能原因是

(3)溶液的pH对铝、铁沉淀率的影响如图所示。“调pH”时应控制溶液的pH范围为

A.3.0~3.5 B.4.0~4.5 C.4.5~5.0
(4)“沉铝”中发生的离子方程式为
(5)得到明矾晶体的“系列操作”包括
您最近一年使用:0次
解题方法
9 . 钠、镁、铝及其化合物具有重要用途,如钠在700~800℃时可将Ti从其氟化物中置换出来,MgO、 熔点很高,可作耐高温材料。将
熔点很高,可作耐高温材料。将 直接加热得MgO。工业上可从铝土矿(主要成分是
直接加热得MgO。工业上可从铝土矿(主要成分是 )中提取Al,主要步骤是将铝土矿溶于NaOH溶液,过滤得
)中提取Al,主要步骤是将铝土矿溶于NaOH溶液,过滤得 溶液,通入足量的
溶液,通入足量的 得
得 沉淀,
沉淀, 热分解得
热分解得 ,电解熔融
,电解熔融 得金属Al。下列物质间的转化在指定条件下表示正确的是
得金属Al。下列物质间的转化在指定条件下表示正确的是
 熔点很高,可作耐高温材料。将
熔点很高,可作耐高温材料。将 直接加热得MgO。工业上可从铝土矿(主要成分是
直接加热得MgO。工业上可从铝土矿(主要成分是 )中提取Al,主要步骤是将铝土矿溶于NaOH溶液,过滤得
)中提取Al,主要步骤是将铝土矿溶于NaOH溶液,过滤得 溶液,通入足量的
溶液,通入足量的 得
得 沉淀,
沉淀, 热分解得
热分解得 ,电解熔融
,电解熔融 得金属Al。下列物质间的转化在指定条件下表示正确的是
得金属Al。下列物质间的转化在指定条件下表示正确的是A.用 制取金属Mg: 制取金属Mg: |
B.用 溶液制取金属Al: 溶液制取金属Al: 溶液 溶液 |
C.铝土矿溶于NaOH溶液的化学方程式: |
D. 溶液中通入足量 溶液中通入足量 的离子方程式: 的离子方程式: |
您最近一年使用:0次
名校
解题方法
10 . 下列指定反应的离子方程式正确的是
A.NH4HCO3溶液中加少量 NaOH 溶液: + + +2OH-= NH3 ↑+ +2OH-= NH3 ↑+  +2H2O +2H2O |
| B.AlCl3溶液中加入过量的氨水:Al3++3OH-=Al (OH)3↓ |
C.稀硫酸和氢氧化钡溶液反应:H++ +Ba2++OH- =BaSO4 ↓+ H2O +Ba2++OH- =BaSO4 ↓+ H2O |
D.过量氨水吸收工业尾气中的SO2: 2NH3·H2O+ SO2=2 + +  +2H2O +2H2O |
您最近一年使用:0次
2023-12-04更新
|
143次组卷
|
2卷引用:云南省昆明市第八中学2023-2024学年高二上学期1月期末化学试题



