名校
1 . CuSO4、Fe2(SO4)3、H2SO4的混合溶液100 mL,已知溶液中阳离子的浓度相同,且SO42—的物质的量浓度为3 mol·L-1,则此溶液最多溶解铁粉的质量为
| A.5.6 g | B.11.2 g | C.22.4 g | D.33.6 g |
您最近一年使用:0次
2018-12-30更新
|
232次组卷
|
6卷引用:3.2 金属材料 期末备考复习 2023-2024学年高一上学期化学人教版(2019)必修第一册
2 . 将 14 g 铁粉溶于 1 L 稀硝酸中恰好完全反应,放出标准状况下 4.48 L NO 气体(假设是惟一还原产物),则原溶液中硝酸的浓度为
| A.1. 0 mol/L | B.0. 4 mol/L | C.0. 6 mol/L | D.0. 8 mol/L |
您最近一年使用:0次
2018-03-26更新
|
1004次组卷
|
4卷引用:山西省太原市2018届高三上学期期末考试化学试题
3 . 下列实验操作对应的实验现象及解释或结论不正确的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 将相同大小的金属钠分别投入乙醇和水中 | 乙醇与钠反应缓慢,水与钠反应剧烈 | 乙醇羟基中的氢原子不如水分子中的氢原子活泼 |
| B | 向 2 mL 1 mol/L NaOH 溶液中先加入3滴 1 mol/L MgCl2,再加入3滴 1 mol/L FeCl3 溶液 | 先生成白色沉淀,后生成红褐色沉淀 | 证明 Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| C | 将水蒸气通过灼热的铁粉 | 生成的气体可以点燃 | 铁与水蒸气在高温下发生反应 |
| D | 将刚摘下的红色花朵放入盛满干燥氯气的集气瓶中,盖上玻璃片 | 花朵褪色 | 因为次氯酸具有漂白作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-03-26更新
|
884次组卷
|
5卷引用:山西省太原市2018届高三上学期期末考试化学试题
名校
4 . 铁是应用最广泛的金属,铁的氯化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)请写出Fe与水蒸气反应的化学方程式:_____________ 。
(2)在实验室中,FeCl2可用铁粉和______ (填名称)反应制备。
(3)Fe3O4可用多种方法制得,其中由一种单质和一种化合物通过化合反应制备的化学方程式为______ 。
(4)红砖是用黏土高温烧结而成的,因其含有Fe2O3呈红色或棕红色而得名,常用作建筑材料。请设计一个简单实验证明红砖中含有Fe3+:_________________ 。
(5)现有一含有FeCl2 和FeCl3的混合物样品,实验测得n(Fe):n(C1)=1:2.1,则该样品中FeCl3的物质的量分数为_________ 。
(6)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:____________ 。
(1)请写出Fe与水蒸气反应的化学方程式:
(2)在实验室中,FeCl2可用铁粉和
(3)Fe3O4可用多种方法制得,其中由一种单质和一种化合物通过化合反应制备的化学方程式为
(4)红砖是用黏土高温烧结而成的,因其含有Fe2O3呈红色或棕红色而得名,常用作建筑材料。请设计一个简单实验证明红砖中含有Fe3+:
(5)现有一含有FeCl2 和FeCl3的混合物样品,实验测得n(Fe):n(C1)=1:2.1,则该样品中FeCl3的物质的量分数为
(6)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:
您最近一年使用:0次
名校
5 . 下列各组中的两种物质作用时,反应条件(温度、反应物用量等)改变,不会引起产物改变的是
| A.NaOH 和CO2 | B.Fe粉在Cl2中燃烧 |
| C.Na和O2 | D.NaOH容液和AlCl3溶液 |
您最近一年使用:0次
名校
解题方法
6 . 镁、铝、铁、铜四种金属粉末混合物,加入过量盐酸充分反应,过滤后向滤液中加入过量烧碱溶液,再过滤,滤液中存在的离子有
| A.Fe3+ | B.Cu2+ | C.Al3+ | D.AlO2- |
您最近一年使用:0次
2018-02-05更新
|
373次组卷
|
3卷引用:山西省大同市第一中学2017-2018学年高一上学期期末考试化学试题
7 . 下列通过实验观察得到的结论正确的是
| 选项 | 实验操作 | 结论 |
| A | AlCl3 溶液中逐滴滴加NaOH溶液至过量 | Al(OH)3 能溶于强碱溶液 |
| B | 铝、镁分别投入相同浓度的NaOH溶液 | 铝比镁更活泼 |
| C | 铝箔用酒精灯加热至熔化,轻轻晃动 | 铝单质熔点高 |
| D | 铁粉与水蒸气反应后固体加稀HCl溶解,再加KSCN溶液,溶液不变红 | 反应后固体中不含+3价的铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-01-31更新
|
369次组卷
|
2卷引用:山西省长治市第二中学2018-2019学年高一上学期期末考试化学试题
2012·湖北·一模
名校
8 . 已知FeS与某浓度的HNO3反应时生成Fe(NO3)3、H2SO4和某一单一的还原产物,若FeS和参与反应的HNO3的物质的量之比为1︰6,则该反应的还原产物是
| A.NO | B.NO2 | C.N2O | D.NH4NO3 |
您最近一年使用:0次
2017-11-09更新
|
568次组卷
|
6卷引用:2013届山西省平遥中学高三上学期12月质检考试化学试卷
(已下线)2013届山西省平遥中学高三上学期12月质检考试化学试卷(已下线)2012届湖北省普通高等学校招生5月适应性考试化学试卷(已下线)2012届北京市清华附中高三考前适应性训练理综化学试卷黑龙江省哈尔滨市第三中学2018届高三上学期(10月)第二次验收考试化学试题广东省清远市第一中学实验学校2020届高三第四次月考理综化学试题(已下线)上海市虹口区2014届高三三模化学试题
名校
9 . 同学们在实验室里用废铁屑(含少量铜)制取FeCl3·6H2O的流程如下。
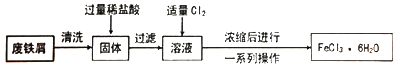
请回答下列问题。
(1)固体中加入过量稀盐酸时的现象是___________ 。
(2)溶液中通入Cl2时发生反应的化学方程式是______________ ,反应中Cl2表现出的性质是_________ ,此处的Cl2也可以用__________ 代替(填序号)。
A.H2O2 B.SO2 C.浓硫酸
(3)上述流程中由浓缩后的溶液获取FeCl3·6H2O的操作包括_____ 、过滤、洗涤。
(4)用FeCl3溶液制备Fe2O3,可向FeCl3溶液中滴加足量____________ ,然后过滤、洗涤、______ ,即可得到Fe2O3。
(5)FeCl3溶液能用作印制电路铜板的腐蚀液,FeCl3溶液与铜反应的离子方程式是______ ,反应一段时间后,取少量腐蚀液,向其中滴加_____ ,观察到_____ ,证明腐蚀液中任含Fe3+。此时腐蚀液中的金属阳离子是_______ 。

请回答下列问题。
(1)固体中加入过量稀盐酸时的现象是
(2)溶液中通入Cl2时发生反应的化学方程式是
A.H2O2 B.SO2 C.浓硫酸
(3)上述流程中由浓缩后的溶液获取FeCl3·6H2O的操作包括
(4)用FeCl3溶液制备Fe2O3,可向FeCl3溶液中滴加足量
(5)FeCl3溶液能用作印制电路铜板的腐蚀液,FeCl3溶液与铜反应的离子方程式是
您最近一年使用:0次
2017-02-27更新
|
270次组卷
|
2卷引用:2016-2017学年山西省太原市高一上学期期末考试化学试卷
10 . 下列物质能通过两种单质化合而成的是
| A.NO2 | B.CuCl2 | C.FeCl2 | D.SO3 |
您最近一年使用:0次



