解题方法
1 . 常温下,下列各组离子在指定溶液中能大量共存的是
A. 溶液: 溶液: 、 、 、 、 |
B. 稀硫酸: 稀硫酸: 、 、 、 、 |
C. 溶液: 溶液: 、 、 、 、 |
D. 溶液: 溶液: 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
2 . 常温下,下列各组离子在指定溶液中能大量共存的是
A.无色透明的溶液中: 、 、 、 、 、 、 |
B.能使甲基橙变红的溶液中: 、 、 、 、 、 、 |
C.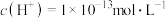 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.中性溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2022-09-08更新
|
218次组卷
|
2卷引用:福建省漳州市2023届高三毕业班9月第一次教学质量检测化学试卷
名校
解题方法
3 . 某研究性学习小组设计下列实验探究Zn和FeCl3溶液的反应,回答下列问题:
(1)由FeCl3固体配制未酸化的250mL0.5mol·L-1FeCl3溶液(pH=1.3),不需要使用的实验仪器有___________ (从下列图中选择,写出名称)。

(2)将Zn投入到未酸化的0.5mol·L-1FeCl3溶液(pH=1.3)中,在不同的实验条件下,实验现象如表:
①实验中产生的气体为___________ ,实验ii中产生气体的速率明显快于实验i,可能的原因是___________ (答出两点)。
②“滴加铁氰化钾溶液后,可见蓝色沉淀”说明混合溶液中存在Fe2+。生成Fe2+的离子方程式为___________ 。
(3)实验i和ii均先有气体生成,后有溶液颜色的变化。研究性学习小组猜想,可能是此实验条件下,氧化性:H+>Fe3+。
①为了检验上述猜想是否正确,查阅资料:可利用标准电极电势(用φθ表示)判断氧化性、还原性强弱,且电极电势越小,还原剂的还原性越强,已知(溶液中离子浓度的影响在此忽略不计):φθ(Fe3+ /Fe2+)=0.77 V,φθ (2H+ /H2)=0 V,φθ (Fe2+ /Fe)=—0.417 V,φθ (Zn2+ /Zn) =—0.76 V。则Fe3+、H+、Zn2+、Fe2+的氧化性大小关系为___________ 。
②研究小组进一步分析后,将锌粒改为锌粉,继续进行实验:
对比实验iii和iv,实验iv中“气泡不明显,红褐色褪色明显”的原因可能为___________ 。
③结合实验探究过程及现象分析,影响Zn与FeCl3溶液反应的条件有___________ (答两点即可的)。
(1)由FeCl3固体配制未酸化的250mL0.5mol·L-1FeCl3溶液(pH=1.3),不需要使用的实验仪器有

(2)将Zn投入到未酸化的0.5mol·L-1FeCl3溶液(pH=1.3)中,在不同的实验条件下,实验现象如表:
| 实验编号 | 条件 | 现象 |
| i | 锌粒18℃ | 刚开始无明显气泡,0.5min后有气体产生,一段时间后,溶液颜色加深。向反应后的溶液中滴加铁氰化钾溶液后,可见蓝色沉淀 |
| ii | 锌粒65℃ | 产生气泡较快,大约12 s后,气泡非常明显,溶液很快转为红棕色。较长时间后发现红棕色基本消失,最后产生红棕色沉淀 |
②“滴加铁氰化钾溶液后,可见蓝色沉淀”说明混合溶液中存在Fe2+。生成Fe2+的离子方程式为
(3)实验i和ii均先有气体生成,后有溶液颜色的变化。研究性学习小组猜想,可能是此实验条件下,氧化性:H+>Fe3+。
①为了检验上述猜想是否正确,查阅资料:可利用标准电极电势(用φθ表示)判断氧化性、还原性强弱,且电极电势越小,还原剂的还原性越强,已知(溶液中离子浓度的影响在此忽略不计):φθ(Fe3+ /Fe2+)=0.77 V,φθ (2H+ /H2)=0 V,φθ (Fe2+ /Fe)=—0.417 V,φθ (Zn2+ /Zn) =—0.76 V。则Fe3+、H+、Zn2+、Fe2+的氧化性大小关系为
②研究小组进一步分析后,将锌粒改为锌粉,继续进行实验:
| 实验编号 | 条件 | 现象 |
| iii | 锌粉18℃ 不振荡 | 大约3min可以看到明显的气泡,溶液颜色逐渐变深。向反应后的溶液中滴加铁氰化钾溶液后,可见蓝色沉淀 |
| iv | 锌粉65℃ 振荡 | 气泡不明显,红褐色褪色明显。向反应后的溶液中滴加铁氰化钾溶液后,可见蓝色沉淀 |
③结合实验探究过程及现象分析,影响Zn与FeCl3溶液反应的条件有
您最近一年使用:0次
2022-01-19更新
|
1229次组卷
|
5卷引用:福建省漳州市2022届高三毕业班第一次质量检测化学试题
福建省漳州市2022届高三毕业班第一次质量检测化学试题(已下线)一轮巩固卷8-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)(已下线)易错点06 铁及其化合物-备战2023年高考化学考试易错题福建省永安第九中学2022-2023学年高三上学期期中考试化学试题(已下线)专题六 金属元素及其化合物-实战高考·二轮复习核心突破
11-12高三上·上海闵行·阶段练习
名校
解题方法
4 . 易拉罐的主要成分为铝合金,其中以铝铁合金和铝镁合金最为常见。为确定铝合金中金属的成分,现取几小块易拉罐碎片进行下列实验,其中实验方案、现象与结论均正确的是
| 选项 | 实验方案 | 现象与结论 |
| A | 加入盐酸 | 产生无色气体,含铝、铁、镁三种金属 |
| B | 加入NaOH溶液 | 有无色气体产生,含有镁、铝两种金属 |
| C | 加入盐酸后,向所得溶液中再加入少量NaOH溶液 | 产生白色沉淀,一定只含有镁 |
| D | 用盐酸溶解并放置一会儿后,加入KSCN溶液 | 溶液呈血红色,含有铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-06更新
|
1616次组卷
|
20卷引用:福建省长泰县第一中学2020届高三上学期期初考试化学试题
福建省长泰县第一中学2020届高三上学期期初考试化学试题(已下线)2011届上海市闵行区高三上学期质量调研考试化学试卷2018版化学(苏教版)高考总复习课时跟踪训练:从铝土矿到铝合金甘肃省武威市第六中学2018届高三上学期第二次阶段性过关考试化学试题湖南省永州市祁阳县高考补习学校2018届高三上学期第二次月考化学试题(已下线)专题3.2 铝及其重要化合物(练)——2020年高考化学一轮复习讲练测(苏教版2019)必修第二册专题9 金属与人类文明 C 高考挑战区(已下线)考点14 铝及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点14 铝及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题03 铁 金属材料-2023年高考化学一轮复习小题多维练(全国通用)陕西省西安市长安区第一中学2017-2018学年高一上学期第二次月考化学(实验班)试题人教版(2019)高一必修第一册第三章 铁 金属材料 高考挑战区(已下线)3.2.1 合金-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)新人教必修1第3章第二节第1课时金属材料与合金(课后)(已下线)易错专题24 铝及其化合物的两性特点-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)广东省梅州市2021-2022学年高一上学期期末考试化学试题(已下线)3.2.1金属材料-同步学习必备知识广东省广州市第一中学2022-2023学年高一上学期期末考试化学试题广东省广州市真光中学2023-2024学年高一上学期12月阶段性测试化学试题陕西省西安市西安区县联考2023-2024学年高一上学期1月期末化学试题
名校
解题方法
5 . 下列反应的离子方程式书写正确的是
A. 溶液加入铁粉: 溶液加入铁粉: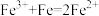 |
B. 溶液通入少量 溶液通入少量 : : |
C.二氧化硫使酸性高锰酸钾溶液褪色: |
D.往盛有水的烧杯中投入金属钠: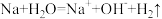 |
您最近一年使用:0次
2021-05-13更新
|
642次组卷
|
7卷引用:福建省漳州市2021届高中毕业班第三次教学质量检测化学试题
6 . 下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将红棕色气体通入淀粉-KI溶液 | 溶液变蓝 | 该气体为NO2 |
| B | 向盛有皂化反应后液体的烧杯中加入NaCl固体向 | 杯底出现白色沉淀 | 该物质为高级脂肪酸钠 |
| C | AgCl浊液中加入过量浓氨水 | 溶液变澄清 | AgCl属于强酸弱碱盐,显酸性 |
| D | 硫酸亚铁固体溶于稀硫酸溶液后,滴加KSCN溶液 | 溶液变为红色 | 硫酸亚铁固体发生了变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 下列有关物质的性质与用途具有对应关系的是
| A.NH3易溶于水,可用作制冷剂 |
| B.溴化银具有感光性,可用于照相机底片 |
| C.FeCl3具有氧化性,可用于自来水的杀菌消毒 |
| D.晶体硅的硬度大,可用于制作光电板 |
您最近一年使用:0次
8 . 某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究。查阅资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O。
实验探究一:学生甲利用如图所示装置进行实验,称量反应前后装置C中样品的质量,以确定样品的组成。回答下列问题:
(1)仪器组装完成后,夹好止水夹,__________________________________ ,则说明装置A的气密性良好。
(2)下列实验步骤中,正确的操作顺序是____________ (填序号)。
①打开止水夹;②熄灭C处的酒精喷灯;③C处冷却至室温后,关闭止水夹;④点燃C处的酒精喷灯;⑤收集氢气并验纯
实验探究二:
(3)学生乙取少量样品于烧杯中,加入过量稀硫酸,并作出如下假设和判断,结论正确的是______ 。
A.若固体全部溶解,说明样品中一定含有Fe2O3,一定不含有Cu2O
B.若固体部分溶解,说明样品中一定含有Cu2O,一定不含有Fe2O3
C.若固体全部溶解,再滴加KSCN溶液,溶液不变红色,说明样品一定含有Fe2O3和Cu2O
D.若固体全部溶解,再滴加KSCN溶液,溶液变红色,说明样品一定含有Fe2O3
另取少量样品于试管中,加入适量的浓硝酸,产生红棕色气体,证明样品中一定含有________ ,写出产生上述气体的化学方程式:____________________ 。
实验探究三:
(4)学生丙取一定量样品于烧杯中,加入足量的稀硫酸,反应后经过滤得到固体6.400g,测得滤液中Fe2+有2.000mol,则样品中n(Cu2O)=________________________ mol。
实验探究一:学生甲利用如图所示装置进行实验,称量反应前后装置C中样品的质量,以确定样品的组成。回答下列问题:
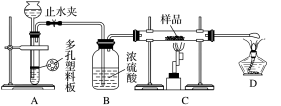
(1)仪器组装完成后,夹好止水夹,
(2)下列实验步骤中,正确的操作顺序是
①打开止水夹;②熄灭C处的酒精喷灯;③C处冷却至室温后,关闭止水夹;④点燃C处的酒精喷灯;⑤收集氢气并验纯
实验探究二:
(3)学生乙取少量样品于烧杯中,加入过量稀硫酸,并作出如下假设和判断,结论正确的是
A.若固体全部溶解,说明样品中一定含有Fe2O3,一定不含有Cu2O
B.若固体部分溶解,说明样品中一定含有Cu2O,一定不含有Fe2O3
C.若固体全部溶解,再滴加KSCN溶液,溶液不变红色,说明样品一定含有Fe2O3和Cu2O
D.若固体全部溶解,再滴加KSCN溶液,溶液变红色,说明样品一定含有Fe2O3
另取少量样品于试管中,加入适量的浓硝酸,产生红棕色气体,证明样品中一定含有
实验探究三:
(4)学生丙取一定量样品于烧杯中,加入足量的稀硫酸,反应后经过滤得到固体6.400g,测得滤液中Fe2+有2.000mol,则样品中n(Cu2O)=
您最近一年使用:0次
2018-08-28更新
|
443次组卷
|
6卷引用:福建省漳州市平和县第一中学2020届高三上学期第一次月考化学试题
9 . 下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | Fe3+有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
| B | 浓硫酸有腐蚀性 | 常温下浓硫酸不能用铁罐盛装 |
| C | Cl2是非金属单质 | Cl2能使湿润的有色布条褪色 |
| D | 熔融状态的Al2O3中有自由移动的Al3+和O2- | 电解熔融状态的Al2O3制备Al |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 生活中的一些问题常涉及到化学知识,则下列叙述不正确的是
| A.高温能杀死流感病毒是因为构成病毒的蛋白质受热变性 |
| B.明矾和漂白粉常用于自来水的净化,但两者的作用原理不相同 |
| C.氯化铁溶液可用于制作印刷电路板是因为其具有较强氧化性,能氧化单质铜 |
| D.“加碘食盐”、“含氟牙膏”、“富硒营养品”、“高钙牛奶”、“加铁酱油”等等,这里的碘、氟、硒指的是对应的单质分子,而钙、铁则分别指的是对应的钙离子和铁离子 |
您最近一年使用:0次
2016-12-09更新
|
507次组卷
|
4卷引用:2015届福建省长泰县一中高三上学期期末考试化学试卷



