解题方法
1 . 现有失去标签的 溶液和NaCl溶液,设计实验进行鉴别。已知①
溶液和NaCl溶液,设计实验进行鉴别。已知① 为弱酸:
为弱酸: 为白色固体,微溶于水②标准电极电势;
为白色固体,微溶于水②标准电极电势; ,
,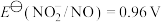 ,
,
 ,
, ,标准电极电势(
,标准电极电势( )越高,氧化剂的氧化性越强。分别取少量溶液进行实验,方案不可行的是
)越高,氧化剂的氧化性越强。分别取少量溶液进行实验,方案不可行的是
 溶液和NaCl溶液,设计实验进行鉴别。已知①
溶液和NaCl溶液,设计实验进行鉴别。已知① 为弱酸:
为弱酸: 为白色固体,微溶于水②标准电极电势;
为白色固体,微溶于水②标准电极电势; ,
,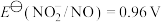 ,
,
 ,
, ,标准电极电势(
,标准电极电势( )越高,氧化剂的氧化性越强。分别取少量溶液进行实验,方案不可行的是
)越高,氧化剂的氧化性越强。分别取少量溶液进行实验,方案不可行的是| A.分别滴入几滴酚酞 |
B.分别滴加稀 溶液,再滴加稀硝酸 溶液,再滴加稀硝酸 |
C.分别滴加 酸化的KI溶液,再加入淀粉溶液 酸化的KI溶液,再加入淀粉溶液 |
D.分别滴加少许 溶液,加入 溶液,加入 酸化,再加入KSCN溶液 酸化,再加入KSCN溶液 |
您最近一年使用:0次
解题方法
2 . 将摩尔盐[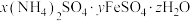 ]溶于水配成溶液,下列说法正确的是
]溶于水配成溶液,下列说法正确的是
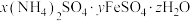 ]溶于水配成溶液,下列说法正确的是
]溶于水配成溶液,下列说法正确的是A.该溶液中还可大量共存 、 、 、 、 |
B.常温下该溶液中水电离出的 可能为 可能为 |
C.加入少量 后再滴入KSCN溶液,溶液变为红色,则证明溶液中含 后再滴入KSCN溶液,溶液变为红色,则证明溶液中含 |
D.向溶液中滴入 溶液使 溶液使 恰好沉淀时, 恰好沉淀时, 和 和 都会参与反应 都会参与反应 |
您最近一年使用:0次
2024·广东梅州·一模
解题方法
3 . 下列操作规范且能达到实验目的的是
|
|
|
|
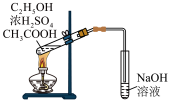
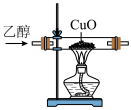
| A.证明碳酸的酸性强于苯酚 | B.制取乙酸乙酯 | C.检验 溶液中的 溶液中的 是否被氧化 是否被氧化 | D.检验乙醇具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 绚烂的颜色变化体现了化学之美。下列关于黄色 溶液叙述正确的是
溶液叙述正确的是
 溶液叙述正确的是
溶液叙述正确的是| A.滴入2~3滴紫色石蕊试液,溶液变成蓝色 |
| B.加入少量Cu粉,溶液变成浅绿色 |
C.滴入少量 溶液,出现白色沉淀 溶液,出现白色沉淀 |
D.滴入2~3滴 溶液,溶液变成红色 溶液,溶液变成红色 |
您最近一年使用:0次
2024-03-26更新
|
57次组卷
|
2卷引用:山东师范大学附属中学2024届高三下学期考前预测化学试题
名校
5 . 下列物质的鉴别或检验一定能达到实验目的的是
A.用饱和 溶液鉴别 溶液鉴别 溶液和 溶液和 溶液 溶液 |
B.用盐酸和KSCN溶液检验Fe粉中是否含有 |
C.用湿润的淀粉-KI试纸鉴别 和溴蒸气 和溴蒸气 |
D.向1-氯丁烷中加入硝酸酸化的 溶液检验氯元素 溶液检验氯元素 |
您最近一年使用:0次
2024-03-24更新
|
674次组卷
|
3卷引用:山东省烟台市2024届高三一模化学试题
6 . 某兴趣小组将过量Cu与 溶液充分反应,静置后取上层清液于试管中,将KSCN溶液滴加到清液中,瞬间产生白色沉淀,附近溶液出现红色;振荡试管,红色又迅速褪去。已知:
溶液充分反应,静置后取上层清液于试管中,将KSCN溶液滴加到清液中,瞬间产生白色沉淀,附近溶液出现红色;振荡试管,红色又迅速褪去。已知:
①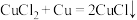 (白色)慢反应
(白色)慢反应
② 快反应
快反应
③ 是拟卤素,化学性质和氯气相似
是拟卤素,化学性质和氯气相似
下列说法正确的是
 溶液充分反应,静置后取上层清液于试管中,将KSCN溶液滴加到清液中,瞬间产生白色沉淀,附近溶液出现红色;振荡试管,红色又迅速褪去。已知:
溶液充分反应,静置后取上层清液于试管中,将KSCN溶液滴加到清液中,瞬间产生白色沉淀,附近溶液出现红色;振荡试管,红色又迅速褪去。已知:①
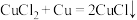 (白色)慢反应
(白色)慢反应②
 快反应
快反应③
 是拟卤素,化学性质和氯气相似
是拟卤素,化学性质和氯气相似下列说法正确的是
A.用KSCN溶液检验 时, 时, 的存在不会对检验产生干扰 的存在不会对检验产生干扰 |
B.局部出现红色主要是因为溶液中的 被空气中的 被空气中的 氧化成 氧化成 , , 与KSCN反应生成 与KSCN反应生成 |
C.白色沉淀是 ,是溶液中 ,是溶液中 与Cu反应生成的 与Cu反应生成的 |
D.红色迅速褪去的原因是振荡试管时 与 与 发生反应,从而使 发生反应,从而使 平衡逆向移动 平衡逆向移动 |
您最近一年使用:0次
7 . 下列物质的性质与用途对应关系错误的是
| A.氧化铝熔点高,可用作耐火材料 |
| B.青铜比纯铜熔点低、硬度大,古代用青铜铸剑 |
C. 具有还原性,可用于去除水体中的 具有还原性,可用于去除水体中的 |
| D.聚合硫酸铁铝能水解形成胶体,可用作净水剂 |
您最近一年使用:0次
名校
解题方法
8 . 根据下列实验操作和现象能得到相应结论的是
选项 | 操作和现象 | 结论 |
A | 向漂白粉溶液中通入SO2,产生白色沉淀 | 酸性:H2SO3>HClO |
B | 常温下,分别测定1 mol·L–1CH3COONH4溶液和0.1 mol·L–1 CH3COONH4溶液的pH,测得pH都等于7 | 同温下,不同浓度CH3COONH4溶液中水的电离程度相同 |
C | 10 mL 0.1 mol·L–1FeCl3溶液和10 mL 0.1 mol·L–1KI溶液充分反应后分成两等份,一份加入2滴KSCN溶液,溶液变红;另一份加入2滴淀粉溶液,溶液变蓝 | FeCl3和KI的反应存在限度 |
D | 向露置在空气中的Na2O2固体中加入稀盐酸,产生气泡 | Na2O2固体已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-09更新
|
319次组卷
|
2卷引用:山东省烟台市2023-2024学年高三上学期期末考试化学试题
名校
9 . 氯化铁在金属蚀刻、污水处理等方面有广泛应用。某兴趣小组以废铁屑为原料,用如图所示装置制备FeCl3·6H2O
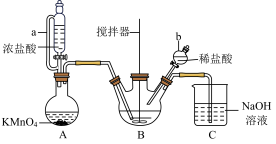
已知:FeCl3易溶于水、甲醇、乙醇,不溶于甘油。实验步骤如下:
I.废铁屑的净化:取一只小烧杯,放入约5g废铁屑,向其中注入15mLlmol/LNa2CO3溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
Ⅱ.FeCl2溶液的制备:将处理后的废铁屑加入装置B的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含FeCl2的混合液。
Ⅲ.FeCl3溶液的制备:由装置A制备氯气;向FeCl2的混合液中缓慢通入足量的氯气。
Ⅳ.FeCl3·6H2O产品的分离提纯:将三颈烧瓶中的FeCl3混合液转移出来,经蒸发浓缩、冷却结晶、过滤、洗涤、重结晶、干燥,得到FeCl3·6H2O产品。
Ⅴ.FeCl3·6H2O产品的纯度测定:用碘量法滴定并计算。
对于上述实验,下列有关装置仪器的说法不正确的是

已知:FeCl3易溶于水、甲醇、乙醇,不溶于甘油。实验步骤如下:
I.废铁屑的净化:取一只小烧杯,放入约5g废铁屑,向其中注入15mLlmol/LNa2CO3溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
Ⅱ.FeCl2溶液的制备:将处理后的废铁屑加入装置B的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含FeCl2的混合液。
Ⅲ.FeCl3溶液的制备:由装置A制备氯气;向FeCl2的混合液中缓慢通入足量的氯气。
Ⅳ.FeCl3·6H2O产品的分离提纯:将三颈烧瓶中的FeCl3混合液转移出来,经蒸发浓缩、冷却结晶、过滤、洗涤、重结晶、干燥,得到FeCl3·6H2O产品。
Ⅴ.FeCl3·6H2O产品的纯度测定:用碘量法滴定并计算。
对于上述实验,下列有关装置仪器的说法不正确的是
| A.装置B中,搅拌器的作用是使反应混合物充分接触 |
| B.装置A、B之间应加装一个盛有饱和食盐水的洗气瓶 |
| C.装置C中,NaOH溶液的作用是吸收逸出的氯气,防止污染空气 |
| D.仪器a和仪器b的功能相同,但操作方法不同 |
您最近一年使用:0次
2024-01-16更新
|
151次组卷
|
2卷引用:山东省青岛第二中学2023-2024学年高三上学期期中考试化学试卷
解题方法
10 . 实验探究是化学学科的魅力所在。下列有关实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向Na2SiO3溶液中滴入稀H2SO4 | 出现白色凝胶 | 说明非金属性:S>Si |
| B | 取少量金属钠在氧气中燃烧所得固体粉末于试管中,加3mL蒸馏水 | 有气体生成 | 固体粉末为Na2O2 |
| C | 将Zn(OH)2固体粉末加入过量NaOH溶液中,充分搅拌 | 固体溶解,得无色溶液 | Zn(OH)2既体现酸性又体现碱性 |
| D | 将Fe(NO3)2溶解在稀H2SO4中,再加入KSCN溶液 | 溶液呈血红色 | 说明Fe(NO3)2已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次